2022年山東省聊城市高考化學模擬試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題2分,共20分。每小題只有一個選項符合題目要求。
-
1.化學與生活、科技、社會發展息息相關。下列有關說法錯誤的是( )
A.我國二氧化碳合成淀粉的顛覆性技術有助于未來實現“碳中和” B.我國率先研制了預防新冠病毒的滅活疫苗,滅活疫苗利用了蛋白質變性原理 C.“天和”核心艙電推進系統中的腔體采用的氮化硼陶瓷屬于新型無機非金屬材料 D.地溝油變廢為寶是實現資源再利用的重要研究課題,地溝油和石蠟油的化學成分相同 組卷:30引用:1難度:0.8 -
2.下列物質應用正確的是( )
A.純堿用作治療胃酸過多的藥物 B.氯氣和消石灰用作生產漂白液的原料 C.二氧化硫用作葡萄酒生產過程中的添加劑 D.二氧化硅用作北斗芯片中的半導體材料 組卷:16引用:1難度:0.6 -
3.利用如圖裝置(夾持裝置省略)進行實驗,能達到實驗目的的是( )
A. 
檢驗1-溴丙烷和氫氧化鈉的醇溶液反應生成丙烯B. 
觀察鐵的吸氧腐蝕C. 
收集氮氣D. 
儀器中液體體積為9.40mL組卷:15引用:2難度:0.5 -
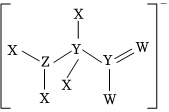 4.X、Y、Z、W為短周期主族元素,其原子序數依次增大,Y、Z、W位于同一周期,基態W原子最高能層電子數是基態Y原子最高能級電子數的3倍,它們形成的某陰離子的結構如圖所示。下列說法錯誤的是( )
4.X、Y、Z、W為短周期主族元素,其原子序數依次增大,Y、Z、W位于同一周期,基態W原子最高能層電子數是基態Y原子最高能級電子數的3倍,它們形成的某陰離子的結構如圖所示。下列說法錯誤的是( )A.離子半徑:X->Li+ B.第一電離能:Z>W>Y C.X、Y、W三種元素可以形成一元酸,也可以形成二元酸 D.由 X、Y、Z、W四種元素組成的化合物的水溶液均顯堿性 組卷:16引用:1難度:0.6 -
5.下列由實驗現象所得結論正確的是( )
A.用坩堝鉗夾住一小塊用砂紙仔細打磨過的鋁箔,在酒精燈上加熱,鋁箔熔化但不滴落,證明鋁的熔點很高 B.用pH試紙測得CH3COONa溶液的pH約為9,NaNO2溶液的pH約為8,證明HNO2酸性大于醋酸 C.向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,溶液由淺綠色變為棕黃色,證明H2O2的氧化性強于Fe3+ D.取三支試管各加入等量的己烷、苯、甲苯,再分別加入幾滴等量的酸性KMnO4溶液,微熱,僅盛有甲苯的試管中溶液褪色,證明苯環能使甲基更易被氧化 組卷:12引用:1難度:0.5 -
6.鎵(Ga)位于周期表中第四周期第IIIA族,與強酸、強堿溶液均能反應生成H2,是一種應用廣泛的金屬元素,可用于制造半導體材料氮化鎵、砷化鎵、磷化鎵等。同溫同壓下,0.1molGa分別與100mL濃度均為2mol/L的鹽酸和氫氧化鈉溶液充分反應,生成H2的體積分別為V1L和V2L。下列說法錯誤的是( )
A.V1:V2=2:3 B.轉移的電子數之比為V1:V2 C.消耗酸和堿的物質的量之比為3V1:V2 D.反應前后兩溶液的質量變化相等 組卷:27引用:1難度:0.6
三、非選擇題:本題共5小題,共60分。
-
19.甘草素(G)常用作糖果、糕點、啤酒、乳品、巧克力等生產中的食品添加劑。一種制備G的合成路線圖如圖:
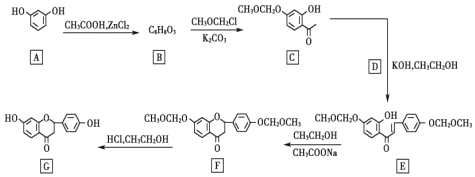
已知:RCHO+R′COCH3RCH=CHCOR′,其中R,R'為烴基或氫。回答下列問題:KOH,CH3CH2OH
(1)A的化學名稱為,A→B的反應類型為。
(2)D 與銀氨溶液混合共熱的化學方程式為。
(3)F 的分子式為;G中含有官能團的化學名稱為羥基、。
(4)C的同分異構體中,同時滿足如下條件的有種。
a.苯環上有4個取代基;
b.能與NaHCO3反應生成氣體;
c.能與3倍物質的量的NaOH反應;
d.分子中有6個氫原子化學環境相同;
其中核磁共振氫譜有5組峰,且峰面積之比為6:2:2:1:1的結構簡式為(任寫一種)。
(5)綜合上述信息,寫出由苯酚和乙醇制備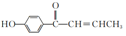 的合成路線(無機試劑任選)。 。組卷:99引用:1難度:0.3
的合成路線(無機試劑任選)。 。組卷:99引用:1難度:0.3 -
20.“雙碳“目標大背景下,研發CO2利用技術,降低空氣中的CO2含量成為研究熱點。
(1)CO2-CH4重整制CO的反應為:CO2(g)+CH4(g)?2CO(g)+2H2(g)△H
已知:
C(s)+2H2(g)═CH4(g)△H1=-74kJ/mol
CO2(g)═C(s)+O2(g)△H2=+394kJ/mol
C(s)+O2(g)═CO(g)△H3=-110kJ/mol12
則△H=。
在pMPa時,將CO2和CH4按物質的量之比為1:1充入密閉容器中,分別在無催化劑及ZrO2催化下反應相同時間,測得CO2的轉化率與溫度的關系如圖1所示: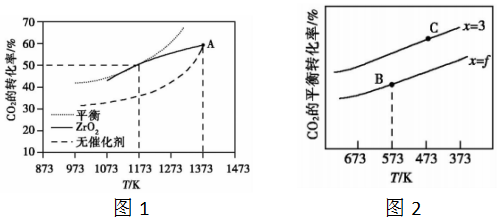
A點CO2轉化率相等的原因是。
(2)工業上CO2催化加氫制乙烯的反應為:2CO2(g)+6H2(g)?C2H4(g)+4H2O(g)。
①在恒容密閉容器中,起始壓強相同,CO2的平衡轉化率隨反應溫度、起始投料比[=x]的變化如圖2所示。則fn(H2)n(CO2)3(填“>“、“=“或“<“,下同);B、C兩點的化學平衡常數KBKC。
②當x=3時,保持體系壓強始終為0.2MPa,平衡時四種組分的物質的量分數y隨溫度T的變化如圖3所示。代表H2O(g)的變化曲線是;根據圖中D(390,0.12)點,列出該反應的平衡常數計算式Kp=(MPa)-3(以分壓表示,分壓=總壓×物質的量分數)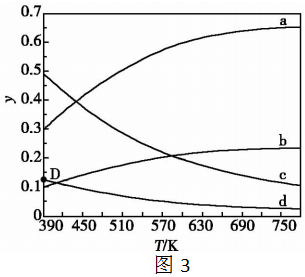
(3)我國化學工作者設計出一種電解裝置,該裝置在堿性條件下能將CO2和甘油(C3H8O3)分別轉化為合成氣(CO、H2)和甘油醛(C3H6O3)。電解過程中,陰極附近溶液的pH(填“增大“、“減小“或“不變“),陽極的電極反應式為。組卷:33引用:1難度:0.5


