2021-2022學年河北省石家莊市元氏四中高二(上)期中化學試卷
發布:2024/12/26 13:30:2
一.選擇題(共9小題,滿分27分,每小題3分)
-
1.下列變化過程中一定不存在化學能轉化為熱能的是( )
A. 
木材燃燒B. 
谷物釀酒C. 
干冰升華D. 
鞭炮燃放組卷:330引用:9難度:0.8 -
2.下列說法正確的是( )
A.1mol H2完全燃燒生成H2O(g)放出的熱量叫H2的燃燒熱 B.25℃、101 kPa時,1mol S和2 mol S的燃燒熱相等 C.已知S(s)+ O2(g)═SO3(g)△H=-269.8kJ/mol,則硫生成SO3的反應熱為269.8kJ/mol32D.25℃、101kPa時,碳的燃燒熱為-393.5kJ/mol 組卷:101引用:3難度:0.4 -
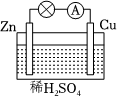 3.如圖所示是Zn和Cu形成的原電池,某實驗興趣小組做完實驗后,在讀書卡上的記錄如下。則卡片上的描述合理的是( )
3.如圖所示是Zn和Cu形成的原電池,某實驗興趣小組做完實驗后,在讀書卡上的記錄如下。則卡片上的描述合理的是( )
實驗后的記錄:
①Cu為正極,Zn為負極
②Cu極上有氣泡產生,發生還原反應
③向Cu極移動SO2-4
④若有0.5mol電子流經導線,則可產生0.25mol氣體
⑤電子的流向是:Cu→Zn
⑥正極反應式:Cu+2e-=Cu2+,發生氧化反應A.①②④ B.②④ C.②③④ D.③④⑤ 組卷:542引用:4難度:0.5 -
4.下列溶液在空氣中蒸干后能得到原溶質的是( )
A.KAl(SO4)2 B.Na2SO3 C.FeSO4 D.MgCl2 組卷:46引用:2難度:0.8 -
5.下列有關電解質的說法正確的是( )
A.某物質如果不是電解質,那它就是非電解質 B.電解質溶液在通電后發生電離 C.水溶液能導電的化合物不一定是電解質 D.將AgCl放入水中不能導電,故AgCl不是電解質 組卷:25引用:2難度:0.7 -
6.某溫度下,將2mol E和3mol F充入一密閉容器中,發生反應:aE(g)+F(g)?M(g)+N(g),平衡常數K等于1,在溫度不變的情況下將容器的體積擴大為原來的2倍,F百分含量不發生變化,則E的轉化率為( )
A.60% B.50% C.30% D.無法確定 組卷:455引用:3難度:0.7
三.填空題(共5小題,滿分41分)
-
18.某食用白醋是由醋酸與純水配制而成,用中和滴定的方法準確測定其中醋酸的物質的量濃度.實驗步驟:①配制500mL濃度約為0.1mol?L-1的NaOH溶液;②用KHC8H4O4標準溶液準確測定該NaOH溶液的濃度;③用已知準確濃度的NaOH溶液測定醋酸的濃度.
(1)稱量所需的NaOH固體置于大燒杯中,加入500mL蒸餾水,攪拌溶解.該配制步驟(填“可行”或“不可行”).
(2)稱量時NaOH在空氣中極易吸水,配制所得的NaOH溶液濃度通常比預期(填“小”或“大”),這是不能直接配制其標準溶液的原因.
(3)查閱白醋包裝說明,醋酸含量約為6g/100mL,換算成物質的量濃度約為mol?L-1,滴定前將白醋稀釋(填“10”或“100”)倍.(已知醋酸的相對分子質量為60)
(4)稀釋白醋時需要的儀器有燒杯、玻璃棒、滴管、酸式滴定管、.
(5)準確量取稀釋后的白醋20.00mL,置于250mL錐形瓶中,加水30mL,再滴加酚酞指示劑,用上述NaOH標準溶液滴定至即為終點.
重復滴定兩次,平均消耗NaOH標準溶液V mL(NaOH溶液濃度為c mol?L-1).
(6)原白醋中醋酸的物質的量濃度=mol?L-1.組卷:119引用:9難度:0.9
四.實驗題(共1小題,滿分16分,每小題16分)
-
 19.如圖是一個電化學原理的示意圖。填寫下列空白:
19.如圖是一個電化學原理的示意圖。填寫下列空白:
(1)請寫出甲、乙兩池的名稱。甲池是,乙池是。
(2)甲池中通入CH3OH的電極名稱是,電極反應方程式為;乙池中B(石墨)電極的名稱是。
(3)電解過程中,乙池溶液pH的變化為(“升高”“降低”或“不變”)。
(4)當乙池中A(Fe)極的質量增加4.32g時,甲池中理論上消耗O2mL(標準狀況下)。
(5)若乙池中的AgNO3換成一定量CuSO4溶液,通電一段時間后,向所得的溶液中加入0.05mol Cu(OH)2后恰好恢復到電解前的濃度和pH,則電解過程中轉移的電子數為mol(忽略溶液體積的變化)。組卷:322引用:4難度:0.5


