2008年湖南省益陽市南縣九年級化學知識競賽復賽試卷
發布:2024/4/20 14:35:0
一、選擇題(每題只有一個選項符合題意,每題2分,共20分)
-
1.實驗測知,化合物均有固定的組成.現有 H(+1)、O(-2)、C(+4)、Ca(+2)四種元素,按指定化合價最多可以組成化合物的種數是( )
A.5 B.6 C.7 D.8 組卷:44引用:1難度:0.9 -
2.碳元素所形成的化合物的種類是所有化合物中最多的.已知碳元素與某非金屬元素R可形成化合物CRX,且知在一個CRX分子中各原子的電子數之和為74,則R的原子序數和X的值分別是( )
A.16,2 B.35,4 C.17,4 D.26,3 組卷:19引用:5難度:0.9 -
3.某一飽和硫酸銅溶液中,加入含18O的帶標記的無水硫酸銅粉末a克,則如果保持溫度不變,其結果是( )
A.無水硫酸銅不再溶解,a克粉末不變 B.溶液中可找到帶標記的SO42-,而且白色粉末變為藍色晶體,其質量大于a克 C.溶液中可找到帶標記的SO42-,而且白色粉末變為藍色晶體,其質量小于a克 D.溶液中溶解與結晶體達到平衡狀態,有部分帶標記的SO42-進入溶液,但固體粉末仍是a克 組卷:55引用:2難度:0.9 -
4.化學概念在邏輯上存在如圖所示關系,對下列概念間的關系說法正確的是( )
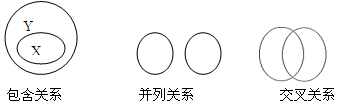
A.純凈物與混合物屬于包含關系 B.化合物與氧化物屬于包含關系 C.單質與化合物屬于交叉關系 D.氧化反應與化合反應屬于并列關系 組卷:237引用:130難度:0.7 -
 5.某同學用自己調節好的托盤天平稱量某固體藥品,其稱量如圖所示.下列對該圖所示稱量的說法正確的是( )
5.某同學用自己調節好的托盤天平稱量某固體藥品,其稱量如圖所示.下列對該圖所示稱量的說法正確的是( )A.該稱量方法是不規范的,藥品的實際質量為25.2g B.該稱量方法是不規范的,藥品的實際質量為24.8g C.該稱量方法是規范的,藥品的實際質量為25.2g D.該稱量方法是規范的,藥品的實際質量為24.8g 組卷:33引用:11難度:0.9 -
6.下列物質在pH=1的溶液中能夠大量共存,且形成無色溶液的是( )
A.CaCl2、NaOH、KNO3、Mg(NO3)2 B.FeCl3、H2SO4、KCl、NaNO3 C.Na2CO3、KCl、NH4NO3、Na2SO4 D.Mg(NO3)2、Na2SO4、NH4Cl、KNO3 組卷:50引用:12難度:0.9 -
7.研究物質的變化時可使用具有放射性的18O作為“示蹤原子”.科學家希爾和尼爾研究證明,光合作用的通式應更合理地表達為:6CO2+12H218O
C6H12O6+6H2O+618O2在光照充分的環境里,將一種植物--黑藻放入含有“示蹤原子”18O的水中一段時間后分析“示蹤原子”,最有可能是( )葉綠體光A.在植物體周圍的空氣中發現 B.在植物體內的葡萄糖(C6H12O6)中發現 C.在植物體內的淀粉和蛋白質中發現 D.無法確定示蹤原子在什么地方出現 組卷:113引用:13難度:0.7 -
8.已知反應2H2S+SO2=3S(固體)+2H2O,在常溫下向容積為10L的真空容器內通入34ag H2S氣體和64bg SO2氣體(a、b均為≤5的正整數),充分反應后容器內的氣體可能達的最大密度為( )
A.49g/L B.28.8g/L C.25.6g/L D.10.2g/L 組卷:42引用:3難度:0.5 -
 9.如圖所示,向小試管中分別加入一定量的下列物質,能使U形管右側紅墨水的液面明顯上升的是( )
9.如圖所示,向小試管中分別加入一定量的下列物質,能使U形管右側紅墨水的液面明顯上升的是( )A.濃硫酸 B.NaCl溶液 C.蔗糖溶液 D.氯化鈣固體 組卷:42引用:2難度:0.9
四、實驗題(每空2分,共18分)
-
28.如右圖,點燃階梯上的蠟燭,將玻璃罩倒扣在水槽內.請你根據已學的知識和經驗做出如下猜想:

(1)當玻璃罩的容積較大時,將觀察到階梯上點燃的蠟燭按(填“先上后下”或“先下后上”)熄滅,其原因是.
(2)當玻璃鐘罩的容積較小時.將觀察到點燃階梯上的蠟燭按先上后下順序熄滅,其原因是.組卷:47引用:1難度:0.5
五、計算題(共8分)
-
29.煤是重要的化工原料,用煤做燃料,不僅是極大的浪費,而且因煙煤中含有硫的化合物(如FeS2),燃燒時會生成SO2氣體造成環境污染.若煤中含FeS25%,燃燒時,有90%的硫的化合物轉化為二氧化硫,被排放入大氣之中.燃燒時化學反應方程式如下:
4FeS2+11O22Fe2O3+8SO2高溫
(1)我國曾計劃從2001年至2005年,將SO2的排放量從1995萬噸降為1800萬噸,意味著2005年比2001年應少燃燒這種煤多少萬噸?
(2)若以SO2形成硫酸酸雨計算,2005年雨水中減少排放硫酸多少萬噸?組卷:22引用:2難度:0.1


