2023年北京四中高考化學零模試卷
發布:2024/4/20 14:35:0
一、第一部分本部分共14題,每題3分,共42分。在每題列出的四個選項中,選出最符合題目要求的一項。
-
1.近年來,我國航空航天事業成果顯著。下列成果所涉及的材料為金屬材料的是( )
A.“天宮二號”航天器使用的質量輕、強度高的材料——鈦合金 B.“北斗三號”導航衛星使用的太陽能電池材料——砷化鎵 C.“長征五號”運載火箭使用的高效燃料——液氫 D.“C919”飛機機身使用的復合材料——碳纖維和環氧樹脂 組卷:139引用:8難度:0.7 -
2.下列物質的應用中,利用了氧化還原反應的是( )
A.用石灰乳脫除煙氣中的SO2 B.用明礬[KAl(SO4)2?12H2O]處理污水 C.用鹽酸去除鐵銹(主要成分Fe2O3?xH2O) D.用84消毒液(有效成分NaClO)殺滅細菌 組卷:689引用:13難度:0.7 -
3.下列化學用語或圖示表達不正確的是( )
A.乙炔的結構簡式:HC≡CH B.順-2-丁烯的分子結構模型: 
C.基態Si原子的價層電子的軌道表示式: 
D.Na2O2的電子式:  組卷:133引用:8難度:0.8
組卷:133引用:8難度:0.8 -
4.下列方程式與所給事實不相符的是( )
A.加熱NaHCO3固體,產生無色氣體:2NaHCO3 Na2CO3+H2O+CO2↑△B.過量鐵粉與稀硝酸反應,產生無色氣體:Fe+ +4H+=Fe3++NO↑+2H2ONO-3C.苯酚鈉溶液中通入CO2,出現白色渾濁: 
D.乙醇、乙酸和濃硫酸混合加熱,產生有香味的油狀液體:CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O△濃硫酸組卷:435引用:5難度:0.5 -
5.硫酸鹽(含
、SO2-4)氣溶膠是PM2.5的成分之一。近期科研人員提出了霧霾微顆粒中硫酸鹽生成的轉化機理,其主要過程示意圖如圖。下列說法不正確的是( )HSO-4
A.該過程有H2O參與 B.NO2是生成硫酸鹽的氧化劑 C.硫酸鹽氣溶膠呈酸性 D.該過程沒有生成硫氧鍵 組卷:594引用:18難度:0.7 -
6.一定溫度下,反應I2(g)+H2(g)?2HI(g)在密閉容器中達到平衡時,測得c(I2)=0.11mmol?L-1,c(H2)=0.11mmol?L-1,c(HI)=0.78mmol?L-1。相同溫度下,按下列4組初始濃度進行實驗,反應逆向進行的是( )
(注:1mmol?L-1=10-3mol?L-1)A B C D c(I2)/mmol?L-1 1.00 0.22 0.44 0.11 c(H2)/mmol?L-1 1.00 0.22 0.44 0.44 c(HI)/mmol?L-1 1.00 1.56 4.00 1.56 A.A B.B C.C D.D 組卷:140引用:4難度:0.5
二、第二部分本部分共5題,共58分。
-
18.香豆素類化合物在藥物中應用廣泛。香豆素類化合物W的合成路線如圖。

已知:
(1)A→B的化學方程式是。
(2)D的分子式是。
(3)條件①是。
(4)F的結構簡式是
(5)1molJ可以生成2molK,J的結構簡式是。
(6)下列說法不正確的是(填序號)。
a.可以用酸性KMnO4溶液鑒別E和G
b.G可以發生加聚反應、還原反應和取代反應
c.1mol P最多可以和5mol H2反應
(7)M為線型不穩定分子,M→P經過兩步反應,R苯環上的一氯代物有3種。
①R的結構簡式是。
②R→P的化學反應類型是。組卷:97引用:3難度:0.4 -
19.某小組探究CuSO4溶液、FeSO4溶液與堿的反應,探究物質氧化性和還原性的變化規律。
將一定濃度CuSO4溶液,飽和FeSO4混合溶液加入適量氨水,產生紅褐色沉淀,經檢驗,紅褐色沉淀含Fe(OH)3。
(1)分析Fe(OH)3產生的原因:O2氧化所致。驗證:向FeSO4溶液中滴入氨水,生成的白色沉淀迅速變為灰綠色,一段時間后有紅褐色沉淀生成。
①生成白色沉淀的離子方程式是。
②產生紅褐色沉淀:4Fe(OH)2+O2+2H2O═4Fe(OH)3。電極反應式:
還原反應:O2+2H2O+4e-═4OH-。
氧化反應:。
(2)提出問題:產生Fe(OH)3的原因可能是Cu2+氧化所致。
驗證如下(溶液A:飽和FeSO4溶液 +CuSO4溶液;已排除空氣的影響):
①Ⅰ中可能產生Cu,運用氧化還原反應規律分析產生Cu的合理性:序號 實驗 試劑 現象 Ⅰ 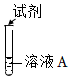
氨水 生成沉淀,一段時間后,產生紅褐色沉淀和灰黑色固體物質 Ⅱ 水 溶液無明顯變化 。
②檢驗:濾出Ⅰ中不溶物,用稀H2SO4溶解,未檢出Cu。分析原因:
ⅰ.Ⅰ中未生成Cu。
ⅱ.Ⅰ中生成了Cu。由于(用離子方程式表示),因此未檢出Cu。
(3)設計實驗(Ⅲ)確認CuSO4的作用(已排除空氣的影響),裝置示意圖如圖所示。
①補全電化學裝置示意圖。經檢驗,實驗中產生了Fe(OH)3、Cu。
②Ⅱ、Ⅲ中均含Cu2+。Ⅲ中產生了Cu,Ⅱ中未產生Cu,試解釋原因。
(4)CH3CHO分別與AgNO3溶液、銀氨溶液混合并加熱,CH3CHO與AgNO3溶液混合物明顯現象,但與銀氨溶液混合能產生銀鏡。試解釋原因:。組卷:117引用:6難度:0.6


