2022-2023學年重慶市縉云教育聯盟高二(下)期末化學試卷
發布:2024/8/3 8:0:9
-
1.下列實驗,能得到溶液的是( )
A. 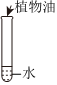
B. 
C. 
D. 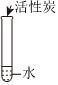 組卷:74引用:1難度:0.8
組卷:74引用:1難度:0.8 -
2.下列關于糖的說法錯誤的是( )
A.淀粉是一種天然高分子化合物 B.糖都能水解 C.纖維素沒有甜味 D.糖類是人體內能量的主要來源之一 組卷:383引用:8難度:0.9 -
3.在一定溫度下A(g)+3B(g)?2C(g)達平衡的標志是( )
A.物質A、B、C的分子個數比為1:3:2 B.單位時間內生成A、C的物質的量之比為1:2 C.單位時間內生成A、B的物質的量之比為1:3 D.反應速率v(A)= =v(B)3v(C)2組卷:73引用:1難度:0.7 -
4.X、Y、Z、W為周期表中前20號元素,原子序數依次增大,W、Y為金屬元素,X原子的最外層電子數是次外層電子數的3倍,Y、Z位于同周期,Z單質是一種良好的半導體。W單質能與冷水劇烈反應,Y、Z原子的最外層電子數之和與X、W原子的最外層電子數之和相等。下列說法正確的是( )
A.原子半徑:W>Y>Z>X B.X與Z形成的化合物可導電 C.Y、Z、W的最高價氧化物的水化物中,堿性最強的為Y D.W可從Y的鹽溶液中置換出Y 組卷:19引用:4難度:0.6 -
5.下列各組中的兩種物質在溶液中的反應,可用同一離子方程式表示的是( )
A.Cu(OH)2+HCl;Cu(OH)2+CH3COOH B.NaHCO3+H2SO4;Na2CO3+HCl C.NaHSO4+NaOH;H2SO4+NaOH D.BaCl2+H2SO4;Ba(OH)2+H2SO4 組卷:60引用:3難度:0.6 -
6.下列關于鈉的敘述正確的是( )
A.鈉在自然界中存在游離態 B.鈉是一種灰色的固體 C.鈉可以保存在煤油中 D.鈉著火時可以用水撲滅 組卷:80引用:3難度:0.7
-
17.過氧化鈣常用作殺菌劑及封閉膠泥的快干劑,難溶于水,溶于酸生成過氧化氫。以大理石(含有少量氧化亞鐵和氧化鐵雜質)為原料制備過氧化鈣的工藝流程如圖所示。
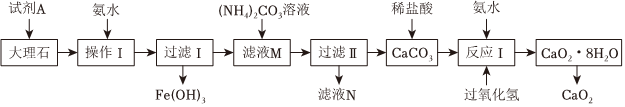
回答下列問題:
(1)操作Ⅰ的目的是調節溶液的pH,使鐵元素完全沉淀,則試劑A最好選用(填標號)
a.鹽酸
b.硝酸
c.鹽酸和過氧化氫
d.硫酸
(2)測得濾液M中Ca2+的物質的量濃度為0.56mol?L-1,若加入等體積的(NH4)2CO3溶液時CaCO3開始沉淀,則(NH4)2CO3的物質的量濃度為【已知Ksp(CaCO3)=2.8×10-9】。
(3)反應Ⅰ是放熱反應。不同濃度的H2O2溶液對反應生成CaO2產率的影響如下表:
分析題給信息,解釋H2O2的濃度大于20%后CaO2產率反而減小的原因:H2O2的濃度/% 5 10 15 20 25 30 CaO2的產率/% 62.40 63.10 63.20 64.54 62.42 60.40 。
(4)制備所得的過氧化鈣中常含有CaO雜質,實驗室可按以下步驟測定CaO2的質量分數:
步驟1:準確稱取0.3900g過氧化鈣樣品,置于250mL的錐形瓶中;
步驟2:加入10mL蒸餾水和20mL磷酸,振蕩使樣品完全溶解;
步驟3:用0.1000mol?L-1的酸性KMnO4溶液滴定至終點,記錄數據;
步驟4:平行測定3次(數據記錄見下表),計算試樣中CaO2的質量分數
已知:上述實驗過程中反應關系為CaO2~H2O2,5H2O2~2KMnO4。實驗 1 2 3 V(酸性KMnO4溶液)/mL 19.50 19.48 19.52
①步驟3判斷滴定達到終點的現象是。
②由表中數據可知,該樣品中CaO2的質量分數為%。若實驗時剛洗凈的滴定管未用酸性KMnO4溶液潤洗,則測定的CaO2的質量分數會(填“偏高”“偏低”或“無影響”)。組卷:35引用:3難度:0.5 -
 18.Ⅰ.將氣體A、B置于固定容積為2L的密閉容器中,發生如下反應:3A(g)+B(g)?2C(g)+2D(g),反應進行到10s末,達到平衡,測得A的物質的量為1.8mol,B的物質的量為0.6mol,C的物質的量為0.8mol,則:
18.Ⅰ.將氣體A、B置于固定容積為2L的密閉容器中,發生如下反應:3A(g)+B(g)?2C(g)+2D(g),反應進行到10s末,達到平衡,測得A的物質的量為1.8mol,B的物質的量為0.6mol,C的物質的量為0.8mol,則:
(1)用C表示10s內正反應的平均反應速率為:。
(2)反應前A的物質的量濃度是:。
(3)10s末,生成物D的濃度為。
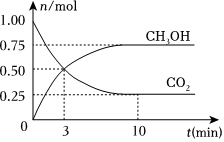
Ⅱ.在體積為2L的密閉容器中(體積不變),充入1molCO2和3molH2,一定條件下發生反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),測得CO2和CH3OH(g)的物質的量隨時間變化如圖所示:
(1)從反應開始到10min,氫氣的平均反應速率v(H2)=。
(2)下列說法正確的是。
A.當t=0時,v(逆)=0
B.進行到3min時,正反應速率和逆反應速率相等
C.10min后容器中壓強不再改變
D.3min前v(正)>v(逆),3min后v(正)<v(逆)組卷:6引用:1難度:0.5


