人教版選修4《第4章 電化學基礎》2009年單元測試卷(湖南省長沙市長郡中學)(1)
發布:2024/4/20 14:35:0
一、選擇題:
-
1.下面有關電化學的圖示,完全正確的是( )
A. 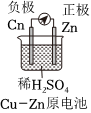
B. 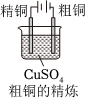
C. 
D. 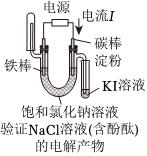 組卷:67引用:18難度:0.7
組卷:67引用:18難度:0.7 -
2.在原電池和電解池的電極上所發生的反應,同屬氧化反應或同屬還原反應的是( )
A.原電池正極和電解池陽極所發生的反應 B.原電池正極和電解池陰極所發生的反應 C.原電池負極和電解池陽極所發生的反應 D.原電池負極和電解池陰極所發生的反應 組卷:38引用:10難度:0.5 -
3.關于電解NaCl水溶液,下列敘述正確的是( )
A.電解時在陽極得到氯氣,在陰極得到金屬鈉 B.若在陽極附近的溶液中滴入KI溶液,溶液呈棕色 C.若在陰極附近的溶液中滴入酚酞試液,溶液呈無色 D.電解一段時間后,將全部電解液轉移到燒杯中,充分攪拌后溶液呈中性 組卷:212引用:56難度:0.7 -
4.一種新型燃料電池,它是用兩根金屬做電極插入KOH溶液中,然后向兩極上分別通甲烷和氧氣,其電池反應為:X極CH4+10OH--8e-═CO32-+7H2O;Y極:4H2O+2O2+8e-═8OH-.下列關于此燃料電池的有關說法中錯誤的是( )
A.通過甲烷的電極(X)為電池的負極,通過氧氣的電極(Y)為電池正極 B.放電一段時間后,電解質溶液中KOH的物質的量改變 C.在標準狀況下,通過5.6L氧氣,完全反應后有1.0mol的電子發生轉移 D.放電時,通過甲烷的一極附近的pH升高 組卷:39引用:5難度:0.7 -
5.100mL濃度為2mol?L-1的鹽酸跟過量的鋅片反應,為了加快反應速率又不影響生成氫氣的總量,可采用的方法是( )
A.加入適量的6 mol?L-1的鹽酸 B.用鋅粉代替鋅片 C.加入適量蒸餾水 D.加入適量的氯化鈉溶液 組卷:11引用:2難度:0.7 -
6.原電池的電極名稱不僅與電極材料的性質有關,也與電解質溶液有關.下列說法中不正確的是( )
A.由Al、Cu、稀H2SO4組成原電池,其負極反應式為:Al-3e-=Al3+ B.由Mg、Al、NaOH溶液組成原電池,其負極反應式為:Al-3e-+4OH-=AlO2-+2H2O C.由Fe、Cu、FeCl3溶液組成原電池,其負極反應式為:Cu-2e-=Cu2+ D.由Al、Cu、濃硝酸組成原電池,其負極反應式為:Cu-2e-=Cu2+ 組卷:553引用:47難度:0.7
二、填空題:
-
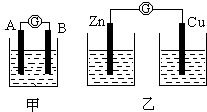 17.某同學設計實驗探究構成原電池的條件,裝置如下:
17.某同學設計實驗探究構成原電池的條件,裝置如下:
實驗一:實驗探究電極的構成<甲圖>
①A、B 兩極均選用石墨作電極,發現電流計指針不偏轉;②A、B 兩極均選用銅片作電極,發現電流計指針不偏轉;③A極用鋅片,B極用銅片,發現電流計指針向左偏轉;④A極用鋅片,B極用石墨,發現電流計指針向左偏轉.
結論一:.
實驗二:探究溶液的構成<甲圖,A極用鋅片,B極用銅片)
①液體采用無水乙醇,發現電流計指針不偏轉;
②改用硫酸溶液,發現電流計指針偏轉,B極上有氣體產生.
結論二:.
實驗三:對比實驗,探究乙圖裝置能否構成原電池
將鋅、銅兩電極分別放入稀硫酸溶液中,發現鋅片上有氣泡產生,銅片上無明顯現象,電流計指針不發生偏轉.
結論三:.
思考:對該同學的實驗,同學乙提出了如下疑問,請你幫助解決.
(1)在甲圖裝置中,若A 為鎂片,B為鋁片,電解質溶液為NaOH溶液,電流計的指針應向偏轉.
(2)一根金屬絲兩端分別放在圖乙的兩個燒杯之中,電流計指針(填“能”或“不能”)偏轉.組卷:54引用:3難度:0.5 -
18.右圖所示裝置中,甲、乙、丙三個燒杯依次分別盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,電極均為石墨電極.

(1)接通電源,經過一段時間后,測得丙中K2SO4濃度為10.47%,乙中c電極質量增加.據此回答問題:
①電源的N端為極;
②電極b上發生的電極反應為;
③列式計算電極b上生成的氣體在標準狀況下的體積:
④電極c的質量變化是g;
⑤電解前后各溶液的酸、堿性大小是否發生變化,簡述其原因:
甲溶液;
乙溶液;
丙溶液;
(2)如果電解過程中銅全部析出,此時電解能否繼續進行,為什么?.組卷:266引用:24難度:0.3


