2020-2021學年黑龍江省哈爾濱七十三中高二(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題含18小題,每題3分,共54分。每題只有一個選項符合題意)
-
1.下列對物質用途的描述中錯誤的是( )
A.鈉、鉀合金可用于作原子反應堆導熱劑 B.BaCO3可用作鋇餐內服藥劑 C.鎂常用于制造信號彈和焰火 D.氧化鐵可制成防銹油漆 組卷:0引用:2難度:0.7 -
2.Na2O2是一種既有氧化性、又有還原性的物質,當Na2O2與某物質Q發生反應并且有氧氣生成時,下列有關說法正確的是( )
A.Q一定是氧化劑 B.當有1 mol O2生成時轉移電子4 mol C.O2一定是氧化產物 D.Na2O2不可能發生還原反應 組卷:23引用:11難度:0.7 -
3.下列關于金屬及其化合物,說法錯誤的是( )
A.黑色金屬材料包括鐵、鉻、錳及其化合物 B.明礬為金屬鋁的化合物,可用作凈水劑 C.俗語“真金不怕火煉”說明某些金屬在高溫的條件下也不與氧氣發生反應 D.金屬鈉具有強還原性,可與TiCl4反應制取金屬Ti 組卷:46引用:3難度:0.5 -
4.下列通過制取硫酸鋁、氫氧化鋁獲得氧化鋁的裝置和原理能達到實驗目的的是( )
A. 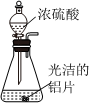
制硫酸鋁B. 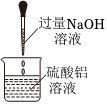
制氫氧化鋁C. 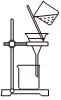
過濾氫氧化鋁D. 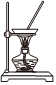
灼燒制氧化鋁組卷:56引用:8難度:0.9 -
5.由Fe2O3、Fe、CuO、C、Al中的幾種物質組成的混合粉末,取樣品進行下列實驗(部分產物略去).關于混合粉末的組成判斷正確的是( )
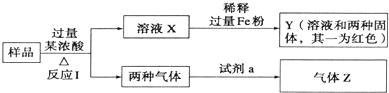
A.一定含CuO和C B.一定含Fe2O3、CuO和C C.一定含CuO和C,一定不含Al D.氣體Z為純凈物 組卷:68引用:7難度:0.7 -
6.某溶液中含有HCO3-、CO32-、SO32-、Na+、NO3-五種離子.若向其中加入過氧化鈉粉末充分反應后(溶液體積變化忽略不計),溶液中離子濃度保持不變的是( )
A.CO32-、NO3- B.NO3- C.SO32-、NO3- D.CO32-、NO3-、Na+ 組卷:28引用:5難度:0.9 -
7.下列關于金屬或金屬化合物的說法錯誤的是( )
A.Al2O3和Al(OH)3均為兩性物質,Al是兩性元素 B.不用試劑即可鑒別Na2CO3溶液和NaHSO4溶液 C.檢驗溶液中的Fe2+,可向溶液中加入KSCN溶液,此時溶液顏色無變化,之后向其中加入少量氯水,溶液變為紅色 D.過量的鐵與稀硝酸溶液反應離子方程式:3Fe+8H++2 ═3Fe2++4H2O+2NO↑NO-3組卷:2引用:2難度:0.7
二、第Ⅱ卷非選擇題(共46分)
-
21.為了保護環境,充分利用資源,常常將工業制硫酸的硫鐵礦燒渣(鐵主要以Fe2O3存在)轉變成重要的化工原料FeSO4(反應條件略)。
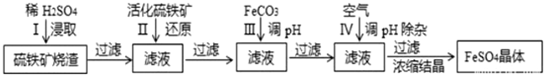
活化硫鐵礦還原Fe3+的主要反應為:FeS2+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4,不考慮其他反應。請回答下列問題:
(1)第Ⅰ步H2SO4與Fe2O3反應的離子方程式是。
(2)檢驗第Ⅱ步中Fe3+是否完全還原,應選擇(填字母編號)。
A.KMnO4溶液
B.淀粉-KI溶液
C.KSCN溶液組卷:0引用:1難度:0.7 -
22.硫、鋅及其化合物用途非常廣泛。回答下列問題:
(1)基態鋅原子的價電子排布式為;鋅的第二電離能I2(Zn)小于銅的第二電離能I2(Cu),其原因是。
(2)O和S處于同一主族,H2O及H2S中,中心原子的雜化方式相同,鍵長及鍵角如圖1。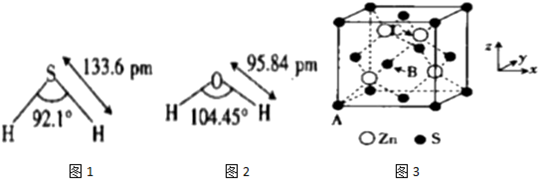
①H2O分子中的鍵長比H2S中的鍵長短,其原因是。
②H2O分子中的鍵角∠HOH比H2S分子中的鍵角∠HSH大,其原因是。
(3)單質硫與熱的NaOH濃溶液反應的產物之一為Na2S3,的空間構型為S2-3。
(4)噻吩( )廣泛應用于合成醫藥、農藥、染料工業。
)廣泛應用于合成醫藥、農藥、染料工業。
①噻吩分子中的大π鍵可用符號表示,其中m代表參與形成大π鍵的原子數,n代表參與形成大π鍵的電子數(如苯分子中的大π鍵可表示為πmn),則噻吩分子中的大π鍵應表示為。
②噻吩的沸點為84℃,吡咯(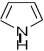 )的沸點在129℃~131℃之間,后者沸點較高,其原因是。
)的沸點在129℃~131℃之間,后者沸點較高,其原因是。
(5)硫化鋅是一種半導體材料,其晶胞結構如圖(3)所示。
①已知A點的原子坐標參數為(0,0,0);B點的原子坐標參數為(,0,12),則C點的原子坐標參數為12。
②硫化鋅晶體的密度為4.05g?cm-3,晶胞邊長為anm,設NA為阿伏加德羅常數的數值,則a=(列出計算表達式即可)。組卷:12引用:1難度:0.6


