2021-2022學年山東省濰坊市昌樂二中高三(上)月考化學試卷(10月份)
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題2分,共20分。每小題只有一個選項符合題目要求。
-
1.化學與生活密切相關,下列有關說法錯誤的是( )
A.高純度的二氧化硅廣泛用于制作光導纖維,光導纖維遇強堿會“斷路” B.《本草經集注》中關于鑒別硝石(KNO3)和樸硝(Na2SO4)的記載:“以火燒之,紫青煙起,乃真硝石也”,該方法應用了焰色反應 C.用漂粉精和潔廁靈(主要成分是鹽酸) 混合后的濃溶液清洗馬桶效果更佳 D.明朝醫學家李時珍在《本草綱目》中對(KNO3)的描述如下:“(火藥)乃焰硝、硫磺、杉木炭所合,以為烽燧銃機諸藥者”,利用了KNO3的氧化性 組卷:13引用:2難度:0.7 -
2.濃硫酸與下列物質作用時,只表現強氧化性的是( )
①紅熱的木炭
②H2S氣體
③Cu
④FeO
⑤NH3
⑥使木材炭化
⑦CuSO4?5H2O
⑧對鐵、鋁的鈍化A.①② B.①②⑧ C.①②④ D.①②⑤ 組卷:54引用:1難度:0.6 -
3.某溶液中含有HCO3-、SO32-、CO32-、CH3COO-四種陰離子。向其中加入足量的Na2O2固體后,溶液中離子濃度基本保持不變的是(假設溶液體積無變化)( )
A.CH3COO- B.SO32- C.CO32- D.HCO3- 組卷:216引用:57難度:0.7 -
4.下列各項操作中發生先沉淀后溶解現象的是( )
A.向飽和Na2CO3溶液中通入過量CO2 B.向Fe(OH)3膠體中逐滴滴加入過量稀H2SO4 C.向Ba(NO3)2溶液中通入過量SO2 D.向CaCl2溶液中通入過量CO2 組卷:33引用:2難度:0.5 -
5.下列反應的離子方程式書寫正確的是( )
A.氯化鐵溶液中通入硫化氫氣體2Fe3++S2-═2Fe2++S↓ B.NaHSO4溶液與Ba(OH)2溶液混合呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O C.用漂白粉溶液吸收尾氣中SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO D.水玻璃中通入過量二氧化碳:Na2SiO3+CO2+H2O=2Na++CO32-+H2SiO3↓ 組卷:12引用:1難度:0.6 -
6.關于下列各實驗裝置的敘述中,不正確的是( )
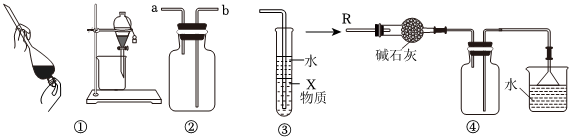
A.裝置①可用于分離C2H5OH和H2O的混合物 B.裝置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等氣體 C.裝置③中X若為CCl4,可用于吸收NH3或HCl,并防止倒吸 D.裝置④可用于干燥、收集NH3,并吸收多余的NH3 組卷:157引用:45難度:0.9
二.(非選擇題,共60分)
-
19.(1)已知充分燃燒a g乙炔(C2H2)氣體時生成1mol二氧化碳氣體和液態水,并放出熱量bkJ,則乙炔燃燒的熱化學方程式
。
(2)若已知:2H2(g)十O2(g)=2H2O(g)△H1=-Q1kJ?mol-1
2H2(g)十O2(g)=2H2O (l)△H2=-Q2kJ?mol-1
則H2O(g)=H2O (l)的△H=kJ?mol-1(用Q1、Q2表示)。
(3)蓄電池是一種反復充電、放電的裝置。有一種蓄電池在充電和放電時發生的反應如下:
NiO2+Fe+2H2OFe(OH)2+Ni(OH)2。放電充電
此蓄電池在充電時,電池負極應與外加電源的極連接,電極反應式為:。
(4)已知肼(N2H4)在氧氣中完全燃燒生成氮氣和水。肼—空氣燃料電池是一種堿性燃料電池,電解質溶液是20%~30%的KOH溶液。肼—空氣燃料電池放電時,負極的電極反應式。
(5)以丙烷為燃料制作新型燃料電池,電池的正極通入O2和CO2,負極通入丙烷,電解質是熔融碳酸鹽。放電時,CO32-移向電池的(填“正”或“負”)極;負極反應為。組卷:7引用:1難度:0.7 -
20.工業上利用廢鐵屑(含少量氧化鋁、氧化鐵等)生產堿式硫酸鐵[Fe(OH)SO4]的工藝流程如圖:
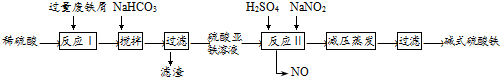
已知:部分陽離子以氫氧化物形式沉淀時溶液的pH如下表:
回答下列問題:沉淀物 Fe(OH)3 Fe(OH)2 Al(OH)3 開始沉淀 2.3 7.5 3.4 完全沉淀 3.2 9.7 4.4
(1)反應Ⅰ中發生的氧化還原反應的化學方程式為.
(2)加入少量NaHCO3的目的是調節pH,使溶液中的(填“Fe3+”、“Fe2+”或“Al3+”)沉淀.該工藝流程中“攪拌”的作用是.
(3)反應Ⅱ的離子方程式為.在實際生產中,反應Ⅱ常同時通入O2以減少NaNO2的用量,O2與NaNO2在反應中均作.若參與反應的O2有11.2L(標準狀況),則相當于節約NaNO2的物質的量為.
(4)堿式硫酸鐵溶于水后產生的Fe(OH)2+離子,可部分水解生成Fe2(OH)42+聚合離子.該水解反應的離子方程式為.
(5)在醫藥上常用硫酸亞鐵與硫酸、硝酸的混合液反應制備堿式硫酸鐵.根據我國質量標準,產品中不得含有Fe2+及.為檢驗所得產品中是否含有Fe2+,應使用的試劑為NO-3(填字母).
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.組卷:23引用:6難度:0.5


