2021-2022學年江蘇省蘇州市工業園區景城學校九年級(上)調研化學試卷
發布:2024/8/8 8:0:9
-
1.化學與生活密切相關,下列說法正確的是( )
A.地溝油經化學方法處理制成航空燃油,實現變廢為寶 B.食品添加劑符合國家許可,制作食品過程中可隨意添加 C.鈣是人體必須的常量元素,吃得越多越好 D.生活污水不是化工廢水,可向江河湖泊里任意排放 組卷:1引用:1難度:0.5 -
2.垃圾分類回收有利于保護環境、節約資源。下列可回收垃圾中屬于金屬材料的是( )
A.玻璃瓶 B.塑料袋 C.易拉罐 D.廢報紙 組卷:334引用:11難度:0.7 -
3.如圖所示實驗操作正確的是( )
A. 
驗滿氧氣B. 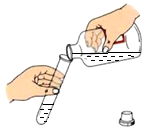
傾倒液體C. 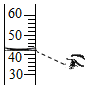
讀取液體體積D. 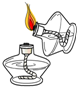
點燃酒精燈組卷:20引用:12難度:0.9 -
4.下列物質是由離子構成的是( )
A.氯氣 B.氯化鈉 C.二氧化碳 D.水銀 組卷:17引用:5難度:0.6 -
5.下列對事實的解釋合理的是( )
A.干冰能形成云霧繚繞的效果——干冰升華形成白色氣體 B.鉛筆能寫出字跡——鉛質地較軟并且為黑色 C.分離液態空氣獲得氧氣——液氧的沸點比液氮低 D.水電解能生成氫氣和氧氣——水中含有氫元素和氧元素 組卷:6引用:1難度:0.5 -
6.將A物質25g,B物質56g在一定條件下反應,反應后的物質中仍有10g A,且B完全反應,生成C的質量為44g.若A、B、C、D的相對分子質量分別為30、32、44、18,則該反應的化學方程式為( )
A.A+2B═2C+D B.2A+2B═C+D C.2A+7B═4C+6D D.A+2B═C+2D 組卷:145引用:5難度:0.7 -
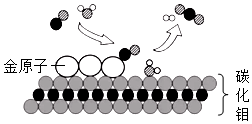 7.如圖所示為碳化鉬(Mo2C)負載金原子組成的高效催化體系催化CO和H2O反應的微觀示意圖,下列說法正確的是( )
7.如圖所示為碳化鉬(Mo2C)負載金原子組成的高效催化體系催化CO和H2O反應的微觀示意圖,下列說法正確的是( )A.圖中有三種化合物 B.反應中金原子對CO起到吸附催化作用 C.反應前后分子種類和數目均不變 D.反應中CO與H2O質量比為14:18 組卷:5引用:1難度:0.5 -
8.乳化劑是表面活性劑(surfactant)的一種,使目標溶液表面張力顯著下降,例如肥皂中的硬脂酸鈉(C17H35COONa)改變液體表面張力起到乳化作用從而除去油污,下列說法正確的是( )
A.從微觀上看:硬脂酸鈉含有18個碳原子、35個氫原子、2個氧原子和1個鈉離子 B.從質量上看:硬脂酸鈉中碳、氧兩種元素的質量比為9:1 C.從宏觀上看:硬脂酸鈉是由碳、氫、氧、鈉四種元素組成 D.從分類上看:硬脂酸鈉屬于氧化物 組卷:3引用:1難度:0.6 -
9.下列關于完全燃燒和不完全燃燒的說法不正確的是( )
A.木炭發生不完全燃燒時,也會釋放的熱量 B.燃燒時產生的CO2含有少量的CO,可以用點燃的方法除去CO C.含碳燃料不完全燃燒時會生成一氧化碳等有毒氣體而污染空氣 D.日常生活中燃料完全燃燒對節約資源、保護環境都有著積極的意義 組卷:20引用:1難度:0.7
Ⅱ卷非選擇題(共60分)
-
27.(一)某科研小組了解到氫氣能和氧化鐵發生反應,生成一種金屬單質和一種氧化物,設計了如圖所示的裝置,測定水的組成(雜質不參加反應,已知濃硫酸具有吸水性,裝置A、C能完全吸收相應的物質)反應后測得裝置B中硬質玻璃管(含藥品)的質量減小ag,裝置c中洗氣瓶(含藥品)的質量增加bg,請回答有關問題。
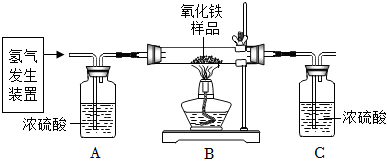
(1)請用含a、b的式子表示出水中氫、氧元素的質量比。
(2)若硬質玻璃管中氧化鐵未完全反應,則求得水中氫、氧元素的質量比會(填“偏大”“偏小”或“不變”)。
(二)一種工業煉鐵方法如圖所示。
①催化反應室中,CH4與CO2或H2O在高溫條件下均能發生反應,產物相同。寫出相應的化學方程式:,。
②該工藝流程中,冶煉出來的鐵水屬于(“純凈物”或“混合物”)。
③某鋼鐵公司用800萬噸含量氧化鐵60%的赤鐵礦,最多能得到含雜質4%的生鐵多少萬噸?(寫出計算過程)組卷:23引用:3難度:0.4 -
28.鐵及其化合物的廣泛應用
(一)鐵的廣泛應用
(1)金屬與人體健康息息相關,人體中的鐵元素屬于(“常量”或“微量”)元素,作用。而人體中含量最多的金屬是(元素名稱)。
(2)鐵制炊具加熱食物,說明鐵具有的性質是。
(3)某嬰兒米粉中含有少量鐵粉,食用后與胃酸(主要成分為鹽酸)發生的化學方程式,幫助補充鐵元素。
(二)草酸亞鐵晶體組成的測定
草酸亞鐵晶體(化學式為FeC2O4?xH2O)是一種淡黃色晶體粉末。
【當x=1時,Mr(FeC2O4?xH2O)=162;當x=2時,Mr(FeC2O4?xH2O)=180;當x=3時,Mr(FeC2O4?xH2O)=198;當x=4時,Mr(FeC2O4?xH2O)=216;當x=5時,Mr(FeC2O4?xH2O)=234;當x=6時,Mr(FeC2O4?xH2O)=252】
【查閱資料】1.白色的無水CuSO4遇水變藍;2.C O 能與氯化鈀(PdCl2)溶液反應生成黑色的鈀粉;3.FeO 和Fe3O4都是黑色物質,FeO在空氣中不穩定,易被氧化。
草酸亞鐵晶體受熱分解生成四種氧化物,為確定分解產物及x的值,設計了如下實驗進行探究:(裝置C、D、E中藥品均足量)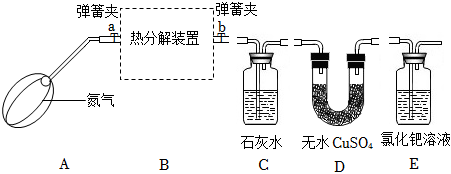
【實驗步驟】
(1)按照氣流從左至右的方向,如圖裝置連接順序為A→B→E,連接好裝置后,;
(2)在裝置B中裝入稱量好的草酸亞鐵晶體,打開彈簧夾a、b,鼓入一段時間氮氣,稱裝置D的質量;
(3)用酒精燈加熱B裝置,直至晶體完全變成黑色,停止加熱;
(4)繼續通氮氣至裝置冷卻,關閉彈簧夾a、b;
(5)再次稱量裝置B中固體質量、裝置D的質量。
【進行實驗】:該小組同學按上述實驗步驟進行實驗,并記錄了如下數據:裝置B中固體質量(/g) 裝置D的質量(/g) 實驗前 9.0 168.2 實驗后 3.6 170.0 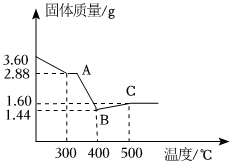
【實驗分析及數據處理】:
(1)加熱前先鼓入一段時間氮氣的目的是。
(2)實驗過程中,裝置D中固體變為藍色,說明草酸亞鐵晶體分解生成了,FeC2O4?xH2O中x的值為;實驗結束后若不繼續通氮氣,x值(填“偏大”、“不變”或“偏小”)。
(3)裝置C中石灰水變渾濁,說明草酸亞鐵晶體分解生成了。
(4)裝置E出現黑色物質,說明草酸亞鐵晶體分解生成了;同時裝置E還具有的作用是。
(5)根據上表數據,計算反應后裝置B中殘留黑色物質的化學式。
【定量研究】取3.60g草酸亞鐵晶體在坩堝中敞口充分加熱,固體質量隨溫度變化的曲線如圖所示,寫出BC段發生反應的化學方程式:。組卷:13引用:1難度:0.3


