2022年湖南省懷化市會同一中高考化學二調試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題2分,共20分。每小題只有一個選項符合題目要求。
-
1.科學防護對預防病毒感染非常重要,下列說法錯誤的是( )
A.制作防護服和口罩的無紡布是有機高分子材料 B.冠狀病毒粒子直徑約60~220nm,介于溶液和膠體粒子之間 C.免洗手消毒液的成分活性銀離子、乙醇均能使蛋白質變性 D.二氧化氯泡騰片可用于水處理 組卷:7引用:3難度:0.5 -
2.短周期主族元素P、Q、X、Y、Z的原子序數依次增加,其中元素P的一種核素僅有一個質子和一個中子;元素X、Z同主族且Z的最高價與最低價的絕對值之比為3;元素Q是組成有機物的基本元素,而元素Y是無機非金屬材料的主角。則下列說法正確的是( )
A.元素P、Q、X所形成的某種化合物可以檢驗Fe3+ B.元素P分別與元素Q、Z所形成的化合物化學鍵一定相同 C.元素Q、Y、Z所形成的最高價氧化物對應的水化物的酸性強弱:Z>Y>Q D.元素Q、Y、Z所形成的單質在一定條件下,均可溶于Z的最高價含氧酸的濃溶液中 組卷:10引用:2難度:0.6 -
3.己二酸(HOOCCH2CH2CH2CH2COOH)是工業上具有重要意義的二元羧酸,它的工業路線和改進的“綠色”合成路線如圖所示。下列說法錯誤的是( )
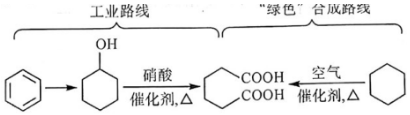
A.1mol己二酸與足量NaHCO3溶液反應生成88gCO2 B.苯、環己烷分子中所有原子均共平面 C.由環己醇生成己二酸的反應類型為氧化反應 D.己二酸與草酸(HOOC-COOH)互為同系物 組卷:6引用:2難度:0.6 -
4.氣相離子催化劑(Fe+、Co+、Mn+等)具有優良的催化效果.其中在氣相Fe+催化下,乙烷發生氧化反應的機理如圖所示(圖中虛線為副反應)。下列說法錯誤的是( )
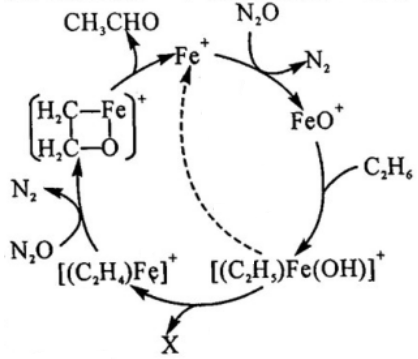
A.主反應為CH3CH3+2N2O→CH3CHO+2N2+H2O B.副反應為CH3CH3+N2O→C2H5OH+N2 C.每生成1molCH3CHO,消耗N2O的物質的量為2mol D.FeO+、[(C2H5)Fe(OH)]+、[(C2H4)Fe]+、 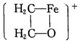 均為反應中間體組卷:18引用:2難度:0.6
均為反應中間體組卷:18引用:2難度:0.6 -
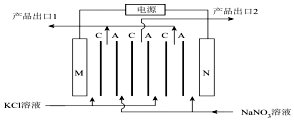 5.某化學興趣小組,根據電化學原理,設計出利用KCl、NaNO3為原料制取KNO3和NaCl的裝置如圖。A、C代表不同類別的選擇性離子通過膜,M、N為惰性電極。下列有關說法中正確的是( )
5.某化學興趣小組,根據電化學原理,設計出利用KCl、NaNO3為原料制取KNO3和NaCl的裝置如圖。A、C代表不同類別的選擇性離子通過膜,M、N為惰性電極。下列有關說法中正確的是( )A.若產品出口1為NaCl溶液,則C為陽離子交換膜 B.電解總反應:電解KCl+NaNO3 KNO2+NaCl電解C.產品出口1溶液離子總濃度與產品出口2相等 D.M上反應確定為:2Cl--2e-═Cl2↑ 組卷:16引用:1難度:0.5 -
6.工業上以黃鐵礦(主要成分為FeS2,含有少量NiS、CuS、SiO2等雜質)為原料制備K4[Fe(CN)6]?3H2O,工藝流程如圖:
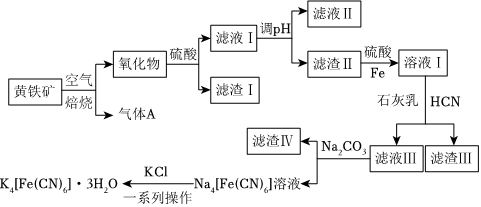
下列說法錯誤的是( )A.“焙燒”時氧化產物有Fe2O3和SO2 B.“調pH”分離Fe3+與Cu2+、Ni2+是利用了它們氫氧化物Ksp的不同 C.“溶液Ⅰ”中主要反應的離子方程式為6OH-+6HCN+Fe2+═[Fe(CN)6]4-+6H2O D.“一系列操作”為過濾、洗滌、干燥 組卷:224引用:8難度:0.3
三、非選擇題:本題共5小題,共60分
-
19.隨著全球氣候問題的日益嚴重,逐步減少使用和倚靠化石燃料已成為必然趨勢,CO2的綜合利用是解決溫室問題的有效途徑
(1)利用CO2合成二甲醚可實現碳循環,其過程主要發生如下反應:
反應Ⅰ:CO2(g)+H2(g)?CO(g)+H2O(g) ΔH1=+41.2kJ?mol-1
反應Ⅱ:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g) ΔH2=-122.5kJ?mol-1
其中反應Ⅱ分以下兩步完成,
反應Ⅲ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g) ΔH3=-49.5kJ?mol-1
反應Ⅳ:2CH3OH?CH3OCH3(g)+H2O(g) ΔH4
①ΔH4=。
②某溫度和壓強下1molCO2與足量的H2在一定的條件下發生上述反應,已知達到平衡時CO2的轉化率為40%,部分物質的物質的量如表:
若反應達到平衡時容器中CO的分壓p(CO)═0.01MPa(氣體分壓=氣體總壓×氣體的物質的量分數),則此時該容器中CO2的分壓p(CO2)═CH3OH CO H2O 0.06 mol 0.02 mol 0.56 mol ,反應Ⅳ的平衡常數Kp═(計算結果保留兩位小數)。
③經研究發現,不同反應條件下反應相同時間(未平衡)測得體系中CH3OH的濃度很低,則可知活化能大小關系為反應Ⅲ(填“大于”“等于”或“小于”)反應Ⅳ。
(2)將CO2轉化為乙醇也可以實現碳循環,發生反應的化學方程式為
2CO2(g)+6H2(g)?C2H5OH(g)+3H2O(g) ΔH<0。實驗測得:v正═k正c2(CO2)?c6(H2),k逆c(C2H5OH)?c3(H2O),k正、k逆為速率常數,只受溫度影響。該反應的lg,lg1k正常數隨溫度的變化的曲線如圖1所示,則1k逆(填m或n)表示lg隨溫度變化的曲線,判斷的理由為1k正。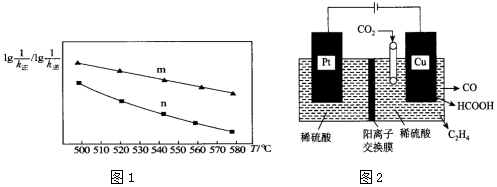
(3)用電解法將CO2轉化為燃料是實現碳循環的另一種途徑,原理如圖2所示。銅電極上產生C2H4的電極反應式為,若陰極只產生CO、HCOOH、C2H4,且生成速率相同,則相同條件下Pt電極與Cu電極上產生的O2與HCOOH的物質的量之比為。組卷:9引用:1難度:0.6 -
20.乙酰氧基胡椒酚乙酸酯(F)具有抗氧化性、抗腫瘤作用,其合成路線如圖所示。
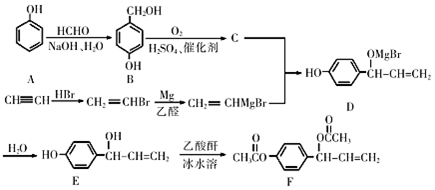
已知:RMgBrR′CHO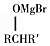
(1)A→B的反應類型為。
(2)化合物C的名稱是。
(3)化合物E中所含官能團的名稱。
(4)寫出化合物F與足量NaOH溶液反應的化學方程式。
(5)寫出同時滿足下列條件的E的一種同分異構體的結構簡式:。
①能與FeCl3溶液發生顯色反應;
②能發生銀鏡反應;
③核磁共振氫譜顯示有4種不同化學環境的氫,其峰面積比為6:2:1:1。
(6)請以乙醛和甲苯為原料制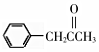 ,寫出相應的合成路線流程圖。(無機試劑任用,合成路線流程圖如題示例)組卷:18引用:4難度:0.5
,寫出相應的合成路線流程圖。(無機試劑任用,合成路線流程圖如題示例)組卷:18引用:4難度:0.5


