2022年湖南省婁底五中高考化學第三次模擬試卷
發布:2024/4/20 14:35:0
一、單項選擇題:本題共10小題,每小題3分,共30分。在每小題給出的四個選項中,只有一項符合題目要求。
-
1.根據樂器的制作材料可對中國古典樂器進行分類。下列對樂器類別及制作材料的相關描述不正確的是( )
選項 樂器類別及制作材料 描述 A 琴(“絲”類):蠶絲可用于制琴弦 蠶絲僅由碳、氫、氧元素組成 B 編鐘(“金”類):青銅可用于鑄造編鐘 青銅是我國使用最早的合金 C 陶塤(“土”類):陶土可用于燒制陶瓷塤 陶瓷屬于無機非金屬材料 D 竹笛(“竹”類):竹子可用于制笛 竹子富含纖維素 A.A B.B C.C D.D 組卷:41引用:2難度:0.7 -
2.環己基乙酸(IV)是一種香料成分,可通過如圖方法合成。下列有關說法正確的是( )
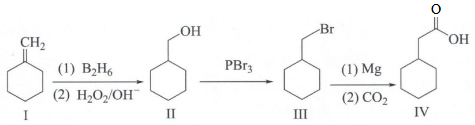
A.I中所有原子均可共平面 B.I與III均屬于烴類物質 C.II中六元環上的一氯代物共有3種 D.II與IV可發生酯化反應 組卷:48引用:2難度:0.6 -
3.2021年我國科學家實現了二氧化碳到淀粉的人工合成。有關物質的轉化過程示意如圖:

下列說法不正確的是( )A.反應①中分解H2O制備H2需從外界吸收能量 B.反應②中CO2→CH3OH,碳原子的雜化方式發生了變化 C.核磁共振、X射線衍射等技術可檢測合成淀粉與天然淀粉的組成結構是否一致 D.C6→淀粉的過程中只涉及O-H鍵的斷裂和形成 組卷:115引用:12難度:0.6 -
4.下列做法或實驗(圖中部分夾持略),不能達到目的的是( )
防止鐵管道被腐蝕 檢驗產生的SO2 制備并收集NH3 精煉粗銅 



A B C D A.A B.B C.C D.D 組卷:71引用:2難度:0.5 -
5.Fe2(SO4)3溶于一定量水中,溶液呈淺棕黃色(a)。加入少量濃HCl黃色加深(b)。
已知:Fe3++4Cl-?[FeCl4]-(黃色);濃度較小時[Fe(H2O)6]3+(用Fe3+表示)幾乎無色
取溶液進行如下實驗,對現象的分析不正確的是( )A.測溶液a的pH≈1.3,證明Fe3+發生了水解 B.加入濃HCl,H+與Cl-對溶液顏色變化、Fe3+濃度大小的影響是一致的 C.向b中加入AgNO3后,黃色褪去,說明H+能抑制Fe3+水解 D.將溶液a滴入沸水中,加熱,檢測有丁達爾效應,說明加熱能促進Fe3+水解 組卷:190引用:6難度:0.7 -
6.實驗室制取下列氣體,所選反應試劑、制備裝置與收集方法合理的是( )
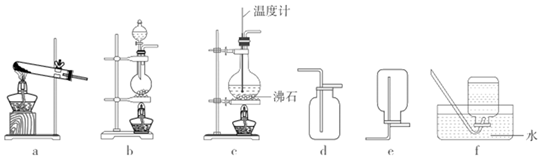
選項 氣體 反應試劑 制備裝置 收集方法 A NO2 Cu、稀硝酸 b e B C2H4 C2H5OH、濃硫酸 c f C NH3 Ca(OH)2、NH4Cl a d D SO2 Na2SO3、70%硫酸 b f A.A B.B C.C D.D 組卷:51引用:3難度:0.5
三、非選擇題:本題共4小題,共50分
-
 18.鐵和鈷是兩種重要的過渡元素。回答下列問題:
18.鐵和鈷是兩種重要的過渡元素。回答下列問題:
(1)基態Fe3+的價電子排布式為
(2)FeCl3的熔點為306℃,沸點為315℃。FeCl3的晶體類型是,實驗室可以用KSCN溶液、苯酚( )檢驗Fe3+。N、O、S的第一電離能由大到小的順序為 (用元素符號表示),SCN-立體構型為。
)檢驗Fe3+。N、O、S的第一電離能由大到小的順序為 (用元素符號表示),SCN-立體構型為。
(3)已知冷的濃硫酸和濃硝酸都能使鐵表面形成致密的氧化膜,工業上一般用冷的濃硫酸進行鋼鐵防腐,而不用冷的濃硝酸進行防腐,其可能的原因是。不同濃度的HNO3與鐵反應的還原產物很復雜,寫出稀硝酸與過量的鐵反應時生成的離子方程式NH+4。
(4)氧化亞鐵晶體的晶胞如圖所示。已知:氧化亞鐵晶體的密度為ρg?cm-3,NA代表阿伏加德羅常數的值。在該晶胞中,與Fe2+緊鄰且等距離的O2-數目為;Fe2+與Fe2+的最短間距為cm。
(5)Co(NH3)5Cl3是鈷的一種配合物,向含0.01mol該配合物的溶液中加入足量AgNO3溶液,生成白色沉淀2.87g,則1mol該配合物的σ鍵數目為。組卷:236引用:4難度:0.5 -
19.某喹啉類化合物P的合成路線如圖:
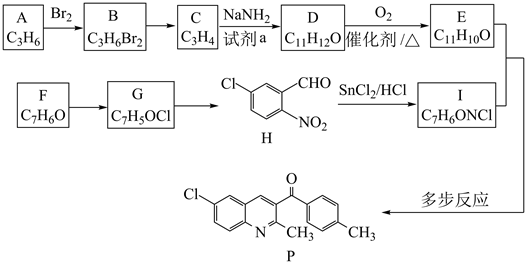
已知:R1-C≡CH+R2CHONaNH3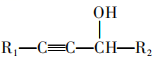
(1)A為鏈狀,按官能團分類,其類別是。
(2)B→C的反應方程式是。
(3)C→D所需的試劑a是。
(4)下列關于E的說法正確的是。
A.能發生銀鏡反應
B.能發生氧化、消去、加聚反應
C.核磁共振氫譜顯示峰面積比為3:2:2:3
D.1molE可以與6molH2發生反應
(5)G的結構簡式為。
(6)H→I的反應類型為。
(7)由I和E合成P的流程如下,M與N互為同分異構體,寫出J、M、N的結構簡式:、、。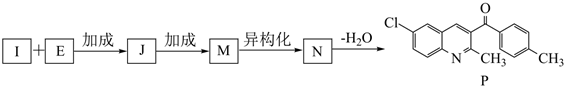 組卷:100引用:7難度:0.5
組卷:100引用:7難度:0.5


