2022-2023學年福建省廈門市思明區(qū)湖濱中學九年級(下)期中化學試卷
發(fā)布:2024/7/9 8:0:8
一、選擇題(每小題只有一個正確選項,1-5題每題2分,6-10題每題3分,共25分)
-
1.端午節(jié)吃粽子是傳統(tǒng)習俗,在制作粽子的過程中一定發(fā)生了化學變化的是( )
A.水洗糯米 B.刀切肉塊 C.粽葉包粽 D.燒火煮粽 組卷:375引用:41難度:0.8 -
2.下列實驗操作不正確的是( )
A. 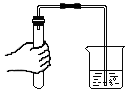
檢查氣密性B. 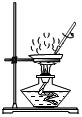
蒸發(fā)C. 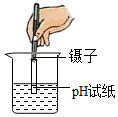
測定溶液pHD. 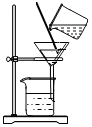
過濾組卷:72引用:8難度:0.9 -
3.下列物質分類正確的是( )
A.食鹽水、空氣、石油—混合物 B.金剛石、石墨、石灰石—化合物 C.生鐵、焊錫、水銀—合金 D.燒堿、純堿、熟石灰—堿 組卷:8引用:2難度:0.8 -
 4.如圖為中考化學試卷答題卡中用于識別考生信息的條形碼。條形碼有黏性,其黏性主要來源于膠黏劑-丙烯酸。丙烯酸的化學式為C3H4O2,下列關于丙烯酸的說法合理的是( )
4.如圖為中考化學試卷答題卡中用于識別考生信息的條形碼。條形碼有黏性,其黏性主要來源于膠黏劑-丙烯酸。丙烯酸的化學式為C3H4O2,下列關于丙烯酸的說法合理的是( )A.丙烯酸中含有氧分子 B.丙烯酸的相對分子質量為72g C.丙烯酸中碳元素與氧元素的質量比為9:8 D.丙烯酸由3個碳原子、4個氫原子和2個氧原子構成 組卷:149引用:5難度:0.5 -
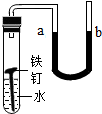 5.如圖所示,在盛水的試管中放入一根潔凈的鐵釘,用帶U形管的膠塞塞緊,U型管內(nèi)水面處于同一高度,一周后觀察U型管內(nèi)水面變化是( )
5.如圖所示,在盛水的試管中放入一根潔凈的鐵釘,用帶U形管的膠塞塞緊,U型管內(nèi)水面處于同一高度,一周后觀察U型管內(nèi)水面變化是( )A.a(chǎn)比b高 B.b比a高 C.一樣高 D.無法判斷 組卷:86引用:17難度:0.9
二、非選擇題
-
16.現(xiàn)有平板電視顯示屏工廠生產(chǎn)過程中丟棄廢玻璃粉末(含SiO2、Fe2O3、CeO2等物質),某課題組以此粉末為原料回收鈰和硫酸亞鐵晶體,設計實驗流程如下:
資料1:CeO2是一種金屬氧化物,化學性質穩(wěn)定,與稀硫酸不反應。在H2O2存在的條件下,兩種物質能反應。
資料2:FeSO4容易被空氣中的O2氧化。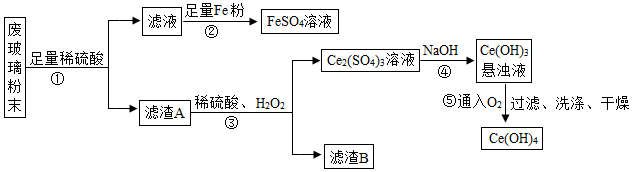
(1)寫出①反應的化學方程式,該反應類型為,為提高①中的反應效率,可采用的具體措施有。(寫一種即可)
(2)將②中所得FeSO4溶液在氮氣環(huán)境中蒸發(fā)濃縮、、過濾,得到FeSO4晶體,其中氮氣的作用是。
(3)請補充完整③反應的化學方程式:2CeO2+3H2SO4+H2O2═Ce2(SO4)3++O2↑,濾渣B的主要成分是。
(4)生產(chǎn)過程中可循環(huán)利用的物質是。
(5)Ce(OH)4中的Ce元素化合價為價。組卷:73引用:3難度:0.4 -
17.碳酸氫鈉是應用廣泛的鹽,化學小組對其進行了探究。
(一)碳酸氫鈉的制備
【查閱資料】Ⅰ.侯氏制堿的原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+H2O+CO2↑。△
Ⅱ.研究發(fā)現(xiàn):NaHCO3溶于水時吸收熱量,Na2CO3溶于水時放出熱量。
【實驗制備】根據(jù)侯氏制堿原理設計,用圖甲裝置制取NaHCO3。反應結束后,將試管中的混合物過濾、洗滌、低溫烘干得到白色固體。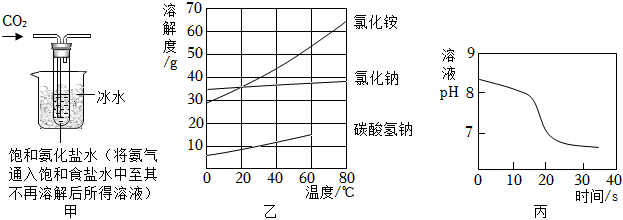
(1)燒杯中冰水的作用是。
(2)能進一步確認該白色固體是NaHCO3的可行方案是(填字母序號)。
A.取少量白色固體于試管中,滴加稀鹽酸,若有氣泡,則固體是NaHCO3
B.取少量白色固體于試管中,加水溶解,并用溫度計測量溫度變化,若溫度計示數(shù)下降,則固體是NaHCO3
(3)圖乙中碳酸氫鈉的溶解度在60℃后無數(shù)據(jù)的原因可能是。
【性質探究】
常溫下,取一定量的NaHCO3溶液于燒杯中,插入pH傳感器,向燒杯中持續(xù)滴加CaCl2溶液,有白色沉淀生成,當溶液的pH變?yōu)?.68時開始有無色氣體產(chǎn)生。反應過程中溶液的pH隨時間變化如圖丙。
【交流反思】
(4)NaHCO3溶液顯(填“酸”“堿”或“中”)性。
(二)測定碳酸氫鈉的含量
已知制得的碳酸氫鈉樣品中含有少量氯化鈉,某探究小組欲測定該碳酸氫鈉的純度。
【實驗步驟】
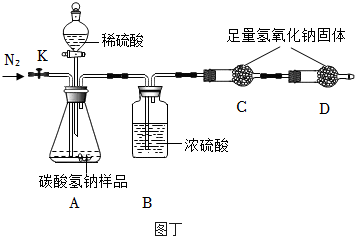
(5)①組裝如圖裝置,并;
②稱取一定量的樣品放入錐形瓶中,加少量水溶解,并在其他裝置中加入相應的藥品;
③打開止水夾K,緩緩通入一段時間N2后關閉K,稱取裝置C的質量;
④打開分液漏斗的旋塞滴入稀硫酸,直到不在產(chǎn)生氣泡為止;
⑤再次打開止水夾K,緩緩通入一段時間N2,再次稱量裝置C的質量。
【實驗分析】
(6)B裝置的作用是。
(7)步驟⑤中緩緩通入一段時間N2的目的是。
(8)如果缺少裝置D,所測樣品中碳酸氫鈉的質量分數(shù)(填“偏大”“偏小”或“不變”)。
(9)取10g碳酸氫鈉固體樣品于錐形瓶中,加入足量的稀硫酸,若C處固體增重4.4g,計算樣品中碳酸氫鈉的質量分數(shù)。
提示:本實驗的化學方程式為:2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O。組卷:29引用:2難度:0.4


