2021-2022學年北京市八一學校高一(上)期中化學試卷
發布:2024/12/11 1:0:1
一、單選題
-
1.關于容量瓶的四種敘述:①是配制準確濃度溶液的儀器;②不宜貯存溶液;③不能用來加熱;④使用之前要檢查是否漏水.這些敘述中正確的是( )
A.①②③④ B.②③ C.①②④ D.②③④ 組卷:168引用:87難度:0.9 -
2.下列物質中,屬于電解質的是( )
A.Fe B.NaCl C.稀鹽酸 D.Na2SO4溶液 組卷:71引用:2難度:0.6 -
3.下列關于物質分類的敘述中,不正確的是( )
A.H2SO3屬于酸 B.Ba(OH)2屬于堿 C.霧屬于氣溶膠 D.氨水屬于純凈物 組卷:15引用:1難度:0.6 -
4.下列關于氨氣性質的描述中,不正確的是( )
A.黃綠色氣體 B.有刺激性氣味 C.相同條件下密度比空氣的小 D.極易溶于水 組卷:38引用:2難度:0.8 -
5.下列物質中,既含有氯分子,又含有氯離子的是( )
A.氯氣 B.氯水 C.氯化鈉 D.氯化氫 組卷:34引用:4難度:0.8 -
6.實驗室中,下列行為不符合安全要求的是( )
A.熄滅酒精燈時,用燈帽蓋滅 B.將實驗剩余的鈉直接丟棄在廢液缸中 C.熄滅少量燃著的金屬鈉,用干燥沙土覆蓋 D.稀釋濃硫酸時,將濃硫酸沿器壁緩慢倒入水中并用玻璃棒不斷攪拌 組卷:3引用:3難度:0.8 -
7.下列說法中,正確的是( )
A.56gFe的物質的量為2mol B.常溫常壓下,1molO2的體積是22.4L C.0.5mol?L-1MgCl2溶液中含有0.5molMg2+ D.1molCO2中含有的分子數約為6.02×1023 組卷:32引用:1難度:0.8 -
8.Fe(OH)3膠體和FeCl3溶液共同具備的性質是( )
A.兩者均有丁達爾效應 B.兩者均能透過半透膜 C.加入鹽酸先沉淀,隨后溶解 D.分散質粒子可通過濾紙 組卷:19引用:4難度:0.8 -
9.下列物質中,不能使有色布條褪色的是( )
A.次氯酸鈉溶液 B.次氯酸鈣溶液 C.新制氯水 D.氯化鈣溶液 組卷:37引用:7難度:0.7 -
10.如圖所示是成都市某日的空氣質量報告內容,以下敘述正確的是( )

A.該日空氣質量等級屬于優 B.該日空氣首要污染物是PM2.5 C.PM2.5、PM10指的是懸浮顆粒物,不會影響人體健康 D.污染物NO2、CO可能來源于機動車尾氣 組卷:22引用:2難度:0.6
三、解答題
-
29.氯氣可用于制取漂白劑和自來水消毒。
(1)將氯氣通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物質是(填寫化學式)。
(2)“84”消毒液也可用于漂白,其工業制法是控制在常溫條件下,將氯氣通入NaOH溶液中,反應的離子方程式為。
(3)同學們探究“84”消毒液在不同pH下使紅紙褪色的情況,做了如下實驗:
步驟1:將5mL市售“84”消毒液稀釋100倍,測得稀釋后溶液的pH=12;
步驟2:將稀釋后溶液各20mL分別加入3個潔凈的小燒杯中;
步驟3:用H2SO4溶液將3個燒杯內溶液的pH分別調至10、7 和4.(溶液體積變化忽略不計)
步驟4:在3個燒杯中分別放入大小相同的紅紙,觀察現象,記錄如下:
已知,溶液中Cl2、HClO和ClO-物質的量分數(α)隨溶液pH變化的關系如圖所示:燒杯 溶液的pH 現象 a 10 10min后,紅紙基本不褪色;4h后紅紙褪色 b 7 10min后,紅紙顏色變淺;4h后紅紙褪色 c 4 10min后,紅紙顏色變得更淺;4h后紅紙褪色 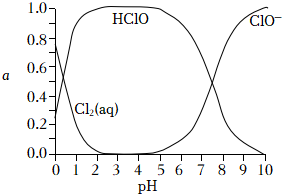
①由實驗現象可獲得以下結論:溶液的pH在4~10范圍內,pH越大,紅紙褪色。
②結合圖象進行分析,b、c兩燒杯中實驗現象出現差異的原因是。
(4)由于氯氣會與自來水中的有機物發生反應生成對人體有害的物質,人們嘗試研究并使用新的自來水消毒劑,如ClO2氣體就是一種新型高效含氯消毒劑。
①一種制備 ClO2的方法是用SO2通入硫酸酸化的NaClO3溶液中,反應的離子方程式為。
②另一種制備 ClO2的方法是用NaClO3與鹽酸反應,同時有Cl2生成,產物中Cl2體積 約占,每生成0.5mol ClO2,轉移13mol e-。組卷:350引用:4難度:0.1 -
30.某實驗小組探究Na2CO3和NaHCO3的性質,發現實驗室里盛放兩種固體的試劑瓶丟失了標簽.于是,他們先對固體A、B進行鑒別,再通過實驗進行性質探究.
(1)分別加熱固體A、B,發現固體A受熱產生的氣體能使澄清石灰水變渾濁.A受熱分解的化學方程式為.
(2)稱取兩種固體各2g,分別加入兩個小燒杯中,再各加10mL蒸餾水,振蕩,測量溫度變化;待固體充分溶解,恢復到室溫,向所得溶液中各滴入2滴酚酞溶液.
①發現Na2CO3固體完全溶解,而NaHCO3固體有剩余,由此得出結論:.
②同學們在兩燒杯中還觀察到以下現象.其中,盛放Na2CO3的燒杯中出現的現象是(填字母序號).
a.溶液溫度下降
b.溶液溫度升高
c.滴入酚酞后呈淺紅色
d.滴入酚酞后呈紅色
(3)如圖所示,在氣密性良好的裝置Ⅰ和Ⅱ中分別放入藥品,將氣球內的固體同時倒入試管中.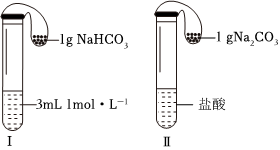
①兩試管中均產生氣體,(填“Ⅰ”或“Ⅱ”)的反應程度更為劇烈.
②反應結束后,氣球均有膨脹,恢復至室溫,下列說法正確的是(填字母序號).
a.裝置Ⅰ的氣球體積較大
b.裝置Ⅱ的氣球體積較大
c.生成氣體的體積根據鹽酸計算
d.生成氣體的體積根據固體計算
(4)同學們將兩種固體分別配制成0.5mol?L-1的溶液,設計如下方案并對反應現象做出預測:
實施實驗后,發現操作2的現象與預測有差異:產生白色沉淀和氣體,則該條件下,NaHCO3溶液與CaCl2溶液反應的離子方程式為實驗方案 預測現象 預測依據 操作1:向2mLNa2CO3溶液中滴加1mL0.5mol?L-1CaCl2溶液 有白色沉淀 Na2CO3溶液中的 濃度較大,能與CaCl2發生反應:CO2-3(寫離子方程式)操作2:向2mLNaHCO3溶液中滴加1mL0.5mol?L-1CaCl2溶液 無白色沉淀 NaHCO3溶液中的 濃度很小,不能與CaCl2反應CO2-3.組卷:56引用:12難度:0.5


