人教版(2019)必修第一冊《4.2 元素周期律》2023年同步練習卷(2)
發布:2024/7/18 8:0:9
一、選擇題
-
1.下列說法 正確的是( )
A.隨著元素原子序數的遞增,原子最外層電子數總是從1到8重復出現 B.同主族元素,隨著原子序數的遞增,元素原子的最外層電子排布呈現周期性變化 C.同周期元素,隨著原子序數的遞增,元素原子的最外層電子排布呈現周期性變化 D.每個周期中,元素原子最外層電子數小于4的為金屬元素,大于4的為非金屬元素 組卷:9引用:2難度:0.8 -
2.除第一周期外,下列關于同周期主族元素性質的變化規律的敘述不正確的是( )
A.從左到右,原子半徑逐漸減小 B.從左到右,單質的氧化性逐漸減弱,還原性逐漸增強 C.從左到右,最高價氧化物對應水化物的堿性逐漸減弱,酸性逐漸增強 D.從左到右,元素最高正化合價從+1遞變到+7(氧、氟除外),最低負化合價從-4遞變到-1 組卷:23引用:3難度:0.6 -
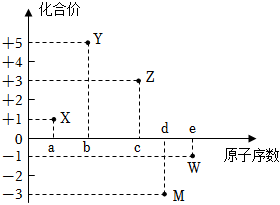 3.五種短周期元素 X、Y、Z、M、W 的原子序數與其某常見化合價的關系如圖所示,下列關 系不正確的是( )
3.五種短周期元素 X、Y、Z、M、W 的原子序數與其某常見化合價的關系如圖所示,下列關 系不正確的是( )A.元素 X可能為鋰 B.原子半徑大小:r(M)>r(W) C.Z元素是形成化合物種類最多的元素 D.氣態氫化物的還原性:YH3<MH3 組卷:26引用:4難度:0.5 -
4.有A、B、C、D、E五種金屬元素。在相同條件下,B元素的最高價氧化物對應水化物的堿性比A的弱;A、B單質均可以從C鹽溶液中置換出C;D單質可以與冷水劇烈反應并放出氫氣;A、B、C、E四種單質分別投入鹽酸中,只有E不放出氫氣。則五種金屬元素的金屬性由強到弱的順序為( )
A.D>B>A>C>E B.D>A>B>C>E C.A>B>C>E>D D.D>E>B>A>C 組卷:151引用:3難度:0.5 -
5.已知X、Y、Z元素的原子具有相同的電子層數,且原子序數依次增大,其最高價氧化物對應的水化物酸性依次增強,則下列判斷正確的是( )
A.原子半徑按X、Y、Z依次增大 B.陰離子的還原性按X、Y、Z順序增強 C.單質的氧化性按X、Y、Z順序增強 D.氫化物的穩定性按Z、Y、X順序增強 組卷:12引用:2難度:0.6 -
6.已知33As、35Br位于同一周期,下列關系正確的是( )
A.還原性:As3->S2->Cl- B.熱穩定性:HCl>AsH3>HBr C.原子半徑:As>Cl>P D.酸性:H3AsO4>H2SO4>H3PO4 組卷:868引用:98難度:0.7
二、填空題
-
19.(1)原子序數大于4的主族元素A和B的離子Am+和Bn-它們的核外電子排布相同,據此推斷:
①A和B所屬周期數之差為,
②A和B的核電荷數之差為(用含m、n的代數式表示)
③B和A的族序數之差為(用含m、n的代數式表示)
(2)A、B兩元素,A的原子序數為x,A和B所在周期包含元素種類數目分別為m和n.①如果A和B同在ⅠA族,
當B在A的上一周期時,B的原子序數為(用含m、n、x的代數式表示,下同);當B在A的下一周期時,B的原子序數為;
②如果A和B同在ⅦA族,
當B在A的上一周期時,B的原子序數為;
當B在A的下一周期時,B的原子序數為.組卷:94引用:5難度:0.5
三、推斷題
-
20.2019年是“國際化學元素周期表年”,回答下列問題:

(1)按照硫元素在周期表里的位置,在圖中用實線畫出周期表的邊界,并用陰影 表示第Ⅷ族的位置。
表示第Ⅷ族的位置。
(2)在圖中用元素符號注明第35號元素位置。
(3)根據元素周期律判斷下列物質性質強弱(填“>”、“<”或“=”)。
A.氧化性強弱:F2Cl2
B.金屬性強弱:KNa
C.酸性強弱:H3PO4H2SO4
D.堿性強弱:NaOHMg(OH)2
(4)下列有關元素周期表的說法正確的是。(填字母序號)
A.周期表中的非金屬元素都位于主族和0族
B.周期表中由短、長周期元素組成的縱列就是主族
C.ⅠA族和0族是包含元素種類最多的縱列
D.可以在過渡元素區域尋找優良的催化劑和耐高溫耐腐蝕的合金材料組卷:8引用:3難度:0.7


