2015-2016學年河南省洛陽市宜陽一高高二(上)第二周周練化學試卷(12月份)
發布:2024/4/20 14:35:0
一.選擇題(共16小題)
-
1.下列圖示與對應的敘述相符的是( )
A. 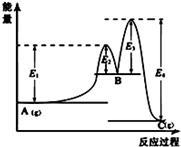
圖中可以看出反應A(g)=C(g)的ΔH=(E1-E4)kJ?mol-1B. 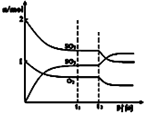
圖中表示一定條件下進行的反應2SO2+O2═2SO3各成分的物質的量變化,t2時刻改變的條件可能是擴大了容器的體積C. 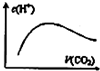
圖中表示將CO2通入NaOH的稀溶液中,隨著CO2的通入,溶液中水電離出的c(H+)變化關系D. 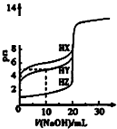
圖中曲線表示用0.1000mol/L NaOH溶液分別滴定濃度相同的三種一元酸,由此可判斷HX的酸性最強組卷:462引用:4難度:0.5 -
2.下列有關能量轉換的說法正確的是( )
A.煤燃燒是化學能轉化為熱能的過程 B.化石燃料和植物燃料燃燒時放出的能量均來源于太陽能 C.動物體內葡萄糖被氧化成CO2是熱能轉變成化學能的過程 D.植物通過光合作用將CO2轉化為葡萄糖是太陽能轉變成熱能的過程 組卷:425引用:34難度:0.5 -
3.甲醇質子交換膜燃料電池中將甲醇蒸氣轉化為氫氣的兩種反應原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)ΔH=+49.0kJ?mol-1
②CH3OH(g)+O2(g)═CO2(g)+2H2(g)ΔH=-192.9kJ?mol-112
下列說法正確的是( )A.CH3OH的燃燒熱為192.9kJ?mol-1 B. 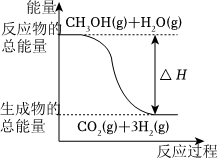
反應①中的能量變化如圖所示C.CH3OH轉變成H2的過程一定要吸收能量 D.根據②推知反應CH3OH(l)+ O2(g)═CO2(g)+2H2(g)的ΔH>-192.9kJ?mol-112組卷:581引用:126難度:0.7 -
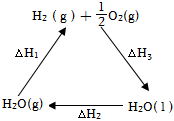 4.某科學家利用二氧化鈰(CeO2)在太陽能作用下將H2O、CO2轉變成H2、CO.其過程如下:
4.某科學家利用二氧化鈰(CeO2)在太陽能作用下將H2O、CO2轉變成H2、CO.其過程如下:
mCeO2(m-x)CeO2?xCe+xO2太陽能①
(m-x)CeO2?xCe+xH2O+xCO2mCeO2+xH2+xCO900℃②
下列說法不正確的是( )A.該過程中CeO2沒有消耗 B.該過程實現了太陽能向化學能的轉化 C.圖中△H1=△H2+△H3 D.以CO和O2構成的堿性燃料電池的負極反應式為CO+4OH--2e-=CO32-+2H2O 組卷:155引用:31難度:0.9 -
5.已知反應:①101kPa時,C(s)+
O2(g)═CO(g)△H1=-110.5kJ/mol12
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列結論正確的是( )A.若碳的燃燒熱用△H3來表示,則△H3<△H1 B.若碳的燃燒熱用△H3來表示,則△H3>△H1 C.濃硫酸與稀NaOH溶液反應的中和熱為57.3kJ/mol D.稀醋酸與稀NaOH溶液反應生成1mol水,放出57.3kJ熱量 組卷:284引用:32難度:0.5 -
 6.T℃時,在1L的密閉容器中充入2mol CO2和6mol H2,一定條件下發生反應:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.0kJ/mol測得H2和CH3OH(g)的濃度隨時間變化如圖所示.下列說法不正確的是( )
6.T℃時,在1L的密閉容器中充入2mol CO2和6mol H2,一定條件下發生反應:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.0kJ/mol測得H2和CH3OH(g)的濃度隨時間變化如圖所示.下列說法不正確的是( )A.0~10min內v(H2)=0.3mol/(L?min) B.T℃時,平衡常數K= ,CO2和H2的轉化率相等127C.T℃時,上述反應中有64gCH3OH生成,同時放出98.0kJ的熱量 D.達到平衡后,升高溫度或再充入CO2氣體,都可以提高H2的轉化率 組卷:92引用:6難度:0.5 -
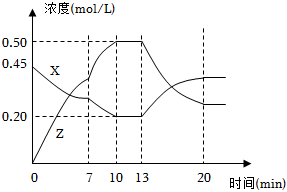 7.向一容積為1L 的密閉容器中加入一定量的X、Y,發生化學反應aX(g)+2Y(s)?bZ(g)△H<0.如圖是容器中X、Z的物質的量濃度隨時間變化的曲線.根據以上信息判斷,下列說法中正確的是( )
7.向一容積為1L 的密閉容器中加入一定量的X、Y,發生化學反應aX(g)+2Y(s)?bZ(g)△H<0.如圖是容器中X、Z的物質的量濃度隨時間變化的曲線.根據以上信息判斷,下列說法中正確的是( )A.用X表示0~10min內該反應的平均速率為v(X)=0.045mol/(L?min) B.化學方程式中a:b=1:3 C.推測在第7min時曲線變化的原因可能是增加X的濃度 D.推測該反應處于化學平衡狀態的時間是10min--13min及第20min后 組卷:92引用:2難度:0.5
二.簡答(共6小題)
-
21.甲、乙兩位同學設計用實驗確定某酸HA是弱電解質,存在電離平衡,且改變條件平衡發生移動.實驗方案如下:
甲:①準確配制0.1mol?L-1的HA、HCl溶液各100mL;
②取純度相同,質量、大小相等的鋅粒于兩支試管中,同時加入0.1mol?L-1的HA、HCl溶液各10mL,
按圖1裝好,觀察現象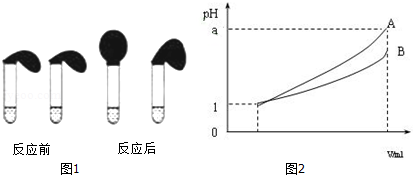
乙:①用pH計測定物質的量濃度均為0.1mol?L-1HA和HCl溶液的pH;
②再取0.1mol?L-1的HA和HCl溶液各2滴(1滴約為1/20mL)分別稀釋至100mL,再用pH計測其pH變化
(1)甲、乙兩方案中都要用到mL的容量瓶.乙方案中說明HA是弱電解質的理由是,測得0.1mol?L-1的HA溶液的pH1(填“>”、“<”或“=”);甲方案中,說明HA是弱電解質的實驗現象是:.
A.加入HCl溶液后,試管上方的氣球鼓起慢
B.加入HA溶液后,試管上方的氣球鼓起慢
C.加入兩種稀酸后,兩個試管上方的氣球同時鼓起,且一樣大
(2)乙同學設計的實驗第步,能證明改變條件弱電解質平衡發生移動.甲同學為了進一步證明弱電解質電離平衡移動的情況,設計如下實驗:①使HA的電離程度和c(H+)都減小,c(A-)增大,可在0.1mol?L-1的HA溶液中,選擇加入試劑;
A.NaA固體(可完全溶于水) B.1mol?L-1NaOH溶液 C.1mol?L-1H2SO4 D.2mol?L-1HA
②使HA的電離程度減小,c(H+)和c(A-)都增大,可在0.1molL-1的HA溶液中,選擇加入試劑.
A.NaA固體(可完全溶于水) B.1mol?L-1NaOH溶液 C.1mol?L-1H2SO4 D.2mol?L-1HA
(3)pH=1的兩種酸溶液A、B各1mL,分別加水稀釋到1000mL,其pH與溶液體積V的關系如圖2所示,則下列說法不正確的有.
A.兩種酸溶液的物質的量濃度一定相等
B.稀釋后,A酸溶液的酸性比B酸溶液弱
C.若a=4,則A是強酸,B是弱酸
D.若1<a<4,則A、B都是弱酸.組卷:55引用:1難度:0.3 -
22.常溫下,某水溶液M中存在的離子有:Na+、A2-、HA-、H+、OH-,存在的分 子有H2O、H2A.根據題意回答下列問題:
(1)寫出酸H2A的電離方程式.
(2)若溶液M由10mL 2mol?L-1NaHA溶液與10mL 2mol?L-1NaOH溶液混合而得,則溶液M的pH7 (填“>”、“<”或“=”),溶液中離子濃度由大到小順序為.(溶液混合時體積變化忽略,下同)
(3)已知Ksp(BaA)=1.8×10-10,向(2)的混合溶液中加入10mL 1mol?L-1BaCl2溶液,混合后溶液中的Ba2+濃度為mol?L-1.
(4)若溶液M由pH=3的H2A溶液V1 mL與pH=11的NaOH溶液V2 mL混合反應而得,混合溶液=104,V1與V2的大小關系為c(H+)c(OH-)(填“大于、等于、小于”或“均有可能”).組卷:91引用:2難度:0.1


