2020-2021學年北京四十三中高二(上)期中化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題(本題包括20小題,每小題2分,共40分)
-
1.下列說法不正確的是( )
A.任何化學反應都會伴隨著能量的變化 B.需要加熱才能發生的反應一定是吸熱反應 C.反應物的總能量大于生成物的總能量,則該反應為放熱反應 D.斷鍵吸收的總能量大于成鍵放出的總能量,則該反應為吸熱反應 組卷:255引用:6難度:0.8 -
2.1mol氫氣燃燒生成液態水,放出285.8kJ熱量。下列熱化學方程式正確的是( )
A.2H2(g)+O2(g)=2H2O(I)△H=-285.8kJ?mol-1 B.2H2(g)+O2(g)=2H2O(g)△H=-285.8kJ?mol-1 C.2H2(g)+O2(g)=2H2O(I)△H=-571.6kJ?mol-1 D.2H2(g)+O2(g)=2H2O(I)△H=+571.6kJ?mol-1 組卷:176引用:5難度:0.9 -
3.已知:H2(g)+F2(g)═2HF(g);△H=-270kJ/mol,下列說法正確的是( )
A.氟化氫氣體分解生成氫氣和氟氣的反應是放熱反應 B.1 mol H2與1 mol F2反應生成2 mol液態HF放出的熱量小于270 kJ C.在相同條件下,1 mol H2與1 mol F2的能量總和大于2 mol HF氣體的能量 D.該反應中的能量變化可用如圖來表示 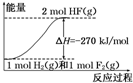 組卷:19引用:9難度:0.9
組卷:19引用:9難度:0.9 -
4.根據以下3個熱化學方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)ΔH=-Q1 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(l)ΔH=-Q2 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(g)ΔH=-Q3kJ/mol
判斷Q1、Q2、Q3三者關系正確的是( )A.Q1>Q2>Q3 B.Q1>Q3>Q2 C.Q3>Q2>Q1 D.Q2>Q1>Q3 組卷:837引用:174難度:0.5 -
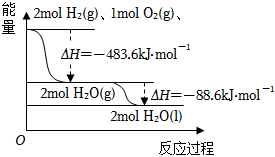 5.依據如圖判斷,下列說法正確的是( )
5.依據如圖判斷,下列說法正確的是( )A.2 mol H2(g)與1 mol O2(g)所具有的總能量比2 mol H2O(g) 所具有的總能量低 B.氫氣的燃燒熱為△H=-241.8 kJ?mol-1 C.H2O(g)生成H2O(l)時,斷鍵吸收的能量小于成鍵放出的能量 D.液態水分解的熱化學方程式為:2H2O(l)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1 組卷:6引用:2難度:0.7 -
6.在2L密閉容器中充入一定量的SO2和O2,化學方程式是2SO2+O2?2SO3.經測定反應開始后3s末O2的物質的量減小了1.5mol,則前3s內SO2的平均反應速率為( )
A.0.25mol?L-1?s-1 B.0.5mol?L-1?s-1 C.0.75mol?L-1?s-1 D.0.83mol?L-1?s-1 組卷:311引用:3難度:0.6 -
7.甲醇質子交換膜燃料電池中將甲醇蒸氣轉化為氫氣的兩種反應原理如方程式①②所示:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ?mol-1
②CH3OH(g)+O2(g)=CO2(g)+2H2(g);△H=-192.9kJ?mol-112
③H2(g)+O2(g)=H2O(g);△H=-241.8kJ?mol-112
下列說法正確的是( )A.CH3OH的燃燒熱為192.9kJ?mol-1 B. 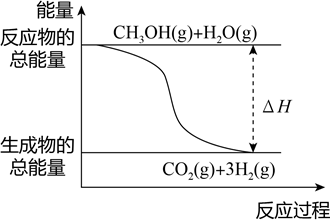
反應①中的能量變化如圖所示C.CH3OH轉變成H2的過程一定要吸收能量 D.根據以上反應可知:CH3OH(g)+ O2(g)=CO2(g)+2H2O(g)的△H=-676.5kJ?mol-132組卷:13引用:3難度:0.7 -
8.下列各組實驗中,化學反應速率最快的是( )
反應物 催化劑 溫度 A 10mL10%H2O2溶液 無 25℃ B 10mL20%H2O2溶液 無 25℃ C 10mL20%H2O2溶液 無 40℃ D 10mL20%H2O2溶液 MnO2粉末 40℃ A.A B.B C.C D.D 組卷:46引用:5難度:0.5 -
9.反應C(s)+H2O(g)?CO(g)+H2(g)在一可變容積的密閉容器中進行,下列條件的改變對其反應速率幾乎無影響的是( )
A.增加C的量 B.將容器的體積縮小一半 C.保持體積不變,通入H2O(g) D.保持壓強不變,充入N2使容器體積增大 組卷:258引用:9難度:0.8
二、填空題(本題包括8小題,共60分)
-
27.恒溫下,在容積為2L的恒容密閉容器A中通入1mol N2與1mol H2的混合氣體,發生如下反應:N2 (g)+3H2(g)?2NH3(g),△H<0,一段時間后,達到平衡,若平衡時氨氣的物質的量為0.4mol.
(1)計算此溫度時該反應的K=,平衡時H2的轉化率為.
(2)若在此溫度下,向另一容積為3L的恒容容器B中按物質的量分別為0.4mol、0.3mol、0.3mol充入N2、H2、NH3,此時,該反應是否處于平衡狀態(填“是”或“否”),此時若沒有達平衡,反應向方向進行,其判斷依據是.組卷:18引用:3難度:0.3 -
28.某密閉容器中發生反應:X(g)+3Y(g)?2Z(g) (正反應為放熱反應);
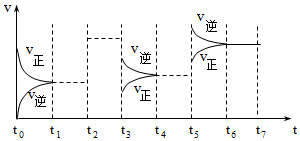
(1)上圖表示該反應的速率(v) 隨時間(t) 變化的關系,t2、t3、t5時刻外界條件有所改變,但都沒有改變各物質的初始加入量。請運用所學的化學原理分析t2、t3、t5時刻改變的條件:
t2時;t3時;t5時。
(2)下列時間段中,Z的百分含量最小的是(填字母)。
A.t1~t2
B.t2~t3
C.t4~t5
D.t6~t7組卷:93引用:2難度:0.6


