2022年北京市房山區高考化學一模試卷
發布:2024/12/29 18:30:3
一、選擇題每小題只有一個選項符合題意,共14小題,每小題3分。
-
1.近年來我國取得讓世界矚目的科技成果,化學功不可沒。下列說法不正確的是( )
A.“天和核心艙”電推進系統中的腔體采用氮化硼陶瓷屬于有機物 B.“北斗系統”組網成功,北斗芯片中的半導體材料為硅 C.“嫦娥五號”運載火箭用液氧液氫推進劑,產物對環境無污染 D.“奮斗者”號潛水器外殼材料為鈦合金,22號鈦元素屬于過渡元素 組卷:92引用:6難度:0.7 -
2.下列圖示或化學用語表示不正確的是( )

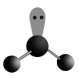
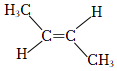
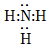
A.乙炔的空間結構模型 B.SO2的VSEPR模型 C.反-2-丁烯的結構簡式 D.氨分子的電子式 A.A B.B C.C D.D 組卷:31引用:2難度:0.7 -
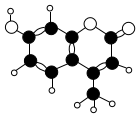 3.香豆素-4是一種激光染料、應用于激光器。香豆素-4由C、H、O三種元素組成,分子的球棍模型如圖所示。下列有關敘述不正確的是( )
3.香豆素-4是一種激光染料、應用于激光器。香豆素-4由C、H、O三種元素組成,分子的球棍模型如圖所示。下列有關敘述不正確的是( )A.屬于芳香族化合物 B.分子中有3種官能團 C.能與飽和溴水發生取代反應 D.1mol香豆素-4最多能與含2molNaOH的溶液反應 組卷:71引用:4難度:0.7 -
4.下列關于元素或物質性質的比較中,不正確的是( )
A.穩定性:HF>HCl>HBr>HI B.第一電離能:C>N>O>F C.酸性:HNO3>H3PO4>H2SiO3 D.電負性:C<N<O<F 組卷:51引用:1難度:0.9 -
5.下列實驗能達到對應目的的是( )
A.配制一定物質的量濃度的NaOH溶液 B.實驗室制取氨氣 C.含氨氣的尾氣吸收 D.除去CO2中的少量HCl 



A.A B.B C.C D.D 組卷:40引用:1難度:0.5 -
6.下列措施不能加快Zn與1mol/LH2SO4反應產生H2的速率的是( )
A.用Zn粉代替Zn粒 B.滴加少量的CuSO4溶液 C.升高溫度 D.再加入1mol/LCH3COOH溶液 組卷:144引用:5難度:0.7
二、填空題
-
18.金屬鈦(Ti)性能優越,被稱為繼鐵、鋁之后的“第三金屬”.工業上以鈦鐵礦(主要成分FeTiO3,含FeO、Al2O3、SiO2等雜質)為主要原料冶煉金屬鈦,其生產的工藝流程圖如下:

已知:2H2SO4(濃)+FeTiO3=TiOSO4+FeSO4+2H2O
(1)步驟I中發生反應的離子方程式:、.
(2)已知:TiO2+易水解,只能存在于強酸性溶液中.25℃時,難溶電解質溶解度(s)與pH關系如圖1,TiO(OH)2溶度積Ksp=1×10-29
①步驟Ⅲ加入鐵屑原因是.
②TiO2+水解的離子方程式為.
向溶液II中加入Na2CO3粉末的作用是.當溶液pH接近時,TiO(OH)2已沉淀完全.
(3)TiCl4Ti反應后得到Mg、MgCl2、Ti的混合物,可采用真空蒸餾的方法分離得到Ti,依據下表信息,需加熱的溫度略高于Mg℃即可.
(4)研究發現,可以用石墨作陽極、鈦網作陰極、熔融CaF2-CaO作電解質,利用右圖所示裝置獲得金屬鈣,并以鈣為還原劑,還原二氧化鈦制備金屬鈦.寫出陽極上所發生的反應式:TiCl4 Mg MgCl2 Ti 熔點/℃ -25.0 648.8 714 1667 沸點/℃ 136.4 1090 1412 3287 .組卷:54引用:2難度:0.3 -
19.某實驗小組在研究硝酸與銅的反應時,發現稀硝酸和銅反應后的混合液為藍色,而濃硝酸和銅反應后的混合液為綠色,為此對產生綠色的原因開展探究。按要求完成下列問題:
【猜想假設】
(1)假設1:。
假設2:硝酸銅溶液中溶解了NO2
【實驗操作及現象分析】
實驗一:向蒸餾水中不斷加入硝酸銅晶體,最終配成飽和溶液。配制過程中溶液顏色始終是藍色,未見綠色出現。
甲同學根據實驗一的現象證明了假設1不成立,請補全假設。
實驗二:
(2)甲同學在實驗一的基礎上繼續開展了實驗二,并初步驗證了假設2成立,他的實驗操作及現象是。
乙同學認為假設2不嚴謹,用以下實驗對假設2進行了深入探究:
實驗三:
(3)結合實驗三,乙同學認為假設2不嚴謹的證據是操作及試劑 現象 向濃硝酸和銅反應后的混合液中通入N2 大量紅棕色氣體放出,短時間內溶液仍保持綠色。長時間后變成藍色 。
(4)乙同學查閱資料發現:
①銅與濃硝酸反應后溶液呈現綠色是由于HNO2(或NO2-)與銅離子作用的結果。
②金屬和濃HNO3的反應一旦發生后速率不斷加快。原因是過程中有HNO2生成。如Cu和濃HNO3反應,開始生成的NO2溶于水形成HNO2,它再和Cu反應,速率就大大加快。
請依據資料完成以下離子反應方程式。
iNO2+H2O═HNO2++;
iiCu+2HNO2+=++;
iii2NO+4H++4NO3-=6NO2+2H2O。
實驗四:乙同學通過以下實驗證實了反應過程中HNO2的生成。
(5)結合化學用語,解釋實驗3產生該現象的原因是實驗 操作 現象 1 向試管a中加入lmL濃硝酸,再插入銅絲 快速產生紅棕色氣體,溶液變為綠色 2 向試管b中加入1mL濃硝酸,3滴蒸餾水,再插入銅絲 快速產生紅棕色氣體溶液變為綠色 3 向試管c中加入1mL濃硝酸,3滴30%H2O2,再插入銅絲 反應較慢,溶液變為藍色 。組卷:52引用:1難度:0.6


