蘇教版高一(上)高考題單元試卷:專題1 化學家眼中的物質世界(03)
發布:2024/11/7 20:0:2
一、選擇題(共18小題)
-
1.用固體樣品配制一定物質的量濃度的溶液,需經過稱量、溶解、轉移溶液、定容等操作。下列圖示對應的操作規范的是( )
A. 
稱量B. 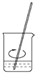
溶解C. 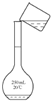
轉移D. 
定容組卷:1374引用:100難度:0.9 -
2.下列操作或裝置能達到實驗目的的是( )
A. 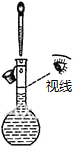
配制一定濃度的NaCl溶液B. 
除去氯氣中的HCl氣體C. 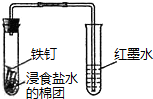
觀察鐵的吸氧腐蝕D. 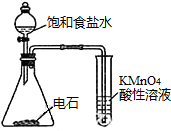 檢驗乙炔的還原性組卷:1624引用:16難度:0.7
檢驗乙炔的還原性組卷:1624引用:16難度:0.7 -
3.下列反應適用于實驗室制備氧氣的是( )
①高錳酸鉀熱分解2KMnO4K2MnO4+MnO2+O2↑△
②硝酸銨熱分解2NH4NO34H2O+N2↑+O2↑△
③過氧化氫催化分解2H2O22H2O+O2↑MnO2
④二氧化氮熱分解2NO22NO+O2.△A.只有① B.①和② C.①和③ D.①③④ 組卷:209引用:13難度:0.9 -
4.下列除雜方案錯誤的是( )
選項 被提純的物質 雜質 除雜試劑 A FeCl3(aq) Al3+(aq) NaOH溶液、鹽酸 B AlCl3(aq) Cu2+ Al粉 C NaHCO3(aq) Na2CO3(aq) CO2氣體 D FeCl3(aq) Cu2+ Fe粉 A.A B.B C.C D.D 組卷:936引用:62難度:0.7 -
5.下列操作不能達到目的的是( )
選項 目的 操作 A. 配制100 mL 1.0 mol/L CuSO4溶液 將25 g CuSO4?5H2O溶于100 mL蒸餾水中 B. 除去KNO3中少量NaCl 將混合物制成熱的飽和溶液,冷卻結晶,過濾 C. 在溶液中將MnO4-完全轉化為Mn2+ 向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 D. 確定NaCl溶液中是否混有Na2CO3 取少量溶液滴加CaCl2溶液,觀察是否出現白色渾濁 A.A B.B C.C D.D 組卷:1971引用:21難度:0.9 -
6.某同學采用硫鐵礦焙燒取硫后的燒渣(主要成分為Fe2O3、SiO2、Al2O3,不考慮其他雜質) 制取七水合硫酸亞鐵(FeSO4?7H2O),設計了如下流程:
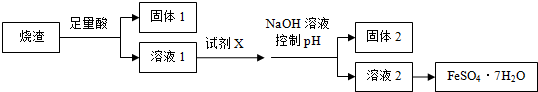
下列說法不正確的是( )A.溶解燒渣選用足量硫酸,試劑X選用鐵粉 B.固體1中一定含有SiO2,控制pH是為了使Al3+轉化為Al(OH)3,進入固體2 C.從溶液2得到FeSO4?7H2O產品的過程中,須控制條件防止其氧化和分解 D.若改變方案,在溶液1中直接加NaOH至過量,得到的沉淀用硫酸溶解,其溶液經結晶分離也可得到FeSO4?7H2O 組卷:1975引用:43難度:0.7
三、解答題(共2小題)
-
19.氯化鉀樣品中含有少量碳酸鉀、硫酸鉀和不溶于水的雜質.為了提純氯化鉀,先將樣品溶于適量水中,充分攪拌后過濾,在將濾液按圖所示步驟進行操作.
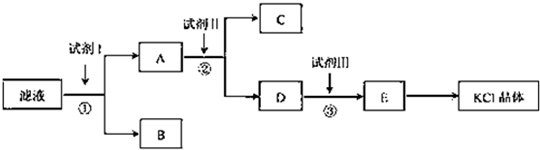
回答下列問題:
(1)起始濾液的pH7(填“大于”、“小于”或“等于”),其原因是.
(2)試劑I的化學式為,①中發生反應的離子方程式為.
(3)試劑Ⅱ的化學式為,②中加入試劑Ⅱ的目的是;
(4)試劑Ⅲ的名稱是,③中發生反應的離子方程式為;
(5)某同學稱取提純的產品0.7759g,溶解后定容在100mL容量瓶中,每次取25.00mL溶液,用0.1000mol?L-1的硝酸銀標準溶液滴定,三次滴定消耗標準溶液的平均體積為25.62mL,該產品的純度為.組卷:579引用:28難度:0.5 -
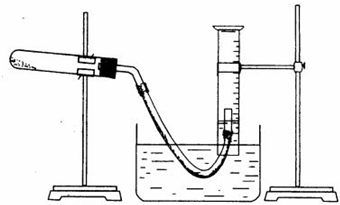 20.某學生利用氯酸鉀分解制氧氣的反應,測定氧氣的摩爾質量。實驗步驟如下:
20.某學生利用氯酸鉀分解制氧氣的反應,測定氧氣的摩爾質量。實驗步驟如下:
①把適量的氯酸鉀粉末和少量二氧化錳粉末混合均勻,放入干燥的試管中,準確稱量,質量為a g。
②裝好實驗裝置。
③檢查裝置氣密性。
④加熱,開始反應,直到產生一定量的氣體。
⑤停止加熱(如圖,導管出口高于液面)。
⑥測量收集到氣體的體積。
⑦準確稱量試管和殘留物的質量為b g。
⑧測量實驗室的溫度。
⑨把殘留物倒入指定的容器中,洗凈儀器,放回原處,把實驗桌面收拾干凈。
⑩處理實驗數據,求出氧氣的摩爾質量。
回答下列問題:
(1)如何檢查裝置的氣密性?。
(2)以下是測量收集到氣體體積必須包括的幾個步驟;①調整量筒內外液面高度使之相同;②使試管和量筒內的氣體都冷卻至室溫;③讀取量筒內氣體的體積。這三步操作的正確順序是:(請填寫步驟代號)
(3)測量收集到氣體體積時,如何使量筒內外液面的高度相同?。
(4)如果實驗中得到的氧氣體積是c L(25℃、1.01×105 Pa),水蒸氣的影響忽略不計,氧氣的摩爾質量的計算式為(含a、b、c,不必化簡):M(O2)=。組卷:622引用:17難度:0.5


