2015-2016學年山東省濱州市博興三中高三(上)開學化學試卷
發布:2024/11/29 19:30:2
一、選擇題(本題包括15小題,每小題2分,共30分,每小題只有一個選項符合題意)
-
1.8月12日天津港發生爆炸,專家對爆炸事故原因猜測認為硝化棉或者硫化鈉自燃是最可能的點火源,因此化學藥品的安全存放是非常重要的.下列有關化學藥品的存放說法不正確的是( )
A.液溴易揮發,應用水液封并放在冷暗處保存 B.金屬鈉遇到氧氣立即反應,應保存在煤油中或者液體石蠟里 C.硝酸見光易分解,應用棕色廣口試劑瓶保存 D.碳酸鈉雖然屬于鹽,但是其水溶液呈堿性,應用帶橡膠塞的試劑瓶保存 組卷:72引用:8難度:0.9 -
2.化學是你,化學是我,化學深入我們生活。下列說法正確的是( )
A.木材纖維和土豆淀粉遇碘水均顯藍色 B.食用花生油和雞蛋清都能發生水解反應 C.包裝用材料聚乙烯和聚氯乙烯都屬于烴 D.PX項目的主要產品對二甲苯屬于飽和烴 組卷:1121引用:38難度:0.9 -
3.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.2.0 O與D2O的混合物中所含中子數為NAgH182B.常溫常壓下,4.4 g乙醛所含σ鍵數目為0.7NA C.標準狀況下,5.6LCO2與足量Na2O2反應轉移的電子數為0.5NA D.50mL 12mol/L鹽酸與足量MnO2共熱,轉移的電子數為0.3NA 組卷:3747引用:29難度:0.7 -
4.金屬Ti(鈦)是一種具有許多優良性能的較為昂貴的金屬,鈦和鈦合金被認為是21世紀的重要金屬材料.
某化學興趣小組用實驗探究Ti、Mg、Cu的活潑性順序.他們在相同溫度下,取大小相同的三種金屬薄片,分別投入等體積等濃度的足量稀鹽酸中,觀察現象如下:下列有關三種金屬的說法正確的是( )金屬學 Ti Mg Cu 金屬表面現象 放出氣泡速度緩慢 放出氣泡速度快 無變化 A.三種金屬的活潑性由強到弱的順序是Ti、Mg、Cu B.若鈦粉中混有Mg,提純Ti時可用稀鹽酸除去Mg C.用Ti從CuSO4溶液中置換出Cu是工業制取Cu的很好途徑 D.Cu和稀鹽酸不發生化學反應 組卷:53引用:11難度:0.7 -
5.常溫下,下列溶液中各組離子一定大量共存的是( )
A.使甲基橙呈紅色的溶液中:Na+、AlO2-、NO3-、CO32- B.c(ClO-)=1.0 mol?L-1溶液:Na+、SO32-、S2-、Cl- C.含有0.1 mol?L-1 HCO3-的溶液:Na+、Fe3+、NO3-、C6H5O- D. =0.1 mol?L-1的溶液:Na+、K+、CO32-、NO3-KWc(H+)組卷:2引用:1難度:0.7 -
6.下列有關實驗裝置進行的相應實驗,能達到實驗目的的是( )
A. 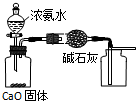
用此圖裝置制取并收集干燥純凈的NH3B. 
用此圖裝置實驗室制備Fe(OH)2C. 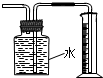
此圖裝置收集并測量Cu與濃硝酸反應產生的氣體及體積D. 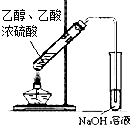
此圖裝置可用于實驗室制取乙酸乙酯組卷:47引用:10難度:0.7 -
7.等物質的量濃度的下列稀溶液:①CH3COONa溶液;②NaHCO3溶液;③X溶液;④Ba(OH)2溶液。它們的pH依次增大,則X溶液不可能是( )
A.Na2CO3溶液 B.Na2SiO3溶液 C.NaOH溶液 D.NaHSO3溶液 組卷:41引用:3難度:0.7 -
8.通過復習總結,下列歸納正確的是( )
A.Na2O,NaOH,Na2CO3,NaCl,Na2SO4,Na2O2都屬于鈉的含氧化合物 B.簡單非金屬陰離子只有還原性,而金屬陽離子不一定只有氧化性 C.一種元素可能有多種氧化物,但同種化合價只對應有一種氧化物 D.物質發生化學變化一定有化學鍵斷裂與生成,并伴有能量變化,而發生物理變化就一定沒有化學鍵斷裂或生成 組卷:121引用:6難度:0.7
三、填空題(共55分)
-
23.SO2的含量是空氣質量日報中一項重要檢測指標,請結合所學知識回答下列問題.
(1)工業制硫酸過程中,SO2催化氧化的原理為:
2SO2(g)+O2(g)2SO3(g)催化劑△
T℃時,向某密閉容器中充入一定SO2(g)和O2(g),發生上述反應,測得SO2(g)的平衡轉化率(a)與體系總壓強(p)的關系如圖1所示.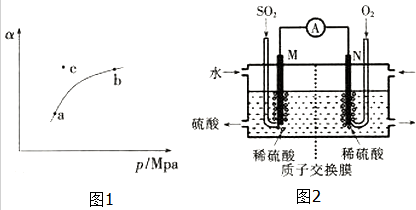
①a、b兩點對應的平衡常數K(a)K(b)(填“>”、“<”或“=”,下同),SO2濃度c(a)c(b).
②c點時,反應速率v(正)v(逆).
(2)電化學法處理SO2.
硫酸工業尾氣中的SO2經分離后,可用于制備硫酸,同時獲得電能,裝置如圖2所示(電極均為惰性材料):
①M極發生的電極反應式為.
②若使該裝置的電流強度達到2.0A,理論上每分鐘應向負極通入標準狀況下氣體的體積為L(已知:1個e-所帶電量為1.6×10-19C).
(3)溶液法處理SO2.
已知常溫下H2SO3和H2CO3的電離常數如表所示:
常溫下,將SO2緩慢通入100mL 0.2mol?L-1的Na2CO3溶液中,當通入448mLSO2時(已折算為標準狀況下的體積,下同),發生的離子方程式為電離常數
酸K1 K2 H2SO3 1.3×10-2 6.3×10-8 H2CO3 4.2×10-7 5.6×10-11 ;當通入896mLSO2時,所得溶液呈弱酸性,溶液中各離子濃度由大到小的順序為.組卷:73引用:1難度:0.1 -
24.利用芳香烴X和烯烴Y可以合成紫外線吸收劑BAD。
已知:G不能發生銀鏡反應,B遇FeCl3溶液顯紫色,C到D的過程為引入羧基(-COOH)的反應。其中BAD結構簡式為: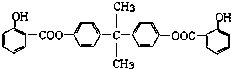
BAD的合成路線如下: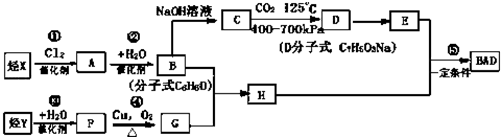
試回答下列問題:
(1)寫出結構簡式YD。
(2)屬于加成反應的有(填數字序號)。
(3)1molBAD最多可與含molNaOH的溶液完全反應。
(4)寫出方程式反應④。F+E。
(5)E有多種同分異構體,判斷符合下列要求的同分異構體數目為種。
①能發生銀鏡反應②遇FeCl3溶液顯紫色③核磁共振氫譜圖中有四個吸收峰。組卷:122引用:12難度:0.3


