2022-2023學年廣東省廣州市番禺中學高一(下)期中化學試卷
發(fā)布:2024/4/20 14:35:0
一、單選題(每題3分,共48分)
-
1.化學與生活密切相關,下列有關說法正確的是( )
A.電池體積很小,所含污染物有限,可隨意丟棄 B.SiO2可用作計算機芯片 C.SO2具有氧化性,可用作食品抗氧化劑 D.S粉可除去溫度計破碎時灑落的Hg 組卷:34引用:3難度:0.7 -
2.下列有關硅及硅酸鹽材料的說法正確的是( )
A.硅酸鈉屬于鹽,不屬于堿,所以硅酸鈉可以保存在磨口玻璃塞試劑瓶中 B.高純度的硅單質(zhì)廣泛用于制作光導纖維 C.普通玻璃、陶器瓷器、水泥等均屬于硅酸鹽材料 D.玻璃塞試劑瓶穩(wěn)定性好,可以保存所有的酸,但不能保存氫氧化鈉固體 組卷:35引用:1難度:0.6 -
 3.為了研究化學反應的能量變化情況,某同學設計了如圖所示裝置。當向盛有試劑甲的試管中加入試劑乙時(必要時可以攪拌),U形管中液面呈現(xiàn)出左高右低的現(xiàn)象,則試劑甲、乙的組合是( )
3.為了研究化學反應的能量變化情況,某同學設計了如圖所示裝置。當向盛有試劑甲的試管中加入試劑乙時(必要時可以攪拌),U形管中液面呈現(xiàn)出左高右低的現(xiàn)象,則試劑甲、乙的組合是( )A.甲:鎂條 乙:鹽酸 B.甲:氫氧化鋇晶體 乙:氯化銨 C.甲:氫氧化鋇 乙:硫酸 D.甲:二氧化錳 乙:雙氧水 組卷:34引用:1難度:0.6 -
4.下列敘述中正確的個數(shù)為( )
①通過豆科植物的根瘤菌將氮氣轉化為含氮化合物,是自然固氮的途徑之一
②硝酸見光分解,所以硝酸一般盛放在棕色試劑瓶中
③CO、NO、NO2都是大氣污染氣體,在空氣中能穩(wěn)定存在
④常溫下,可以用鐵制容器盛裝濃硝酸,這是因為鐵在常溫下與濃硝酸不反應
⑤NH4Cl受熱易分解,可用于實驗室制氨氣
⑥N2性質(zhì)穩(wěn)定,工業(yè)生產(chǎn)金屬鎂時,為防止其氧化,可以用N2作保護氣A.4個 B.3個 C.2個 D.1個 組卷:52引用:2難度:0.7 -
 5.如圖所示裝置制取、提純并收集表中的四種氣體(a、b、c表示相應儀器中加入的試劑),其中可行的是( )
5.如圖所示裝置制取、提純并收集表中的四種氣體(a、b、c表示相應儀器中加入的試劑),其中可行的是( )氣體 a b c A CO2 鹽酸 碳酸鈣 飽和NaHCO3溶液 B SO2 濃硫酸 Fe 濃硫酸 C NH3 濃氨水 生石灰 堿石灰 D Cl2 濃鹽酸 MnO2粉末 濃硫酸 A.A B.B C.C D.D 組卷:39引用:3難度:0.7 -
6.下列有關熱化學方程式的敘述正確的是( )
A.已知CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H,則△H代表甲烷的燃燒熱 B.已知4P(紅磷,s)═P4(白磷,s)△H>0,則白磷比紅磷穩(wěn)定 C.含20.0g NaOH的稀溶液與稀硫酸完全中和,放出28.7kJ的熱量,則表示該反應中和熱的熱化學方程式為:2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H=-57.4kJ/mol D.S(s)+O2(g)═SO2(g)△H1 S(g)+O2(g)=SO2(g)△H2 則△H1>△H2 組卷:18引用:2難度:0.5
二、填空與簡答
-
19.回答下列問題
(1)如圖所示是一種原電池的裝置圖,請回答: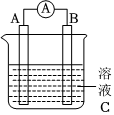
若溶液C為氯化鐵溶液,電流表指針發(fā)生偏轉,A、B電極材料分別為銅和銀,則A、B電極上發(fā)生的電極反應分別為、。
(2)CO與H2反應還可制備CH3OH,CH3OH可作為燃料使用,用CH3OH和O2組合形成的質(zhì)子交換膜燃料電池的結構示意如圖所示: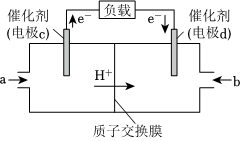
電池總反應為2CH3OH+3O2=2CO2+4H2O,a口通入的物質(zhì)是,若線路中轉移6mol電子,則消耗的O2在標準狀況下的體積為L。
(3)家用液化氣中主要成分之一是丁烷,當1g丁烷氣體完全燃燒并生成CO2和氣態(tài)水時,放出熱量50kJ每摩爾水氣化時吸收40kJ的熱量,試寫表示丁烷燃燒熱的熱化學方程式:。組卷:34引用:1難度:0.5 -
20.用如圖方法回收廢舊CPU中的單質(zhì)Au(金),Ag和Cu。
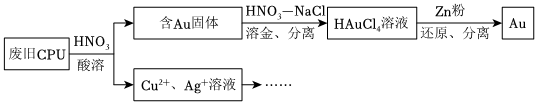
已知:①濃硝酸不能單獨將Au溶解。
②HAuCl4=H++。AuCl-4
(1)酸溶后經(jīng)操作,將混合物分離。
(2)濃、稀HNO3均可作酸溶試劑。溶解等量的Cu消耗HNO3的物質(zhì)的量不同,寫出消耗HNO3物質(zhì)的量少的反應的化學方程式:。
(3)HNO3-NaCl與王水[V(濃硝酸):V(濃鹽酸)=1:3]溶金原理相同。關于溶金的下列說法正確的是。
A.用到了HNO3的氧化性
B.王水中濃鹽酸的主要作用是增強溶液的酸性
C.用濃鹽酸與NaNO3也可使Au溶解
(4)若用Zn粉將溶液中的1molHAuCl4完全還原,則參加反應的Zn的物質(zhì)的量是mol。
(5)用適當濃度的鹽酸、NaCl溶液、氨水與鐵粉,可按照如圖方法從酸溶后的溶液中回收Cu和Ag(圖中標注的試劑和物質(zhì)均不同)。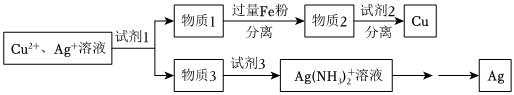
試劑1是,物質(zhì)2是。組卷:23引用:1難度:0.4


