2021-2022學年浙江省杭州市九年級(上)質檢科學試卷(三)
發布:2024/4/20 14:35:0
一、選擇題(本大題共60分,每小題3分,每小題只有一個選項符合題意)
-
1.下列實驗操作中,不正確的是( )
A. 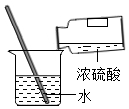
稀釋濃硫酸B. 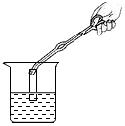
測溶液pHC. 
聞食醋D. 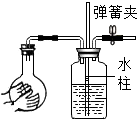 檢查裝置氣密性組卷:21引用:9難度:0.5
檢查裝置氣密性組卷:21引用:9難度:0.5 -
2.電腦芯片的制作要用到高純度的硅,目前廣泛采用石英砂(主要成分是 SiO2)為原料制取,其中有一步反應為:SiO2+2C
Si+2CO↑。下列對該反應分析正確的是( )高溫A.該反應屬于復分解反應 B.SiO2發生了還原反應 C.碳元素化合價由0價變為+4價 D.該反應利用了CO的還原性 組卷:1引用:1難度:0.5 -
3.明代于謙《石灰吟》中“千錘萬鑿出深山,烈火焚燒若等閑,粉身碎骨渾不怕,要留清白在人間”四句詩所描述的四種物質分別是( )
A.石灰石、生石灰、熟石灰、碳酸鈣 B.碳酸鈣、生石灰、熟石灰、石灰石 C.生石灰、熟石灰、石灰石、碳酸鈣 D.石灰石、碳酸鈣、熟石灰、生石灰 組卷:6引用:1難度:0.5 -
4.化學實驗過程中一定要注意安全,萬一發生事故也不必驚慌,要冷靜地處理。下列做法錯誤的是( )
A.不慎將氫氧化鈉溶液沾到皮膚上,立刻用大量水沖洗,再涂上硼酸溶液 B.不慎將白磷灑落在桌面上,立刻掃入盛水的燒杯中 C.不慎將酒精燈碰倒,灑出的酒精在桌上燃燒起來,立刻用濕布蓋滅 D.不慎將濃硫酸沾到皮膚上,立刻用大量水沖洗,再涂上 3%~5%食醋 組卷:16引用:1難度:0.5 -
5.四只燒杯中分別盛有稀鹽酸,并滴加了數滴紫色石蕊試液。現分別向這四只燒杯中不斷加入下列物質,直至過量,其中能使溶液最后呈紫色的物質是( )
A.CaO B.NaOH C.Mg(OH)2 D.AgNO3 組卷:14引用:3難度:0.5 -
6.將一定質量金屬M的粉末放入盛有Cu(NO3)2溶液的燒杯中,充分反應后溶液呈無色;繼續向燒杯中加入一定量的AgNO3溶液,待充分反應后過濾,得藍色濾液和濾渣.根據實驗分析,以下結論錯誤的是( )
A.金屬活動性順序:M>Cu>Ag B.濾液中一定含有M的陽離子和Cu2+ C.濾渣中一定含有Ag和Cu D.向濾液中滴加稀鹽酸,可能產生白色沉淀 組卷:32引用:2難度:0.5 -
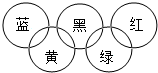 7.奧運會會標是五環旗,假定奧運五環旗中的每一環或每種顏色表示一種物質,相連的環(物質)間在一定條件下能發生常見反應,不相連的環(物質)間不能發生反應,且四種反應中必須包含化合反應、置換反應及復分解反應,適合的一組物質是( )
7.奧運會會標是五環旗,假定奧運五環旗中的每一環或每種顏色表示一種物質,相連的環(物質)間在一定條件下能發生常見反應,不相連的環(物質)間不能發生反應,且四種反應中必須包含化合反應、置換反應及復分解反應,適合的一組物質是( )選項 藍 黃 黑 綠 紅 A CO2 KOH 溶液 FeCl3溶液 Cu O2 B H2O NH3 稀硫酸 NaOH 溶液 Al(OH)3 C O2 Zn 稀硫酸 NaOH 溶液 CO2 D O2 Fe CuSO4溶液 NaOH 溶液 稀鹽酸 A.A B.B C.C D.D 組卷:4引用:1難度:0.5 -
8.下列主要成分中含有少量雜質,選用試劑進行檢驗雜質、除去雜質是化學實驗中的常見實際問題,若一種試劑既能檢驗所含雜質、又能除去雜質,該試劑我們就能稱為“高效試劑”,下列選項中不能稱為“高效試劑”(所加試劑均適量且忽略分離步驟)的是( )
選項 主要成分 所含的雜質 “高效試劑” A HNO3 H2SO4 Ba(NO3)2 B BaCl2 HCl BaCO3 C CaCl2 HCl Ca(OH)2 D MgCl2 MgSO4 BaCl2 A.A B.B C.C D.D 組卷:25引用:4難度:0.5 -
9.建立微觀和宏觀之間的聯系是一種科學的思維方式,下列敘述合理的是( )
A.溫度計受熱時水銀柱上升,是因為汞原子受熱時體積變大 B.C-12和C-14屬于同種元素,是因為它們的原子結構完全相同 C.稀硫酸和稀鹽酸都能使石蕊試液變紅,是因為兩種酸均能電離出酸根陰離子 D.向氫氧化鋇溶液中逐滴滴加稀硫酸,溶液的導電能力減弱,是因為溶液中自由移動離子減少 組卷:30引用:3難度:0.5 -
10.小明同學往氫氧化鈉溶液中滴加稀鹽酸研究中和反應時,忘記了滴加酸堿指示劑。為了確認滴加的鹽酸是否已經過量,從燒杯中取少量反應后的溶液于試管中,用某種試劑進行檢驗。下表是小明同學設計的實驗方案,其中不正確的是( )
實驗方案 使用的試劑 判斷的方法 A 鐵粉 如果有氣泡產生,表明鹽酸已經過量 B pH試紙 如果pH<7,表明鹽酸已經過量 C 硝酸銀溶液 如果有白色沉淀產生,表明鹽酸已經過量 D 紫色石蕊試劑 如果溶液變成紅色,表明鹽酸已經過量 A.A B.B C.C D.D 組卷:82引用:21難度:0.5 -
11.下列物質的變化中,只有加酸才能一步實現的是( )
A.CaCO3→CO2 B.Zn→ZnSO4 C.CuO→CuCl2 D.KOH→KCl 組卷:194引用:10難度:0.5
四、解答題(本大題共28分)
-
34.甲、乙、丙、丁四位同學用鋅和稀硫酸反應,所得相關數據記錄如下:(誤差忽略不計)
計算:甲 乙 丙 丁 取用的稀硫酸的質量/g 100 100 100 100 加入金屬的質量/g x 1.25x 1.5x 2x 生成氫氣的質量/g 0.4 0.5 0.6 0.6
(1)甲同學加入的金屬鋅的質量x。
(2)稀硫酸中溶質的質量分數。組卷:2引用:1難度:0.5 -
35.燃燒是人類最早有意識利用的化學反應,火的使用標志著人類文明的偉大進步。

(1)原始人使用木柴燃燒釋放的能烘烤食物,告別了茹毛飲血的野蠻時代。現在,人們仍然利用燃料燃燒蒸煮食物,家用液化氣的成分之一丙烯(C3H6)燃燒的化學方程式為。從微觀角度分析丙烯液化與丙烯燃燒兩個過程的主要區別。
(2)燃燒產生的高溫可用于冶煉金屬。木炭在高溫條件下還原氧化銅生成銅和二氧化碳,該反應的化學方程式為,基本反應類型是。銅的使用使人類社會邁入青銅器時代。
(3)在大棚中燃燒沼氣可以提高作物產量,沼氣的主要成分燃燒的微觀示意圖如圖所示,下列說法正確的有。
A.參加反應的 與
與 的質量比為16:32
的質量比為16:32
B.反應前后各元素的化合價都不變
C.該反應屬于置換反應
D.點燃沼氣前,需要檢驗純度,防止發生爆炸
(4)大棚中燃燒沼氣可以提高作物產量的原因是(寫出兩條)。組卷:4引用:1難度:0.5


