2021-2022學(xué)年甘肅省武威七中高二(上)期中化學(xué)試卷
發(fā)布:2024/5/23 8:0:8
一、選擇題(每題3分,共60分)
-
1.下列對化學(xué)反應(yīng)的認識,錯誤的是( )
A.會引起化學(xué)鍵的變化 B.會產(chǎn)生新物質(zhì) C.必然引起物質(zhì)狀態(tài)的變化 D.必然伴隨著能量的變化 組卷:699引用:85難度:0.9 -
2.關(guān)于化學(xué)反應(yīng)與能量的說法正確的是( )
A.中和反應(yīng)是吸熱反應(yīng) B.燃燒屬于放熱反應(yīng) C.化學(xué)鍵斷裂放出能量 D.反應(yīng)物總能量與生成物總能量一定相等 組卷:184引用:51難度:0.9 -
3.對于在密閉容器中、一定條件下進行的可逆反應(yīng)N2(g)+3H2(g)?2NH3(g),能說明反應(yīng)已達到平衡狀態(tài)的是( )
A.各物質(zhì)體積分數(shù)相等 B.c(NH3)保持不變 C.各物質(zhì)濃度相等 D.c(NH3):c(N2):c(H2)=2:1:3 組卷:61引用:18難度:0.5 -
4.在可逆反應(yīng)中,改變下列條件一定能加快反應(yīng)速率的是( )
①增大反應(yīng)物濃度 ②升高溫度 ③增大壓強 ④使用催化劑 ⑤增大表面積.A.全部 B.①② C.①②③ D.①②③④ 組卷:8引用:2難度:0.9 -
5.下列說法正確的是( )
A.ΔH的單位是kJ B.相同條件下,生成物的總能量高于反應(yīng)物的總能量時,反應(yīng)吸熱,ΔH>0 C.在任何條件下,化學(xué)反應(yīng)的焓變都等于化學(xué)反應(yīng)的反應(yīng)熱 D.任何化學(xué)反應(yīng)的反應(yīng)熱均可通過實驗直接測定 組卷:1引用:1難度:0.7 -
6.在醋酸中存在電離平衡:CH3COOH?CH3COO-+H+,要使電離平衡右移且c(H+)增大,應(yīng)采取的措施是( )
A.加入NaOH(s) B.加入鹽酸 C.加蒸餾水 D.升高溫度 組卷:74引用:15難度:0.9 -
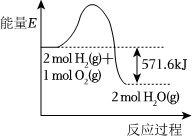 7.如圖所示,下列敘述正確的是( )
7.如圖所示,下列敘述正確的是( )A.生成物能量總和大于反應(yīng)物能量總和 B.生成2molH2O(l)要吸收571.6kJ熱量 C.2H2O(g)=2H2(g)+O2(g)ΔH=+571.6kJ?mol-1 D.2H2(g)+O2(g)=2H2O(l)ΔH>-571.6kJ?mol-1 組卷:2引用:4難度:0.5 -
8.下列關(guān)于能量變化的說法正確的是( )
A.“冰,水為之,而寒于水”說明相同質(zhì)量的水和冰相比較,冰的能量高 B.化學(xué)反應(yīng)在物質(zhì)變化的同時,伴隨著能量變化,其表現(xiàn)形式只有吸熱和放熱兩種 C.1molH2的能量大于2molH的能量 D.化學(xué)反應(yīng)遵循質(zhì)量守恒的同時,也遵循能量守恒 組卷:6引用:3難度:0.5
三、計算題(每題10分,共20分。)
-
24.在一定溫度下,密閉容器中發(fā)生反應(yīng):2NO2?2NO+O2,經(jīng)2min后,測得混合氣中NO2濃度為0.06mol?L-1,O2的濃度為0.12mol?L-1,且各物質(zhì)的濃度不再發(fā)生變化。
求:
(1)NO2的起始濃度。
(2)2min時NO2的轉(zhuǎn)化率。
(3)2min內(nèi)生成NO的化學(xué)反應(yīng)速率。組卷:5引用:2難度:0.7 -
25.某溫度下,將H2(g)和I2(g)各1mol的氣態(tài)混合物充入2L的密閉容器中,充分反應(yīng),5min后達到平衡,測得c(HI)=0.2mol/L.
(1)計算從反應(yīng)開始至達到平衡,用H2(g)表示的反應(yīng)速率.
(2)求該反應(yīng)的平衡常數(shù).
(3)保持溫度不變,若向上述容器中充入H2(g)和I2(g)各2mol,求達到平衡時I2(g)的物質(zhì)的量濃度.組卷:28引用:3難度:0.3


