2021-2022學年黑龍江省哈爾濱市德強高級中學高一(上)月考化學試卷(10月份)
發布:2024/4/20 14:35:0
一、單選題(16道小題,共48分)
-
1.人體正常的血紅蛋白應含Fe2+.若誤食外表與食鹽相近的亞硝酸鹽,則導致血紅蛋白中的Fe2+轉化成Fe3+而中毒,服用維生素C可解除亞硝酸鹽中毒,下列敘述中正確的是( )
A.亞硝酸鹽是還原劑 B.維生素C是還原劑 C.維生素C是氧化劑 D.亞硝酸鹽被氧化 組卷:24引用:6難度:0.7 -
2.下列說法正確的是( )
A.單質中只含一種元素,所以只含一種元素的物質一定是單質 B.化學變化前后物質的質量總和不變,所以1g H2和1g O2一定能夠生成2g H2O C.堿性溶液能使酚酞溶液變紅,所以能使酚酞溶液變紅的物質一定呈堿性 D.根據分散系是否具有丁達爾效應將分散系分為溶液、膠體、濁液 組卷:18引用:1難度:0.8 -
3.下列說法中正確的是( )
A.熔融的氯化氫不能導電,所以氯化氫是非電解質 B.SO2氣體溶于水能導電,所以SO2是電解質 C.氯化銀難溶于水,所以氯化銀是非電解質 D.蔗糖溶液和熔融的蔗糖都不能導電,所以蔗糖是非電解質 組卷:77引用:7難度:0.6 -
4.下列物質分類的正確組合是( )
堿 酸 鹽 堿性氧化物 酸性氧化物 A Cu2(OH)2CO3 H2SO4 NaHCO3 SiO2 CO2 B NaOH HCl NaCl Na2O CaO C NaOH NH3 CaCl2 MgO SO2 D KOH HNO3 CaCO3 CaO SO3 A.A B.B C.C D.D 組卷:74引用:6難度:0.7 -
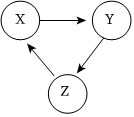 5.X、Y、Z有如圖所示的轉化關系(“→”表示反應一步實現,部分物質和反應條件已略去),則符合要求的X、Y、Z依次為( )
5.X、Y、Z有如圖所示的轉化關系(“→”表示反應一步實現,部分物質和反應條件已略去),則符合要求的X、Y、Z依次為( )A.Cu、CuO、Cu(OH)2 B.C、CO、H2CO3 C.CaO、Ca(OH)2、CaCO3 D.H2O2、H2、H2O 組卷:28引用:8難度:0.5 -
6.下列電離方程式錯誤的是( )
A.KAl(SO4)2═K++Al3++2SO42- B.NaHCO3=Na++HCO3- C.H2SO4═2H++SO42- D.NH3?H2O═NH4++OH- 組卷:37引用:4難度:0.9
二、非選擇題(3道小題,共52分)
-
18.離子反應是中學化學中重要的反應類型,回答下列問題:
(1)在發生離子反應的反應物或生成物中,一定存在(填編號)。
①單質 ②氧化物 ③電解質 ④鹽 ⑤化合物
(2)將兩種化合物一起溶于水得到一種無色透明溶液,溶液中含有下列離子中的某些離子:K+、Mg2+、Fe3+、Ba2+、SO42-、OH-、CO32-和Cl-,取該溶液進行如下實驗:
Ⅰ取少量溶液滴入紫色石蕊試液,溶液呈藍色。
Ⅱ取少許溶液滴入BaCl2溶液,無白色沉淀產生。
Ⅲ取少許溶液先滴加硝酸再加AgNO3 ;溶液,產生白色沉淀。
Ⅳ再取少許原溶液滴入少量H2SO4溶液,有白色沉淀產生。
①根據以上現象判斷,原溶液中肯定不存在的離子是肯定存在的離子是。
②寫出實驗Ⅲ和Ⅳ中可能發生反應的離子方程式
Ⅲ,
Ⅳ
③如溶液中各種離子的濃度相等,確定溶液中(填有或無)K+.判斷依據是組卷:200引用:11難度:0.4 -
19.按要求填空。
(1)配平氧化還原離子方程式:Cu++NO-3H+=NO↑+Cu2++H2O。
(2)已知KMnO4與濃鹽酸室溫下可發生如下反應。2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O
①用“雙線橋法”標出上述反應的電子轉移情況。
②此反應體現HCl的性和性,氧化產物是,生成71gCl2時消耗的還原劑的質量為g。
③若分別用①KMnO4(還原產物是Mn2+);②MnO2(還原產物是Mn2+);③Ca(ClO)2(還原產物是Cl2)氧化濃鹽酸制備氯氣,當濃鹽酸足量且消耗這三種氧化劑的數目相同時,生成氯氣分子的數目之比是。
(3)油畫所用顏料含有某種白色鉛化合物,置于空氣中天長日久就會變成黑色,從而使油畫色彩變暗。若用H2O2來“清洗”,則可將PbS轉變成白色的PbSO4,從而使油畫的色彩“復原”。上述“清洗”反應的化學方程式為,此反應中H2O2為劑。組卷:45引用:1難度:0.5


