2022年湖南省六校高考化學聯考試卷
發布:2024/11/7 9:30:3
一、選擇題:本題共10小題,每小題3分,共30分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.下列生產、生活和科學中的化學敘述錯誤的是( )
A.我國是全球最大的鋰電池生產國,鋰電池的比能量高、電壓高、工作溫度寬、可儲存時間長 B.制作宇航服所使用的聚酯纖維屬于合成纖維 C.漂白液、漂白粉、漂粉精既可作漂白棉、麻、紙張的漂白劑,也可用作游泳池和環境的消毒劑 D.熔融燒堿時,不能使用普通玻璃坩堝、石英坩堝、陶瓷坩堝、鐵坩堝,可使用鎳坩堝 組卷:99引用:3難度:0.7 -
2.設NA是阿伏加德羅常數的值,下列說法正確的是( )
A.60g冰醋酸與葡萄糖的混合物中含有的原子數為8NA B.標準狀況下,4.48LN2與3.36L2H2充分反應后,所得NH3分子數為0.25NA C.pH=5的NH4Cl溶液中,水電離出來的OH-的數目為10-5NA D.5.6g鐵粉與足量的水蒸氣在高溫下反應,轉移電子數為0.3NA 組卷:34引用:1難度:0.5 -
3.下列實驗設計不能達到實驗目的的是( )
選項 實驗目的 實驗設計 A 驗證犧牲陽極的陰極保護法 用Fe作被保護電極、Zn作輔助電極,以經過酸化的3%NaCl溶液作電解質溶液,連接成原電池裝置。一段時間后,取Fe電極區域的少量溶液于潔凈試管中,滴加黃色K3[Fe(CN)6]溶液 B 探究氯氣與氫氣的反應 在空氣中點燃氫氣,然后把導管緩緩伸入盛滿氯氣的集氣瓶中 C 制備乙酸乙酯 在一支試管中加入2mL濃硫酸,然后邊振蕩試管邊緩慢加入2mL乙醇和3mL乙酸,連接好裝置,加熱,將產生的蒸氣經導管通到飽和Na2CO3溶液的液面下 D 探究濃度對化學反應速率的影響 取編號為①、②的兩支試管,各加入4mL0.01mol?L-1的酸性KMnO4溶液,然后向①試管中加入2mL0.1mol?L-1的H2C2O4溶液;向②試管中加入2mL0.2mol?L-1的H2C2O4溶液,分別記錄溶液褪色所需的時間 A.A B.B C.C D.D 組卷:61引用:2難度:0.5 -
 4.重鉻酸鉀(K2Cr2O7)俗稱紅礬,是一種重要的化工產品。將鉻鐵礦[主要成分為亞鉻酸亞鐵Fe(CrO2)2]和純堿置于坩堝中,在空氣中加熱,發生反應:Fe(CrO2)2+Na2CO3+O2→Na2CrO4+Fe2O3+CO2,將生成物加水溶解,過濾掉Fe2O3,得Na2CrO4溶液,酸化后,加KCl溶液,經過一系列操作可制得K2Cr2O7。已知相關物質溶解度曲線如圖所示。對于以上操作過程,下列說法正確的是( )
4.重鉻酸鉀(K2Cr2O7)俗稱紅礬,是一種重要的化工產品。將鉻鐵礦[主要成分為亞鉻酸亞鐵Fe(CrO2)2]和純堿置于坩堝中,在空氣中加熱,發生反應:Fe(CrO2)2+Na2CO3+O2→Na2CrO4+Fe2O3+CO2,將生成物加水溶解,過濾掉Fe2O3,得Na2CrO4溶液,酸化后,加KCl溶液,經過一系列操作可制得K2Cr2O7。已知相關物質溶解度曲線如圖所示。對于以上操作過程,下列說法正確的是( )A.制備Na2CrO4的反應中,氧化劑與還原劑的物質的量之比為4:7 B.過濾需要用到的玻璃儀器有:漏斗、燒杯 C.“一系列操作”是指蒸發結晶、過濾、洗滌、干燥 D.“酸化”步驟可用硫酸酸化,發生的離子反應為:2CrO42-+2H+?Cr2O72-+H2O 組卷:26引用:1難度:0.4 -
5.對下列粒子組在溶液中能否大量共存的判斷和分析均正確的是( )
選項 粒子組 判斷和分析 A S2-、SO32-、K+、OH- 能大量共存,粒子間不反應 B H+、Ba2+、H2O2、I- 能大量共存,粒子間不反應 C Al3+、AlO2-、Na+、HCO3- 不能大量共存,因只發生反應:Al3++3AlO2-+6H2O═4Al(OH)3↓ D CO2、  、Na+、K+
、Na+、K+不能大量共存,因發生反應:CO2+2  +H2O→CO32-+2
+H2O→CO32-+2
A.A B.B C.C D.D 組卷:38引用:1難度:0.6 -
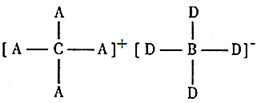 6.A、B、C、D、E是原子序數依次增大的五種常見的短周期主族元素,其中A、B、C、D四種元素的原子序數之和為E元素原子序數的2倍。E是短周期中原子半徑最大的元素。A、B、C、D四種元素形成的化合物[CA4]+[BD4]-有多種用途,可用來合成納米管,還可作殺蟲劑、催化劑、助熔劑、阻燃劑等,其結構如圖所示。下列說法正確的是( )
6.A、B、C、D、E是原子序數依次增大的五種常見的短周期主族元素,其中A、B、C、D四種元素的原子序數之和為E元素原子序數的2倍。E是短周期中原子半徑最大的元素。A、B、C、D四種元素形成的化合物[CA4]+[BD4]-有多種用途,可用來合成納米管,還可作殺蟲劑、催化劑、助熔劑、阻燃劑等,其結構如圖所示。下列說法正確的是( )A.元素A、C能形成含有非極性鍵的18電子化合物 B.最簡單氫化物的穩定性:C>D C.元素A、E形成的化合物不能與水發生氧化還原反應 D.化合物[CA4]+[BD4]-中各原子均滿足8電子穩定結構 組卷:96引用:10難度:0.5
(二)選考題:共15分。請考生從給出的兩道題中任選一題作答。如果多做,則按所做的第一題計分。[選修3:物質結構與性質]
-
18.氮化鎵(GaN)、碳化硅(SiC)材料是最成熟的第三代半導體的代表,GaN通常以GaCl3為鎵源,NH3為氮源制備,具有出色的抗擊穿能力,能耐受更高的電子密度。

(1)請寫出基態Ga原子的核外電子排布式。Ga、N和O的第一電離能由小到大的順序為。
(2)GaCl3熔點為77.9℃,氣體在270℃左右以二聚物存在,GaF3熔點1000℃,GaCl3的熔點低于GaF3的原因為。
(3)GaCl3?xNH3(x=3,4,5,6)是一系列化合物,向含1molGaCl3?xNH3的溶液中加入足量AgNO3溶液,有難溶于硝酸的白色沉淀生成;過濾后,充分加熱濾液,有4mol氨氣逸出,且又有上述沉淀生成,兩次沉淀的物質的量之比為1:2。
①NH3的VSEPR模型名稱為。
②GaCl3?xNH3含有的化學鍵類型有(填標號)。
A.極性共價鍵
B.離子鍵
C.配位鍵
D.金屬鍵
E.氫鍵
③能準確表示GaCl3?xNH3結構的化學式為。
(4)與鎵同主族的B具有缺電子性,硼砂(四硼酸鈉Na2B4O7?10H2O)中B4O72-是由兩個H3BO3和兩個[B(OH)4]-縮合而成的雙六元環,應寫成[B4O5(OH)4]2-的形式,結構如圖1所示,則該離子存在的作用力含有(填標號),B原子的雜化方式為。
A.離子鍵
B.極性鍵
C.氫鍵
D.范德華力
E.配位鍵
(5)GaN也可采用MOCVD(金屬有機物化學氣相淀積)技術制得:以合成的Ga(CH3)3為原料,使其與NH3發生系列反應得到GaN和另一種產物,該過程的化學方程式為。
(6)氮化鎵的晶胞如圖2所示,Ga原子與N原子半徑分別為apm和bpm,阿伏加德羅常數的值為NA,晶胞密度為cg/cm3,則該晶胞的空間利用率為(已知空間利用率為晶胞內原子體積占晶胞體積的百分比)。組卷:54引用:1難度:0.4
[選修5:有機化學基礎]
-
19.化合物G俗稱依普黃酮,是一種抗骨質疏松藥物的主要成分。以甲苯為原料合成該化合物的路線如圖所示。

已知:①G的結構簡式為
②ROOH+ 一定條件
一定條件 +H2O
+H2O
(1)反應①的反應條件為,反應F→G的反應類型為。
(2)化合物H用習慣命名法命名為。
(3)E與足量的H2完全加成后所生成的化合物中手性碳原子(連接四個不同原子或基團)的個數為。
(4)已知N為催化劑,則E+HC(OC2H5)3→F的化學方程式為。
(5)K是D的同系物,其相對分子質量比D多14,滿足下列條件的K的同分異構體共有種。
①苯環上只有兩個側鏈;
②能與Na反應生成H2;
③能與銀氨溶液發生銀鏡反應。
(6)根據上述信息,設計以苯酚和 為原料,制備
為原料,制備 的合成路線 (無機試劑任選)。組卷:158引用:5難度:0.5
的合成路線 (無機試劑任選)。組卷:158引用:5難度:0.5


