2013-2014學年廣東省高一(上)化學寒假作業(十)
發布:2024/4/20 14:35:0
一、選擇題(本題包括20小題,共40分)
-
1.下列說法正確的是( )
A.摩爾既是表示微粒,又是表示質量的單位 B.反應前各物質的“物質的量”之和與反應后各物質的“物質的量”之和一定相等 C.氫氧化鈉的摩爾質量是40g D.氬氣的摩爾質量(以g/mol為單位)在數值上等于它的相對原子質量 組卷:332引用:9難度:0.9 -
2.現有三組溶液:①汽油和氯化鈉溶液 ②39%的乙醇溶液 ③氯化鈉和單質溴的水溶液,分離以上各混合液的正確方法依次是( )
A.分液、蒸餾、萃取 B.萃取、蒸發、分液 C.分液、萃取、蒸餾 D.蒸餾、萃取、分液 組卷:181引用:359難度:0.9 -
3.為了除去粗鹽中的Ca2+、Mg2+、SO42-和泥沙,可將粗鹽溶于水,然后進行下列五項操作:①過濾 ②加過量的NaOH溶液 ③加適量鹽酸 ④加過量Na2CO3溶液 ⑤加過量BaCl2溶液,正確的操作順序是( )
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.④⑤②①③ 組卷:404引用:233難度:0.7 -
4.能用離子方程式H++OH-═H2O表示的反應是( )
A.稀醋酸和稀氨水反應 B.稀硫酸和燒堿溶液反應 C.稀鹽酸和氫氧化銅反應 D.稀硫酸和氫氧化鋇溶液反應 組卷:45引用:8難度:0.9 -
5.分類法在化學學科的發展中起到了非常重要的作用,下列分類標準不合理的是( )
A.根據是否具有丁達爾效應,將分散系分為溶液、濁液和膠體 B.根據反應中是否有電子轉移,將化學反應分為氧化還原反應和非氧化還原反應 C.根據是否含氧元素,將物質分為氧化劑和還原劑 D.根據水溶液或熔融狀態是否能夠導電,將化合物分為電解質和非電解質 組卷:14引用:1難度:0.7 -
6.甲、乙、丙、丁四種易溶于水的物質,分別由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同陽離子和陰離子各一種組成,已知:
①將甲溶液分別與其他三種物質的溶液混合,均有白色沉淀生成;
②0.1mol/L乙溶液中c(H+)>0.1mol/L;
③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
下列結論不正確的是( )A.甲溶液含有Ba2+ B.乙溶液含有SO42- C.丙溶液含有Cl- D.丁溶液含有Mg2+ 組卷:550引用:85難度:0.9 -
7.在pH=1的無色溶液中,能大量共存的是( )
A.Al3+、Na+、NO3-、Cl- B.Cu2+、Na+、NO3-、Cl- C.Ba2+、K+、CO32-、MnO4- D.NH4+、H+、CH3COO-、OH- 組卷:3引用:2難度:0.9 -
8.下列按純凈物、混合物、電解質和非電解質順序排列的是( )
A.鹽酸、空氣、醋酸、干冰 B.冰醋酸、福爾馬林、硫酸鈉、乙醇 C.蛋白質、油脂、苛性鉀、石灰石 D.膽礬、漂白粉、氯化鉀、硫酸鋇 組卷:218引用:11難度:0.9
二、實驗題(本題包括3小題,共45分)
-
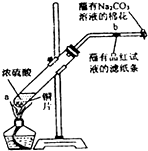 23.在一支試管中放入一塊很小的銅片,再加入少量濃硫酸,然后把試管固定在鐵架臺上.把一小條蘸有品紅溶液的濾紙放入帶有單孔橡皮塞的玻璃管中.塞緊試管口,在玻璃導管口處纏放一團蘸有Na2CO3溶液的棉花.給試管加熱,觀察現象.反應一段時間后,停止加熱.回答下列問題:
23.在一支試管中放入一塊很小的銅片,再加入少量濃硫酸,然后把試管固定在鐵架臺上.把一小條蘸有品紅溶液的濾紙放入帶有單孔橡皮塞的玻璃管中.塞緊試管口,在玻璃導管口處纏放一團蘸有Na2CO3溶液的棉花.給試管加熱,觀察現象.反應一段時間后,停止加熱.回答下列問題:
(1)寫出a處反應的化學方程式.
(2)試管中的液體反應一段時間后,b處濾紙條的變化為.待試管中反應停止后,給玻璃管放有蘸過品紅溶液的濾紙處微微加熱,濾紙條的變化為.
(3)待試管中的液體冷卻后,將試管上層液體倒去,再將剩余物質慢慢加入水中,可觀察溶液呈色.
(4)玻璃導管口處纏放一團蘸有Na2CO3溶液的棉花所起的作用是,反應的化學方程式為.
(5)若用濃度為18mol/L的濃硫酸100mL與過量的銅片,加熱使之反應,則被還原的硫酸(選填“大于”、“等于”或“小于”)0.9mol.組卷:23引用:4難度:0.1
三、計算題(本題共15分)
-
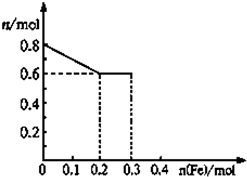 24.有三份不同質量的鐵粉樣品①②③,甲、乙、丙三位同學各取一份樣品分別與含有0.8molHNO3的稀硝酸反應,反應后硝酸和鐵均無剩余,且硝酸的還原產物只有NO.據此回答下列問題:
24.有三份不同質量的鐵粉樣品①②③,甲、乙、丙三位同學各取一份樣品分別與含有0.8molHNO3的稀硝酸反應,反應后硝酸和鐵均無剩余,且硝酸的還原產物只有NO.據此回答下列問題:
(1)甲取樣品①,反應后的溶液中鐵只以Fe3+離子的形式存在,則樣品①的質量為g.
(2)乙取樣品②,反應后的溶液中既含有Fe3+、又含有Fe2+離子,則樣品②的質量(設為ag)范圍是.
(3)丙取樣品③,將其慢慢加入到稀硝酸中,并不斷攪拌,反應過程中溶液里Fe3+、Fe2+、NO3-三種離子中的兩種離子的物質的量的變化曲線如圖所示,則該曲線表示的是物質的量變化的曲線,請你在此圖中再畫出另外種離子的物質的量的變化曲線.組卷:23引用:5難度:0.3


