2023年湖南省株洲市南方中學高考化學模擬試卷(六)
發布:2024/4/20 14:35:0
一、選擇題:本題共14小題,每小題3分,共42分。每小題只有一個選項符合題目要求。
-
1.化學與能源、材料和環境密切相關。下列有關說法錯誤的是( )
A.我國科學家研制的層狀磷酸鋯材料可除去廢水中的 Sr,9038Sr中含有的中子數為529038B.我國科學家利用赤泥和玉米秸稈制備的新型多孔生物炭具有強吸附性 C.杭州2022年第19屆亞運會“薪火“火炬使用了1070鋁合金,鋁合金屬于金屬材料 D.我國科學家制備了一種新型的催化劑InNi3Co0.5/Fe3O4,該催化劑中只含主族元素 組卷:46引用:5難度:0.6 -
2.設NA為阿伏加德羅常數的值。下列說法錯誤的是( )
A.0.2molCl2溶于水,轉移的電子數小于0.2NA B.3.1gP4(正四面體結構)所含共價鍵的數目為0.15NA C.1L1mol?L-1的NH4Cl溶液中NH4+和Cl-的數目均為1NA D.標準狀況下,2.24L的CO和N2混合氣體中含有的質子數為1.4NA 組卷:29引用:3難度:0.6 -
3.環氧樹脂膠粘劑廣泛應用于日常生活和工業生產等各種方面。制取環氧樹脂膠粘劑的反應如圖:
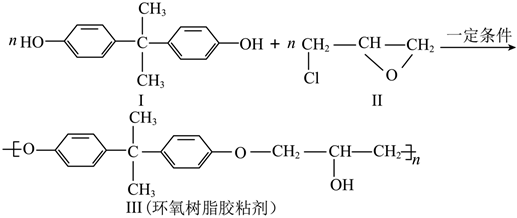
下列說法正確的是( )A.Ⅰ和Ⅱ均能與NaOH溶液反應 B.Ⅰ至少有9個原子處于同一直線上 C.該反應屬于加聚反應 D.Ⅰ、Ⅱ、Ⅲ均不含手性碳原子 組卷:36引用:3難度:0.7 -
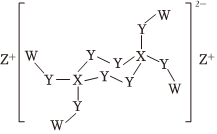 4.W、X、Y、Z是原子序數依次增大的短周期主族元素,原子序數總和為25,Y是地殼中含量最多的元素,由這四種元素形成的某化合物的結構如圖所示。下列敘述正確的是( )
4.W、X、Y、Z是原子序數依次增大的短周期主族元素,原子序數總和為25,Y是地殼中含量最多的元素,由這四種元素形成的某化合物的結構如圖所示。下列敘述正確的是( )A.原子半徑大小:Z>Y>X>W B.該化合物具有強氧化性,用于消毒殺菌 C.X可與Y形成XY、XY2等共價化合物 D.W分別與X、Y、Z形成的化合物所含化學鍵類型相同 組卷:124引用:11難度:0.7 -
5.用如圖實驗裝置進行有關實驗,能達到實驗目的的是( )
A B C D 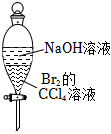
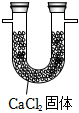
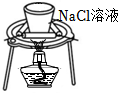
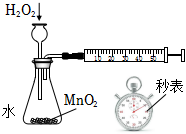
除去溶在CCl4中的Br2 干燥氨氣 將NaCl從溶液中結晶析出 測定化學反應速率 A.A B.B C.C D.D 組卷:19引用:2難度:0.8 -
6.某小組探究Na2S溶液與KMnO4溶液反應,實驗過程如下:
實驗過程Ⅰ:向5mL0.01mol?L-1酸性KMnO4溶液(pH=0)中滴加約0.3mL0.01mol?L-1Na2S溶液后,紫色變淺(pH<1),生成棕褐色沉淀(MnO2)。
實驗過程Ⅱ:向5mL0.01mol?L-1Na2S溶液中滴加約0.3mL0.01mol?L-1酸性KMnO4溶液(pH=0)后,溶液呈淡黃色(pH≈8),生成淺粉色沉淀(MnS)。
已知:
①在強酸性條件下被還原為Mn2+,在近中性條件下被還原為MnO2。MnO-4
②單質硫可溶于硫化鈉溶液,溶液顯淡黃色。
下列說法錯誤的是( )A.實驗Ⅰ說明酸性條件下S2-能將 還原為MnO2MnO-4B.實驗Ⅰ中生成棕褐色沉淀的原因:2H2O+2 +3Mn2+=5MnO2+4H+MnO-4C.實驗Ⅱ得到淺粉色沉淀,由于S2-將新生成的MnO2還原為Mn2+并迅速與其結合 D.該實驗說明:物質變化除與自身性質有關,還與濃度、用量、溶液的酸堿性有關 組卷:31引用:1難度:0.6
二、非選擇題(本題共4小題,共58分。)
-
17.氮及其化合物的利用是科學家們一直在探究的問題,它們在工農業生產和生命活動中起著重要的作用。
(1)已知:2C(s)+O2(g)═2CO(g) ΔH=-221kJ?mol-1
C(s)+O2(g)═CO2(g) ΔH=-393.5kJ?mol-1
N2(g)+O2(g)═2NO(g) ΔH=+181kJ?mol-1
若某反應的平衡常數表達式為K=,請寫出此反應的熱化學方程式:c(N2)?c2(CO2)c2(CO)?c2(NO)。
(2)汽車尾氣中的NO和CO在一定條件下可發生反應生成無毒的N2和CO2。將NO和CO以一定的流速通過兩種不同的催化劑(cat1、cat2)進行反應,相同時間內測得的脫氮率(脫氮率即NO的轉化率)如圖1所示。M點(填“是”或“不是”)對應溫度下的平衡脫氮率,理由是。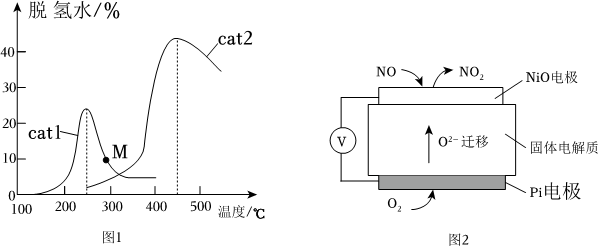
(3)通過NOx傳感器可監測NOx的含量,其工作原理如圖2。
①Pt電極上發生的是反應(填“氧化”或“還原”)。
②寫出NiO電極上的電極反應式:。
(4)某溫度下,在一密閉容器中充入一定量NO(g)發生反應4NO(g)?N2(g)+2NO2(g) ΔH<0,其正反應速率表達式為v正=k正?cn(NO)(k正為速率常數,只與溫度有關),測得反應速率和NO濃度的數據如表所示。
則k正=序號 c(NO)/(mol?L-1) v正/(mol?L-1?s-1) ① 0.10 4.00×10-9 ② 0.20 6.40×10-8 ③ 0.30 3.24×10-7 mol-3?L3?s-1;下列對于該反應的說法正確的是(填標號)。
A.當混合氣體顏色保持不變時,反應達到化學平衡狀態
B.當的比值保持不變時,反應達到化學平衡狀態n(N2)n(NO2)
C.反應達到化學平衡狀態時,每消耗0.1molNO就會消耗0.05molNO2
D.反應達到平衡狀態后,若降低溫度,則混合氣體的顏色變淺
E.反應達到平衡狀態后,若減小壓強,則混合氣體的平均相對分子質量減小組卷:138引用:5難度:0.6 -
18.嗎氯貝胺臨床上為單胺氧化酶抑制劑類抗抑郁藥,由芳香烴A合成嗎氯貝胺的路線如圖所示:
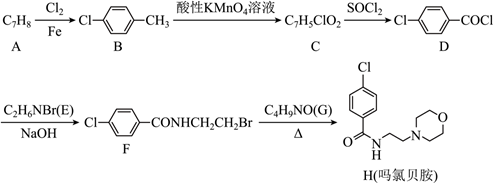
回答下列問題:
(1)A的化學名稱為,F中含氧官能團的名稱為。
(2)C的結構簡式為,由D生成F的反應類型為。
(3)F+G→嗎氯貝胺的化學方程式為。
(4)化合物C的同分異構體中滿足下列條件的有種(不考慮立體異構):
①屬于芳香族化合物;
②能發生銀鏡反應。(不考慮Cl-O)
其中核磁共振氫譜有三組峰且峰面積比為2:2:1的結構前式為。
(5)設計由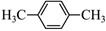 和CH3NH2制備
和CH3NH2制備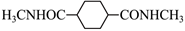 的合成路線 。(無機試劑任選)組卷:33引用:3難度:0.6
的合成路線 。(無機試劑任選)組卷:33引用:3難度:0.6


