2021-2022學年上海市楊浦區高三(上)期末化學試卷(一模)
發布:2024/4/20 14:35:0
一、選擇題(本題共40分,每小題2分,每小題只有一個正確答案)
-
1.應對“新冠疫情”的常見措施如圖所示,其基本原理與“過濾”類似的是( )
A. 
B. 
C. 
D.  組卷:37引用:3難度:0.9
組卷:37引用:3難度:0.9 -
2.單質不可能形成( )
A.離子晶體 B.原子晶體 C.分子晶體 D.金屬晶體 組卷:96引用:3難度:0.8 -
3.下列鋁的反應中,對氧化劑的判斷錯誤的是(括號中是氧化劑)( )
A.鋁熱反應(金屬氧化物) B.Al在濃硫酸中鈍化(濃硫酸) C.Al溶于NaOH溶液(NaOH) D.Al在空氣中生成氧化膜(O2) 組卷:68引用:1難度:0.8 -
4.與物質溶解度有關的分離方法是( )
A.萃取 B.升華 C.蒸餾 D.蒸發 組卷:16引用:2難度:0.6 -
5.下列能量屬于反應熱的是( )
A.1molHCl分解成H、Cl時吸收的能量 B.石墨轉化成金剛石時吸收的能量 C.Na變成Na+時吸收的能量 D.冰變成水時吸收的能量 組卷:51引用:2難度:0.5 -
6.只用水不能鑒別( )
A.苯和CCl4 B.KMnO4晶體和I2晶體 C.Na2O2和硫粉 D.乙酸乙酯和乙酸丁酯 組卷:79引用:2難度:0.5 -
 7.科研人員制出了由18個碳原子構成的環碳分子(如圖示).對該物質的說法正確的是( )
7.科研人員制出了由18個碳原子構成的環碳分子(如圖示).對該物質的說法正確的是( )A.與C60互為同素異形體 B.硬度大、熔點高 C.與乙炔互為同系物 D.是一種共價化合物 組卷:52引用:2難度:0.8 -
8.下列離子常用“氣體法”檢驗的是( )
A.SO42- B.NH4+ C.I- D.Fe2+ 組卷:41引用:3難度:0.5
二、綜合題(共60分)
-
23.喹啉類有機物X可用于制取醫藥、燃料、殺蟲劑等,它的一種合成路線如圖:
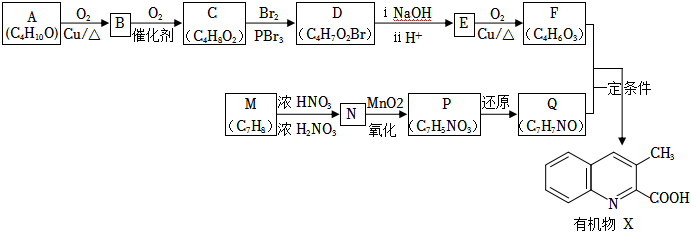
已知:①RNH2+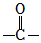 +H2O一定條件
+H2O一定條件
②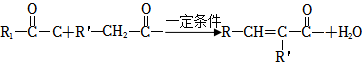
完成下列填空:
(1)A無支鏈,A官能團的名稱是;A生成B的化學方程式為:.
(2)M→N的反應類型:反應.
(3)W是C的同分異構體,寫出兩種屬于不同類有機物的W的結構簡式..
(4)1molD與NaOH溶液反應時,最多消耗molNaOH.
(5)P能發生銀鏡反應,寫出P的結構簡式.
(6)利用已學知識和本題中的信息,寫出以乙烯為原料合成A的路線(無機試劑任用).(合成路線的表示方法為:甲乙…反應試劑反應條件目標產物)反應試劑反應條件組卷:82引用:2難度:0.5 -
24.銅是不活潑的金屬,常見有+1、+2價.為探究銅及其化合物的性質,完成了兩組實驗,部分記錄如下:
第一組:
完成下列填空:序號 試劑 實驗步驟 實驗現象 ① 試管1中加2mL0.05mol?L-1Fe2(SO4)3溶液 加入1mL0.1mol?L-1KSCN溶液 溶液變為紅色 ② 試管2中加2mL0.05mol?L-1Fe2(SO4)3溶液 ⅰ加入0.16g銅粉 黃色溶液變為淺藍色溶液 ⅱ取上層清液,加入1滴0.1mol?L-1KSCN溶液 液滴接觸上方變為紅色,下方有白色沉淀生成 ③ 試管3中加2mL0.1mol?L-1CuSO4溶液 加入1mL0.1mol?L-1KSCN溶液 溶液變成綠色
(1)寫出試管1中發生反應的離子方程式.
(2)試管2,預測步驟ⅱ后溶液不應呈紅色,依據是.
(3)經測定試管②中得到的白色沉淀是CuSCN.
對生成CuSCN有兩種猜測:
猜測①Cu2+和SCN-反應生成CuSCN,根據,推知這一猜測錯誤.
猜測②生成白色沉淀是因為:Cu++SCN-→CuSCN↓.再請結合步驟ⅱ溶液出現紅色的現象,解釋生成沉淀的可能原因.(用離子方程式表示)
第二組:水合肼(N2H4?H2O)和堿性銅氨([Cu(NH3)4]2+)溶液混合反應,生成銅.
(3)水合肼溶液顯弱堿性,其電離與NH3?H2O相似,寫出水合肼的電離方程式:.
(4)將下列化學方程式補充完整、配平,并標出電子轉移的數目和方向.N2H4?H2O+[Cu(NH3)4]2+OH-→N2↑+Cu+NH3+.
(5)水合肼可用于還原鍋爐水中溶解的O2,防止鍋爐被腐蝕.與Na2SO3相比,使用水合肼處理水中溶解O2的優點是(任寫一點).組卷:39引用:1難度:0.6


