2011-2012學年遼寧省大連市瓦房店高級中學高二(下)暑假化學作業(十)
發布:2024/4/20 14:35:0
一、第Ⅰ卷選擇題(本題包括18小題,每小題只有一個選項符合題意,每小題3分,共54分)
-
1.下列化學式能真實表示物質分子組成的是( )
A.NaOH B.SO3 C.CsCl D.SiO2 組卷:274引用:18難度:0.9 -
2.按電子排布,可把周期表里的元素劃分成5個區,以下元素屬于P區的是( )
A.Fe B.Mg C.P D.La 組卷:76引用:19難度:0.9 -
3.元素x的陰離子與元素y的陽離子具有相同的電子層結構,由此可知( )
A.x的原子半徑大于y的原子半徑 B.x的電負性小于y的電負性 C.x 的氧化性小于y的氧化性 D.x的第一電離能大于y 的第一電離能 組卷:29引用:11難度:0.9 -
4.長式周期表共有18個縱行,從左到右排為1-18列,即堿金屬為第一列,稀有氣體元素為第18列.按這種規定,下列說法正確的是( )
A.第16列中元素中沒有非金屬元素 B.只有第二列的元素原子最外層電子排布為ns2 C.第四周期第8列元素是鐵元素 D.第15列元素原子的最外層電子排布為ns2 np5 組卷:27引用:8難度:0.9 -
5.下列各項所述的數字不是6的是( )
A.在NaCl晶體中,與一個Na+最近的且距離相等的Cl-的個數 B.在金剛石晶體中,最小的環上的碳原子個數 C.在二氧化硅晶體中,最小的環上的原子個數 D.在石墨晶體的片層結構中,最小的環上的碳原子個數 組卷:116引用:30難度:0.7 -
6.下列物質的熔、沸點高低順序正確的是( )
A.金剛石>晶體硅>二氧化硅>碳化硅 B.CI4>CBr4>CCl4>CH4 C.MgO>H2O>N2>O2 D.金剛石>生鐵>純鐵>鈉 組卷:89引用:7難度:0.7 -
7.在以下的分子或離子中,空間結構的幾何形狀不是三角錐形的是( )
A.NF3 B.CH3- C.BF3 D.H3O+ 組卷:68引用:9難度:0.7
二、第Ⅱ卷非選擇題
-
 21.已知A、B、C、D、E、F為元素周期表中原子序數依次增大的前20號元素,A與B;C、D與E分別位于同一周期.A原子L層上有2對成對電子,B、C、D的核外電子排布相同的簡單離子可形成一種C3DB6型離子晶體X,CE、FA為電子數相同的離子晶體.
21.已知A、B、C、D、E、F為元素周期表中原子序數依次增大的前20號元素,A與B;C、D與E分別位于同一周期.A原子L層上有2對成對電子,B、C、D的核外電子排布相同的簡單離子可形成一種C3DB6型離子晶體X,CE、FA為電子數相同的離子晶體.
(1)寫出A元素的基態原子價電子排布式;F離子電子排布式.
(2)寫出X的化學式和化學名稱.
(3)寫出X涉及化工生產中的一個化學方程式.
(4)試解釋工業冶煉D不以DE3而是以D2A3為原料的原因:.
(5)CE、FA的晶格能分別為786KJ/mol l、3401KJ/mo,試分析導致兩者晶格能差異的主要原因是:.
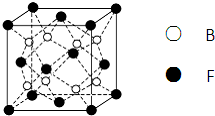
(6)F與B可形成離子化合物,其晶胞結構如圖所示:F與B形成離子化合物的化學式為;該離子化合物晶體的密度為a g/cm3,則晶胞的體積是(只要求列出算式).組卷:31引用:5難度:0.5 -
 22.決定物質性質的重要因素是物質結構.請回答下列問題.
22.決定物質性質的重要因素是物質結構.請回答下列問題.
(1)已知A和B為第三周期元素,其原子的第一至第四電離能如下表所示:
A通常顯電離能/kJ?mol-1 I1 I2 I3 I4 A 578 1817 2745 11578 B 738 1451 7733 10540 價,A的電負性B的電負性(填“>”、“<”或“=”).
(2)紫外光的光子所具有的能量約為399kJ?mol-1.根據下表有關蛋白質分子中重要化學鍵的信息,說明人體長時間照射紫外光后皮膚易受傷害的原因:.組成蛋白質的最簡單的氨基酸中的碳原子雜化類型是.
(3)實驗證明:KCl、MgO、CaO、TiN這4種晶體的結構與NaCl晶體結構相似(如圖1所示),已知3種離子晶體的晶格能數據如下表:共價鍵 C-C C-N C-S 鍵能/kJ?mol-1 347 305 259
則該4種離子晶體(不包括NaCl)熔點從高到低的順序是:離子晶體 NaCl KCl CaO 晶格能/kJ?mol-1 786 715 3401 .其中MgO晶體中一個Mg2+周圍和它最鄰近且等距離的Mg2+有個.
(4)金屬陽離子含未成對電子越多,則磁性越大,磁記錄性能越好.離子型氧化物V2O5和CrO2中,適合作錄音帶磁粉原料的是.
(5)某配合物的分子結構如圖2所示,其分子內不含有(填序號).
A.離子鍵 B.極性鍵 C.金屬鍵
D.配位鍵 E.氫鍵 F.非極性鍵.組卷:51引用:10難度:0.5


