2021-2022學年廣東省深圳市六校高三(上)第一次聯考化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共16小題,共44分,第1~10小題,每小題2分;第11-16小題,每小組4分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.“17世紀中國工藝百科全書”《天工開物》中記載“凡取煤經歷久者,從土面能辨有無之色,然后挖掘。深至五丈許,方始得煤。”下列說法錯誤的是( )
A.煤是不可再生能源 B.煤的組成以碳元素為主 C.煤的氣化、液化過程均為物理變化 D.煤通過干餾可以得到煤焦油、焦爐煤氣以及焦炭等 組卷:62引用:1難度:0.3 -
2.化學與生活息息相關。下列說法錯誤的是( )
A.NaCl可用作食品防腐劑 B.純堿可用于治療胃酸過多 C.甘油具有護膚保濕作用 D.地溝油可用于制肥皂 組卷:30引用:2難度:0.9 -
3.下列化學用語錯誤的是( )
A.S2-的結構示意圖為 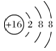
B.銨根的電子式為 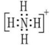
C.二氧化硅的化學式為 SiO2 D.次氯酸的結構式為 H-Cl-O 組卷:6引用:2難度:0.7 -
4.用下列裝置進行相應實驗,不能達到實驗目的的是( )
選項 A B C D 裝置 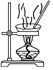
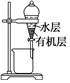
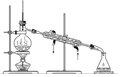
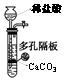
目的 蒸干NH4Cl溶液制備NH4Cl晶體 分離有機層和水層 分離苯和硝基苯 制備CO2 A.A B.B C.C D.D 組卷:7引用:2難度:0.5 -
5.設NA為阿伏加德羅常數的值,下列說法錯誤的是( )
A.常溫常壓下,7.0 g乙烯與丙烯的混合物中含有氫原子的數目為NA B.常溫下,100 mL pH=1的醋酸溶液中含有的氫離子數目為0.01NA C.用1L 1 mol?L-1 FeCl3溶液充分反應制備氫氧化鐵膠體,該體系中含氫氧化鐵膠體粒子數目為NA D.某密閉容器盛有0.1 mol N2和0.3 mol H2,在一定條件下充分反應,轉移電子的數目小于0.6NA 組卷:25引用:2難度:0.5 -
6.肉桂酸甲酯是一種常用的食用香料。工業上以苯乙烯為原料,可通過如下反應合成肉桂酸甲酯:

下列說法錯誤的是( )A.苯乙烯屬于芳香烴 B.苯乙烯和肉桂酸甲酯均能使酸性高錳酸鉀溶液褪色 C.肉桂酸甲酯所有原子可處于同一平面 D.肉桂酸甲酯可與NaOH溶液發生取代反應 組卷:10引用:3難度:0.6 -
7.下列實驗操作不能達到實驗目的是( )
選項 實驗目的 實驗操作 A 除去試管中附著的硫單質 加入適量氫氧化鈉溶液并加熱 B 配制銀氨溶液 將氨水逐滴滴入硝酸銀溶液至沉淀恰好溶解 C 比較HClO和CH3COOH的酸性強弱 常溫下,用pH計分別測定濃度均為0.1 mol?L-1的NaClO溶液和CH3COONa 溶液的pH D 檢驗加碘鹽中的碘元素 取適量加碘鹽溶解后,滴加數滴淀粉溶液 A.A B.B C.C D.D 組卷:6引用:1難度:0.5
選考題:共14分。請考生從2道題中任選一題作答。如果多做,則按所做的第一題計分。[選修3:物質結構與性質]
-
20.鐵(Fe)、鈷(Co)、鎳(Ni)是第四周期第Ⅷ族的元素,在化學上稱為鐵系元素,其化合物在生產生活中應用廣泛。
(1)基態Ni原子的核外電子排布式為。
(2)鐵系元素能與CO形成Fe(CO)5、Ni(CO)4等金屬羰基化合物。已知室溫時Fe(CO)5為淺黃色液體,沸點103℃,則Fe(CO)5中含有的化學鍵類型包括。
A.極性共價鍵
B.離子鍵
C.配位鍵
D.金屬鍵
(3)以甲醇為溶劑,Co2+可與色胺酮分子配位結合形成對DNA具有切割作用的色胺酮鈷配合物(合成過程如下所示)。色胺酮分子中所含元素(H、C、N、O)第一電離能由大到小的順序為,色氨酮分子中N原子的雜化類型為。X射線衍射分析顯示色胺酮鈷配合物晶胞中還含有一個CH3OH分子,CH3OH是通過作用與色胺酮鈷配合物相結合。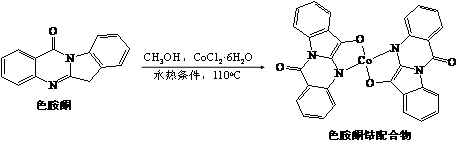
(4)LiFePO4常用作鋰離子電池的正極材料,其陰離子PO43-的空間構型為,與PO43-互為等電子體的微粒有(任寫一種)。
(5)Fe、Co、Ni與Ca都位于第四周期且最外層電子數相同,但相應單質的熔點,Fe、Co、Ni明顯高于Ca,其原因是。
(6)ZnS是一種使用廣泛的熒光材料。已知立方ZnS的晶胞結構如圖所示: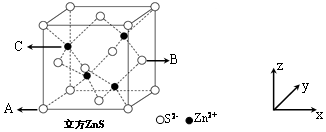
①已知A、B 點的原子坐標分別為(0,0,0)和(1,,12),則 C 點的原子坐標為12;
②立方ZnS的晶胞參數 a=541pm,則其晶體密度為g?cm-3。(列出計算表達式,設NA為阿伏加德羅常數的值)組卷:28引用:2難度:0.5
[化學——選修5:有機化學基礎]
-
21.化合物E是某藥物合成的中間體,其一種合成路線如圖所示:
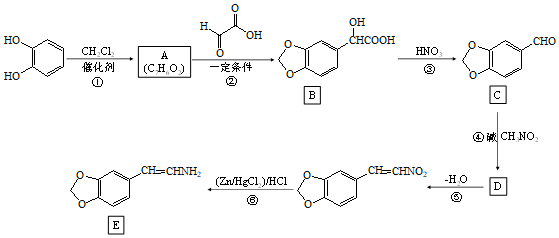
回答下列問題:
(1)化合物C中的含氧官能團名稱為。
(2)反應①的化學方程式為。
(3)②和⑥的反應類型分別為、。
(4)已知④的反應類型為加成反應,則D的結構簡式為。
(5)已知芳香族化合物M與E互為同分異構體,M滿足以下條件:
①苯環上有多個取代基,其中一個取代基為-NH2;
②能與溴水發生加成反應;
③能與NaHCO3反應;
則M的可能結構有種,其中核磁共振氫譜僅五組峰的結構簡式為(任寫一種)。
(6)根據上述信息,寫出氯化芐(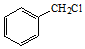 )及硝基芐(
)及硝基芐(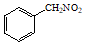 )為原料合成
)為原料合成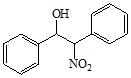 的路線(其他無機試劑任選) 。組卷:16引用:2難度:0.5
的路線(其他無機試劑任選) 。組卷:16引用:2難度:0.5


