2022年北京171中高考化學(xué)三模試卷
發(fā)布:2024/4/20 14:35:0
一、每小題只有一個(gè)選項(xiàng)符合題意。共14個(gè)小題,每小題3分,共42分
-
1.下列化學(xué)用語(yǔ)或圖示表示不正確的是( )
A.HCl的電子式是 
B.反-2-丁烯的結(jié)構(gòu)簡(jiǎn)式: 
C.SO3的VSEPR模型: 
D.As的原子結(jié)構(gòu)示意圖:  組卷:35引用:2難度:0.6
組卷:35引用:2難度:0.6 -
2.下列性質(zhì)的比較,不能用元素周期律解釋的是( )
A.酸性:H2SO3<HCl B.非金屬性:Cl>Br C.堿性:NaOH>Mg(OH)2 D.第一電離能:K<Ca 組卷:33引用:2難度:0.8 -
3.下列方程式與所給事實(shí)不相符的是( )
A.SO2通入氯水中,溶液褪色:SO2+Cl2+2H2O═2HCl+H2SO4 B.酚酞滴入NaHCO3溶液中變?yōu)闇\紅色:HCO3-?CO32-+H+ C.冷凝NO2氣體得到N2O4液體:2NO2(g)?N2O4(l)ΔH<0 D.制備Fe(OH)2時(shí),需除去溶液中的氧氣,防止發(fā)生:4Fe(OH)2+O2+2H2O═4Fe(OH)3 組卷:94引用:2難度:0.5 -
 4.離子液體具有較好的化學(xué)穩(wěn)定性、較低的熔點(diǎn)以及對(duì)多種物質(zhì)有良好的溶解性,因此被廣泛應(yīng)用于有機(jī)合成、分離提純以及電化學(xué)研究中。如圖為某一離子液體的結(jié)構(gòu)。下列選項(xiàng)不正確的是( )
4.離子液體具有較好的化學(xué)穩(wěn)定性、較低的熔點(diǎn)以及對(duì)多種物質(zhì)有良好的溶解性,因此被廣泛應(yīng)用于有機(jī)合成、分離提純以及電化學(xué)研究中。如圖為某一離子液體的結(jié)構(gòu)。下列選項(xiàng)不正確的是( )A.該離子液體能與水分子形成氫鍵 B.該結(jié)構(gòu)中不存在手性碳原子 C.該結(jié)構(gòu)中C原子的軌道雜化類型有3種 D.BF4-中存在配位鍵,B原子的軌道雜化類型為sp3 組卷:124引用:4難度:0.7 -
 5.一種對(duì)中樞神經(jīng)有抑制作用的藥物結(jié)構(gòu)如圖。其中W、X、Y、Z原子序數(shù)依次增大,X、Y、Z位于第二周期,Y的氣態(tài)氫化物的水溶性顯堿性。下列判斷不正確的是( )
5.一種對(duì)中樞神經(jīng)有抑制作用的藥物結(jié)構(gòu)如圖。其中W、X、Y、Z原子序數(shù)依次增大,X、Y、Z位于第二周期,Y的氣態(tài)氫化物的水溶性顯堿性。下列判斷不正確的是( )A.第一電離能:X<Z<Y B.XZ2晶體屬于共價(jià)晶體 C.W與Z可按原子個(gè)數(shù)比2:1和1:1形成兩種化合物 D.該藥物在堿性溶液中加熱,可水解產(chǎn)生Y的氣態(tài)氫化物 組卷:149引用:7難度:0.5 -
6.2021年我國(guó)科學(xué)家實(shí)現(xiàn)了二氧化碳到淀粉的人工合成。有關(guān)物質(zhì)的轉(zhuǎn)化過(guò)程示意如圖:

下列說(shuō)法不正確的是( )A.反應(yīng)①中分解H2O制備H2需從外界吸收能量 B.反應(yīng)②中CO2→CH3OH,碳原子的雜化方式發(fā)生了變化 C.核磁共振、X射線衍射等技術(shù)可檢測(cè)合成淀粉與天然淀粉的組成結(jié)構(gòu)是否一致 D.C6→淀粉的過(guò)程中只涉及O-H鍵的斷裂和形成 組卷:115引用:12難度:0.6
二、解答題(共5小題,滿分58分)
-
18.藥物Q能阻斷血栓形成,它的一種合成路線如圖所示。
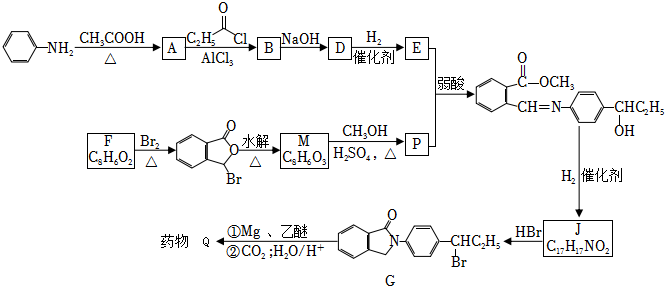
已知:i.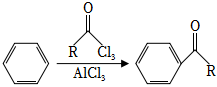
ii.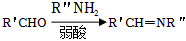
(1)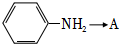 的反應(yīng)方程式是 。
的反應(yīng)方程式是 。
(2)B的分子式為C11H13NO2。E的結(jié)構(gòu)簡(jiǎn)式是。
(3)M→P的反應(yīng)類型是。
(4)M能發(fā)生銀鏡反應(yīng)。M分子中含有的官能團(tuán)是。
(5)J的結(jié)構(gòu)簡(jiǎn)式是。
(6)W是P的同分異構(gòu)體,寫(xiě)出一種符合下列條件的W的結(jié)構(gòu)簡(jiǎn)式:。
i.包含2個(gè)六元環(huán),不含甲基
ii.W可水解。W與NaOH溶液共熱時(shí),1molW最多消耗3molNaOH
(7)Q的結(jié)構(gòu)簡(jiǎn)式是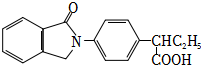 ,也可經(jīng)由P與Z合成。
,也可經(jīng)由P與Z合成。
已知:
合成Q的路線如圖(無(wú)機(jī)試劑任選),寫(xiě)出X、Y、Z的結(jié)構(gòu)簡(jiǎn)式:。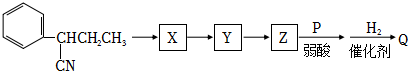 組卷:488引用:10難度:0.3
組卷:488引用:10難度:0.3 -
19.某小組探究CuSO4溶液、FeSO4溶液與堿的反應(yīng),探究物質(zhì)氧化性和還原性的變化規(guī)律。
將一定濃度CuSO4溶液,飽和FeSO4混合溶液加入適量氨水,產(chǎn)生紅褐色沉淀,經(jīng)檢驗(yàn),紅褐色沉淀含F(xiàn)e(OH)3。
(1)分析Fe(OH)3產(chǎn)生的原因:O2氧化所致。驗(yàn)證:向FeSO4溶液中滴入氨水,生成的白色沉淀迅速變?yōu)榛揖G色,一段時(shí)間后有紅褐色沉淀生成。
①生成白色沉淀的離子方程式是。
②產(chǎn)生紅褐色沉淀:4Fe(OH)2+O2+2H2O═4Fe(OH)3。電極反應(yīng)式:
還原反應(yīng):O2+2H2O+4e-═4OH-。
氧化反應(yīng):。
(2)提出問(wèn)題:產(chǎn)生Fe(OH)3的原因可能是Cu2+氧化所致。
驗(yàn)證如下(溶液A:飽和FeSO4溶液 +CuSO4溶液;已排除空氣的影響):
①Ⅰ中可能產(chǎn)生Cu,運(yùn)用氧化還原反應(yīng)規(guī)律分析產(chǎn)生Cu的合理性:序號(hào) 實(shí)驗(yàn) 試劑 現(xiàn)象 Ⅰ 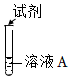
氨水 生成沉淀,一段時(shí)間后,產(chǎn)生紅褐色沉淀和灰黑色固體物質(zhì) Ⅱ 水 溶液無(wú)明顯變化 。
②檢驗(yàn):濾出Ⅰ中不溶物,用稀H2SO4溶解,未檢出Cu。分析原因:
ⅰ.Ⅰ中未生成Cu。
ⅱ.Ⅰ中生成了Cu。由于(用離子方程式表示),因此未檢出Cu。
(3)設(shè)計(jì)實(shí)驗(yàn)(Ⅲ)確認(rèn)CuSO4的作用(已排除空氣的影響),裝置示意圖如圖所示。
①補(bǔ)全電化學(xué)裝置示意圖。經(jīng)檢驗(yàn),實(shí)驗(yàn)中產(chǎn)生了Fe(OH)3、Cu。
②Ⅱ、Ⅲ中均含Cu2+。Ⅲ中產(chǎn)生了Cu,Ⅱ中未產(chǎn)生Cu,試解釋原因。
(4)CH3CHO分別與AgNO3溶液、銀氨溶液混合并加熱,CH3CHO與AgNO3溶液混合物明顯現(xiàn)象,但與銀氨溶液混合能產(chǎn)生銀鏡。試解釋原因:。組卷:117引用:6難度:0.6


