2023年四川省南充市閬中中學高考化學模擬試卷(4月份)
發布:2024/4/20 14:35:0
一、選擇題:本題共7小題,每小題6分。在每小題給出的四個選項中,只有一項是
-
1.近年來我國科技發展迅速,下列關于我國新科技的敘述正確的是( )
A.詩句“東風夜放花千樹”中蘊含的焰色試驗原理屬于物理變化 B.醫用酒精和“84消毒液”混合使用可以顯著提升對COVID-19病毒的殺滅能力 C.高鐵機車用于導電的受電弓板是碳系新材料,是利用石墨耐高溫、有潤滑感性能 D.我國C919大飛機所用的材料中,尾翼主盒(碳纖維)主要成分是傳統無機非金屬材料 組卷:26引用:1難度:0.8 -
2.Z是一種治療糖尿病藥物的中間體,可從下列反應制得:
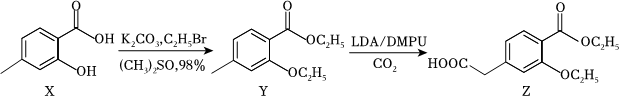
下列說法正確的是( )A.1molX能與2molNaHCO3反應 B.1molZ與足量NaOH溶液反應消耗2molNaOH C.X→Y→Z發生反應的類型都是取代反應 D.苯環上取代基與X相同的X的同分異構體有9種 組卷:77引用:3難度:0.6 -
3.下列過程中的化學反應,相應的離子方程式書寫正確的是( )
A.用足量氨水吸收SO2:NH3?H2O+SO2=NH4++HSO3- B.硫酸酸化的淀粉碘化鉀溶液久置后變藍:2I-+O2+4H+=I2+2H2O C.向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好為中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O D.向含氯化鐵的氯化鎂溶液中加入氧化鎂:2Fe3++3MgO+3H2O=2Fe(OH)3↓+3Mg2+ 組卷:36引用:3難度:0.6
三、非選擇題:本卷包括必考題和選考題兩總分。第22~32題為必考題,每個試題考生
-
10.甲醇是一種基礎有機化工原料,廣泛應用于有機合成、醫藥、農藥、染料、高分子等化工生產領域。利用二氧化碳合成甲醇,能有效降低二氧化碳排放量,為甲醇合成提供了一條綠色合成的新途徑。
相關化學鍵的鍵能數據
方法Ⅰ:二氧化碳催化加氫制甲醇化學鍵 C=O H-H C-H C-O H-O 鍵能E/(kJ?mol-1) 806 436 413 343 465
在一定溫度下,利用催化劑將CO2和H2合成CH3OH。已知各反應物、產物均為氣體。回答下列問題: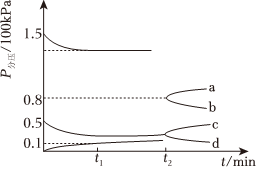
(1)寫出CO2和H2反應生成CH3OH和水的熱化學方程式:。
(2)某興趣小組對該反應進行了實驗探究。在一定溫度和催化劑條件下,將1molCO2和3molH2通入2L密閉容器中進行反應(此時容器內總壓強為200kPa),反應物和產物的分壓隨時間的變化曲線如圖所示。若保持容器體積不變,t1時反應達到平衡,測得H2的體積分數為。23
①此時用H2壓強表示0~t1時間內的反應速率v(H2)=kPa?min-1,若再向該容器中充入1molCO2和3molH2,平衡將(填正向,逆向或不)移動。
②t2時將容器體積迅速壓縮為原來的一半,圖中能正確表示壓縮體積后CO2分壓變化趨勢的曲線是(用圖中a、b、c、d表示),理由。
若其它條件不變,T1℃時測得平衡體系的壓強為plkPa;T2℃時,測得平衡體系的壓強為p2kPa,若p1>p2,則T1T2(填“>”、“<”或“無法確定)。
③在該溫度下,反應的標準平衡常數Kθ=。(已知:分壓=總壓×該組分物質的量分數,對于反應dD(g)+eE(g)=gG(g)+hH(g),Kθ=,其中pθ=100kPa,pG、pH、pD、pE為組分平衡分壓)(pGpθ)g?(pHpθ)h(pDpθ)d?(pEpθ)e
方法Ⅱ:CO2電解法制甲醇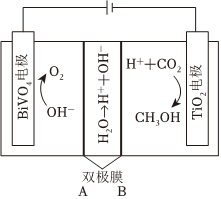
利用電解原理,可將CO2轉化為CH3OH,其裝置如圖所示。
(3)雙極膜B側為(填“陰離子”或“陽離子”)交換膜。組卷:18引用:1難度:0.4
[化學選修3:物質結構與性質]
-
 11.我國是率先掌握通過非線性光學晶體(KBBF)變頻來獲得深紫外激光技術的國家,KBF4是合成KBBR的主要原料,高溫下分解為KF和BF3。
11.我國是率先掌握通過非線性光學晶體(KBBF)變頻來獲得深紫外激光技術的國家,KBF4是合成KBBR的主要原料,高溫下分解為KF和BF3。
(1)灼燒鉀及其化合物時,會產生特殊的焰色。這是由于鉀元素的核外電子由(填“激發態”成“基態“)躍遷到另一個狀態時產生的光譜,該光譜屬于(填“發射”或“吸收”)光譜。
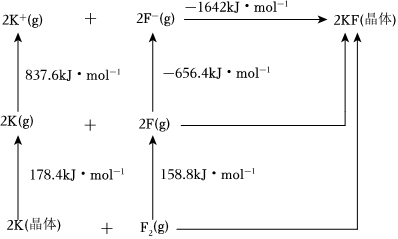
(2)離子晶體KF的晶格能(氣態離子形成1mol離子晶體釋放的能量)可通過Bom-Haber 循環計算得到(如圖)。
①KF的晶格能為kJ?mol-1。
②已知:氣態非金屬原子獲得1個電子形成氣態陰離子所釋放的能量叫該原子的第一親和能,則F原子的第一親和能為kJ?mol-1,試解釋同周期元素第一親和能F>O>C>N的原因:。
(3)BF3、NH3和PH3分子中鍵角由大到小的順序為。
(4)已知BF3中存在π鍵,則BF3中B-F鍵的鍵長(填“大于”、“小于”或“等于”)中B-F鍵的鍵長;BF-4的中心原子的軌道雜化類型是BF-4。
(5)KF晶體的晶胞與NaCl相似,若K+按ABCABC??????方式堆積,則F-占據的是K+圍成的空隙(填幾何空間構型),每個K+周圍緊鄰的K+個數為。設NA為阿伏加德羅常數的值,KF晶體的密度為ρg?cm-3,則K+與K+的最短距離為pm(用含ρ、NA的代數式表示)。組卷:20引用:2難度:0.6


