2020-2021學年黑龍江省雞西一中高一(上)第一次月考化學試卷
發布:2024/11/15 7:0:2
一、單選題
-
1.下列有關膠體的說法正確的是( )
A.稀豆漿、氯化鐵溶液均為膠體 B.膠體與溶液的本質區別是能否產生丁達爾現象 C.AgI膠體的分散質微粒在電場中定向移動 D.明礬溶于水形成的氫氧化鋁膠體可用于水的消毒、殺菌 組卷:4引用:1難度:0.7 -
2.下列物質分類正確的是( )
A.波爾多液、工業酒精、氨水均為混合物 B.根據酸分子中含有的氫原子個數,將酸分為一元酸、二元酸和多元酸 C.硫酸、純堿、小蘇打分別屬于酸、堿、鹽 D.MgO、Fe3O4、Na2O2均為堿性氧化物 組卷:12引用:2難度:0.8 -
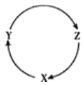 3.下列各選項中,不能滿足如圖一步關系選項是( )
3.下列各選項中,不能滿足如圖一步關系選項是( )A.X為銅、Y為氧化銅、Z為硫酸銅 B.X為二氧化碳、Y氧氣、Z為一氧化碳 C.X為碳酸鈣、Y氧化鈣、Z為氫氧化鈣 D.X為氫氧化鈉、Y氯化鈉、Z為碳酸鈉 組卷:55引用:6難度:0.8 -
4.進行化學實驗要注意實驗安全,正確的實驗操作是獲得正確的實驗結果和保障人身安全的前提。圖中的實驗操作正確的是( )
A. 
熄滅酒精燈B. 
稀釋濃硫酸C. 
鉀離子的檢驗D. 
稱量NaOH固體組卷:6引用:4難度:0.6 -
5.某無色溶液可能由Na2CO3、MgCl2、NaHCO3、BaCl2中的一種或幾種混合而成.該溶液加入NaOH溶液出現白色沉淀;加入稀H2SO4也出現白色沉淀,并放出氣體.據此分析,下述組合判斷正確的是:( )
①肯定有BaCl2 ②肯定有MgCl2 ③肯定有NaHCO3 ④肯定有NaHCO3或Na2CO3 ⑤肯定沒有MgCl2.A.①②③ B.①③ C.②④ D.①③⑤ 組卷:49引用:7難度:0.7 -
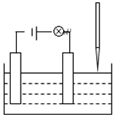 6.在電解質溶液的導電性實驗中(裝置如圖所示),若向某一電解質溶液中逐滴加入另一溶液時,則燈泡由亮變暗,至熄滅后又逐漸變亮的是( )
6.在電解質溶液的導電性實驗中(裝置如圖所示),若向某一電解質溶液中逐滴加入另一溶液時,則燈泡由亮變暗,至熄滅后又逐漸變亮的是( )A.硫酸溶液中逐滴加入氫氧化鈉溶液 B.硫酸銅溶液中逐滴加入氫氧化鋇溶液 C.鹽酸中逐滴加入硝酸銀溶液 D.鹽酸中逐滴加入碳酸鈉溶液 組卷:6引用:1難度:0.7 -
7.與離子方程式H++OH-=H2O相對應的化學方程式正確的是( )
A.Mg(OH)2+2HCl=MgCl2+2H2O B.Cu(OH)2+2HCl=CuCl2+2H2O C.Ba(OH)2+H2SO4=BaSO4↓+2H2O D.2NaOH+H2SO4=Na2SO4+2H2O 組卷:162引用:5難度:0.8 -
8.溶液中存在有五種離子,其中各離子個數比Cl-:
:Fe3+:K+:M=2:3:1:3:1,則M為( )SO2-4A. CO2-3B.Mg2+ C.Na+ D.Ba2+ 組卷:177引用:24難度:0.9 -
9.下列變化中,需要加入氧化劑才能實現的是( )
A.Cl-→Cl2 B.CuO→Cu C.CaCO3→CO2 D.H2O2→O2 組卷:917引用:13難度:0.5
二、填空題
-
28.目前,能較穩定存在的氯的氧化物有Cl2O、ClO2、Cl2O7等.有關數據見表:
請回答下列問題:化學式 Cl2O ClO2 Cl2O7 沸點/℃ 3.8 11.0 82.0
(1)常溫、常壓下,三種氧化物中屬于氣體的是.
(2)Cl2O7屬于酸性氧化物,它與水反應的離子方程式為.
(3)ClO2是一種常用的消毒劑,我國從2000年起逐步用ClO2代替氯氣對飲用水進行消毒.在消毒水時,ClO2還可將水中的Fe2+、Mn2+等轉化成Fe(OH)3和MnO2等難溶物除去,說明ClO2具有性.
(4)工業上可以用下列反應制備ClO2:2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,請用單線橋法
表示出該反應電子轉移的方向和數目.
(5)工業上制備ClO2的反應原理為:2NaClO3+4HCl(濃)=2ClO2↑+Cl2↑+2H2O+2NaCl.
①濃鹽酸在反應中顯示出來的性質是(填序號).
A.還原性 B.氧化性 C.酸性
②若上述反應中產生0.1molClO2,則轉移的電子數為.組卷:107引用:4難度:0.1 -
29.某純堿樣品中含有少量NaCl雜質,現用如圖所示裝置來測定純堿樣品中Na2CO3的質量分數(鐵架臺、鐵夾等在圖中均已略去;堿石灰是生石灰與氫氧化鈉的混合物,可以吸收水和二氧化碳)。
實驗步驟如下: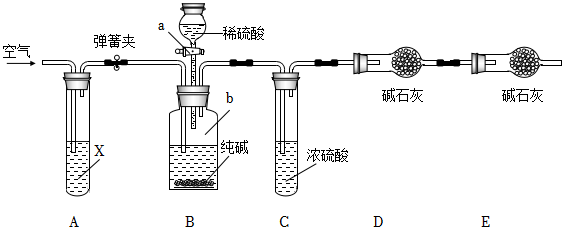
①按圖連接裝置,并檢查氣密性;
②準確稱得盛有堿石灰的干燥管D的質量為80.20g;
③準確稱得20.00g純堿樣品放入容器b中;
④打開分液漏斗a的旋塞,緩緩滴入稀硫酸,至不再產生氣泡為止;
⑤打開彈簧夾,往試管A中緩緩鼓入一定量空氣;
⑥然后稱得干燥管D的總質量為86.36g;
⑦重復步驟⑤和⑥的操作,直到干燥管D的質量不變,為86.80g。
試回答:
(1)裝置B中發生反應的離子方程式;
(2)裝置A中試劑X應選用足量的
A.飽和NaCl溶液 B.濃H2SO4 C.NaHCO3溶液 D.NaOH溶液
(3)①請用文字敘述裝置C的作用:。
②請用文字敘述裝置E的作用:。
(4)如果將分液漏斗中的硫酸換成濃度相同的鹽酸,則會導致測定結果(填“偏大”、“偏小”或“不變”,下同);若沒有操作⑤⑦,則會導致測定結果。
(5)根據實驗中測得的有關數據,計算出純堿樣品Na2CO3的質量分數為。組卷:27引用:3難度:0.6


