2015年全國第二十五屆天原杯復試化學試卷
發布:2024/11/29 5:30:2
一、選擇題(本題包括15個小題,每小題2分,共30分.每小題有1個或2個選項符合題意.若有2個答案的錯1個不得分,漏選1個扣1分.請將答案填在答題卡相應題號的空格內)
-
1.網絡神曲“化學是你,化學是我”揭示了化學與生活的密切關系.下列有關說法中正確的是( )
A.碳酸鈉俗名純堿,也叫蘇打,可用于清洗廚房用具的油污 B.84消毒液在日常生活中使用廣泛,溶液無色、有漂白作用,它的有效成分為Ca(ClO)2 C.青銅是我國使用最早的合金材料,目前世界上使用量最大的合金材料是鋁合金 D.明礬[KAl(SO4)2?12H2O]溶于水會形成膠體,因此可用于自來水的消毒殺菌 組卷:70引用:1難度:0.9 -
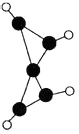 2.科學家最近在-100℃的低溫下合成一種化合物X,此分子的模型如圖,其中每個●代表一個碳原子,每個〇代表一個氫原子。下列說法中不正確的是( )
2.科學家最近在-100℃的低溫下合成一種化合物X,此分子的模型如圖,其中每個●代表一個碳原子,每個〇代表一個氫原子。下列說法中不正確的是( )A.該分子的分子式為C5H4 B.該分子中碳元素的質量分數是93.75% C.該分子中的氫原子與碳原子的個數比是4:5 D.等質量的該物質與甲烷相比,燃燒時消耗的氧氣更多 組卷:158引用:29難度:0.7 -
3.下列做法不會使人中毒的是( )
A.用工業酒精配制白酒飲用 B.將燃氣熱水器安裝在浴室內 C.向蔬菜大棚內通入適量的CO2 D.用膽礬對飲用水進行消毒 組卷:82引用:4難度:0.7 -
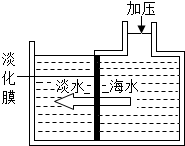 4.如圖,海水淡化可采用膜分離技術,對淡化膜右側的海水加壓,水分子可以透過淡化膜進入左側淡水池,而海水中的各離子不能通過淡化膜,從而得到淡水。對加壓后右側海水成分變化進行分析,正確的是( )
4.如圖,海水淡化可采用膜分離技術,對淡化膜右側的海水加壓,水分子可以透過淡化膜進入左側淡水池,而海水中的各離子不能通過淡化膜,從而得到淡水。對加壓后右側海水成分變化進行分析,正確的是( )A.溶質質量增加 B.溶劑質量減少 C.溶液質量不變 D.溶質質量分數減少 組卷:733引用:122難度:0.9 -
5.已知①鈉、鎂等活潑金屬能與乙醇反應,生成乙醇的金屬化合物和氫氣;②二氧化碳不支持燃燒是相對的,有些金屬如鎂能在二氧化碳中燃燒生成金屬氧化物和單質碳.則在下表各選項中,不能利用置換反應通過Y得到W的一組化合物是( )
A B C D Y CO2 Fe2O3 C2H5OH FeCl3 W MgO Al2O3 C2H5ONa CuCl2 A.A B.B C.C D.D 組卷:105引用:5難度:0.9 -
6.已知加熱蒸干MgCl2溶液可得到MgO固體.某同學通過系列實驗探究Mg及其化合物的性質,操作正確且能達到目的的是( )
A.將水加入濃硫酸中得到稀硫酸,置鎂條于其中探究Mg的活潑性 B.將NaOH溶液緩慢滴入MgSO4溶液中,觀察Mg(OH)2沉淀 C.將Mg(OH)2濁液直接倒入已裝好濾紙的漏斗中過濾,洗滌并收集沉淀 D.將Mg(OH)2沉淀轉入蒸發皿中,加足量稀鹽酸,加熱蒸干得無水MgCl2 組卷:85引用:3難度:0.9 -
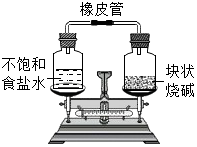 7.如圖所示,將密閉的相互連通的裝置放在天平上,調節天平使之平衡。經過一段時間后,下列有關敘述與事實相符合的是( )
7.如圖所示,將密閉的相互連通的裝置放在天平上,調節天平使之平衡。經過一段時間后,下列有關敘述與事實相符合的是( )A.指針偏左,食鹽溶液一定變稀,燒堿不潮解 B.指針偏右,食鹽溶液不一定飽和,燒堿潮解 C.指針偏左,食鹽溶液一定變濃,燒堿潮解 D.指針偏右,食鹽溶液一定變濃,燒堿潮解 組卷:170引用:3難度:0.7 -
8.CO2是造成溫室效應增強的主要氣體,在工業上可用CO2來制備甲醇等物質.“碳捕捉技術”是指通過一定的方法,將工業生產中產生的CO2分離出來并利用,能有效地減少CO2氣體的排放.如可利用NaOH溶液來“捕捉”CO2,其基本過程如圖所示(部分條件及物質未標出).下列有關該方法的敘述中正確的是 ( )
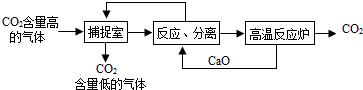
A.能耗大是該方法的一大缺點 B.整個過程中,只有一種物質可以循環利用 C.“反應分離”環節中,分離物質的基本操作是蒸發結晶 D.該方法可以減少碳排放,捕捉到的CO2還可以用來制備甲醇等產品 組卷:97引用:2難度:0.5 -
9.19世紀60年代,通過對當時發現的63種元素采用科學的分類方法,研制出世界上第一張元素周期表的科學家是( )
A.戴維 B.道爾頓 C.門捷列夫 D.阿伏加德羅 組卷:116引用:8難度:0.9 -
10.車用乙醇汽油是由乙醇與汽油按1:9的比例混合而成,下列有關推廣使用乙醇汽油的說法正確的是( )
A.可大大降低油料價格 B.有助于減輕大氣污染,改善大氣環境 C.乙醇是一種不可再生的能源 D.有助于促進糧食轉化,提高農民收入 組卷:159引用:3難度:0.9
四、計算題(本題包括2個小題,共10分)
-
30.工業上用CO和H2在170℃-200℃溫度下,用鈷做強化劑時,可以反應生成n=5~8的烷烴,這是人工合成汽油的方法之一。
(1)寫出用CnH2n+2表示的人工合成汽油的配平的化學方程式。
(2)如果向密閉的合成塔里通入恰好能完全反應的CO和H2,當完全反應后,合成塔內溫度不變,而塔內氣體壓強降低到原來的,試通過計算來說明這時有無汽油生成。25
(3)要達到上述合成汽油的要求,CO和H2的體積比的取值范圍是。組卷:105引用:2難度:0.5
四、附加題(10分,不計入總分)
-
31.煤和石油是重要的能源,也是生產化工產品的重要原料.如圖1是煤化工產業鏈的一部分.
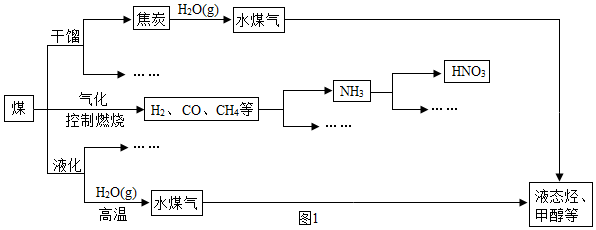
試用所學知識,解決下列問題:
(1)柴油是由石油加工得到的重要產品,它在燃燒時往往冒黑煙,可能的原因是.
(2)煤經過干餾可以得到焦爐氣、煤焦油和焦炭等.煤的干餾屬于(填“物理”或“化學”)變化.
(3)煤的直接液化是煤和適當溶劑混合在高溫和存在下與作用生成液態燃料的過程.
(4)煤和石油等化石燃料燃燒排放的大量二氧化碳會引起全球氣候變暖.一種新的處理方法是將二氧化碳氣體通入含有長石(地殼中最常見的礦石,含量高達60%)成分的水溶液里,其中一種反應的化學方程式:KAlSi3O8+CO2+2H2O=KHCO3+X↓+3SiO2↓,則X的化學式為.
(5)在煤燃燒前需對煤進行脫硫處理.煤的某種脫硫技術的原理如下所示:
FeS2Fe2++SO42-在微生物作用下h→O2/H2OFe3+在微生物作用下h→O2/H+
這種脫硫技術稱為微生物脫硫技術.該技術的第一步反應的化學方程式為,第二步反應的化學方程式為.
(6)工業上主要采用氨氧化法生產硝酸,如圖2是氨氧化率與氨-空氣混合氣中氧氨比的關系.其中直線表示反應的理論值;曲線表示生產實際情況.當氨氧化率達到100%,理論上γ{n(O2)/n(NH3)}=1.25,實際生產要將γ值維護在1.7-2.2之間,原因是.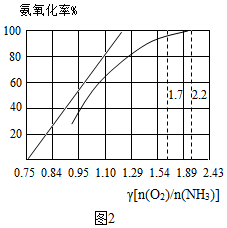
溫馨提示:n(O2)是可以認為是表示氧氣分子堆積數目的一種物理量.n(O2)數目越大,說明氧分子堆積數目越大.組卷:188引用:1難度:0.3


