2022-2023學年黑龍江省大慶鐵人中學高三(上)開學化學試卷
發布:2024/11/30 12:0:2
一、選擇題(本題包括20小題,1-10題每題2分,11-20題每題3分,共50分。每題只有一個選項符合題意)
-
1.化學與生活皆有著密切聯系。下列有關說法錯誤的是( )
A.用純堿和用清潔劑都能洗滌玻璃儀器表面油污,但去污原理不同 B.制作煙花的過程中常加入金屬發光劑和發色劑使煙花放出五彩繽紛的顏色 C.草莓棚中使用的“吊袋式二氧化碳氣肥”的主要成分可以是碳酸鈣 D.芒硝晶體(Na2SO4?10H2O)白天在陽光下曝曬后失水、溶解吸熱,晚上重新結晶放熱,實現了太陽能轉化為化學能繼而轉化為熱能 組卷:13引用:5難度:0.7 -
2.下列除去雜質(括號里為少量雜質)的實驗方法正確的是( )
A.CO2(CO):用酒精燈點燃 B.Fe2O3(Al2O3):加入氫氧化鈉溶液,過濾、洗滌 C.FeCl2(FeCl3):加入足量銅粉,過濾 D.K2CO3(NaHCO3):置于坩堝中加熱 組卷:4引用:3難度:0.5 -
3.設NA為阿伏加德羅常數的值,下列說法不正確的是( )
A.常溫下,1LpH=10的Na2CO3溶液中所含OH-的數目為10-10NA B.氯堿工業中轉移2mol電子時,通過陽離子交換膜的離子數目為2NA C.過量的銅與含0.2molHNO3的濃硝酸反應轉移電子的數目大于0.1NA D.室溫下向1LpH=1的醋酸溶液中加水稀釋,所得溶液中H+的數目大于0.1NA 組卷:8引用:1難度:0.5 -
4.下列常見實驗的現象或表述正確的是( )
A.向某溶液中加入2滴KSCN溶液,溶液不顯紅色,再向溶液中加入幾滴新制的氯水,溶液變為紅色,該溶液中一定含有Fe2+ B.為檢驗紅磚中鐵的價態,向紅磚粉末中加入鹽酸,充分反應后取上層清液于試管中,滴加KSCN溶液2~3滴,溶液變為紅色,說明紅磚中只有三氧化二鐵 C.制備氫氧化亞鐵時,向硫酸亞鐵溶液中滴加氫氧化鈉溶液,邊加邊攪拌,即可制得白色的氫氧化亞鐵 D.將(NH4)2Fe(SO4)2?6H2O試樣溶于稀硝酸中,滴加KSCN溶液,出現血紅色,說明檢驗前該試樣已變質 組卷:26引用:7難度:0.7 -
5.從牛至精油中提取的三種活性成分的結構簡式如圖所示,下列說法正確的是( )
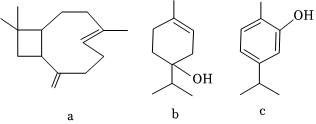
A.c分子中所有碳原子可能處于同一平面 B.a、b分子都存在屬于芳香族化合物的同分異構體 C.b中含有1個手性碳原子(手性碳原子指連有四個不同基團的碳原子) D.a、b、c均能發生加成反應、取代反應、加聚反應 組卷:13引用:1難度:0.7 -
6.有關下列實驗裝置的說法中正確的是( )
A. 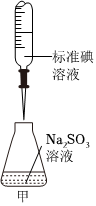
甲裝置:用于測定Na2SO3溶液的濃度B. 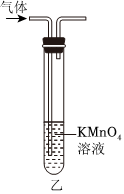
乙裝置:除去甲烷中的少量雜質乙烯C. 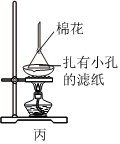
丙裝置:分離碘和氯化鈉混合物D. 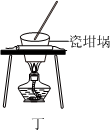
丁裝置:用于熔融NaOH固體組卷:5引用:1難度:0.5 -
7.下列離子方程式書寫正確的是( )
A.FeCl3溶液可以刻蝕電路板:2Fe3++Cu=2Fe2++Cu2+ B.Na可以將CuSO4溶液中的Cu置換出來:2Na+Cu2+=2Na++Cu C.AlCl3溶液中滴加過量氨水:Al3++4OH-=AlO2-+2H2O D.向FeBr2溶液中充入少量Cl2:2Br-+Cl2=Br2+2Cl- 組卷:50引用:3難度:0.5 -
8.由實驗操作和現象,可得出相應正確結論的是( )
實驗操作 現象 結論 A 向NaBr溶液中滴加過量氯水,再加入淀粉KI溶液 先變橙色,后變藍色 氧化性:Cl2>Br2>I2 B 用潔凈的鉑絲蘸取溶液進行焰色試驗 火焰呈黃色 原溶液中有Na+,無K+ C 取FeSO4少許溶于水,加入幾滴KSCN溶液 溶液變紅色 FeSO4全部被氧化 D 向無色溶液中滴加氯水和CCl4,振蕩,靜置 下層呈紫色 原溶液中有I- A.A B.B C.C D.D 組卷:9引用:1難度:0.5
二、非選擇題(本題包括4小題,共50分)
-
23.釩具有廣泛用途。黏土釩礦中,釩以+3、+4、+5價的化合物存在,還包括鉀、鎂的鋁硅酸鹽,以及SiO2、Fe3O4。采用以下工藝流程可由黏土釩礦制備NH4VO3。
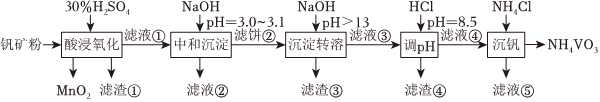
該工藝條件下,溶液中金屬離子開始沉淀和完全沉淀的pH如表所示。
回答下列問題:金屬離子 Fe3+ Fe2+ Al3+ Mn2+ 開始沉淀pH 1.9 7.0 3.0 8.1 完全沉淀pH 3.2 9.0 4.7 10.1
(1)“酸浸氧化”需要加熱,其原因是。
(2)“酸浸氧化”中,VO+和VO2+被氧化成,同時還有VO+2離子被氧化。寫出VO+轉化為反應的離子方程式VO+2。
(3)“中和沉淀”中,釩水解并沉淀為V2O5?xH2O,隨濾液②可除去金屬離子K+、Mg2+、Na+、,以及部分的。
(4)“沉淀轉溶”中,V2O5?xH2O轉化為釩酸鹽溶解。濾渣③的主要成分是。
(5)“調pH”中有沉淀生產,生成沉淀反應的化學方程式是。
(6)“沉釩”中析出NH4VO3晶體時,需要加入過量NH4Cl,其原因是。組卷:102引用:3難度:0.5 -
24.由芳香烴A與鹵代烴E為原料制備J和高聚物G的一種合成路線如圖:
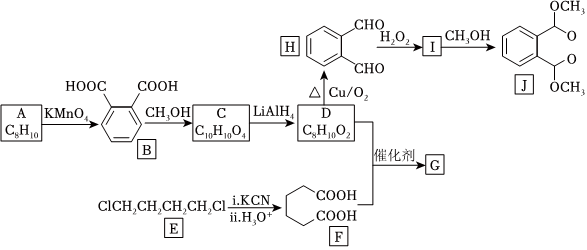
已知:①酯能被LiAlH4還原為醇;
②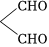 H2O2
H2O2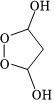
回答下列問題:
(1)A的化學名稱是,J的分子式為。
(2)D生成H的反應類型為反應,E在NaOH/乙醇溶液中完全反應生成的有機物結構簡式為。
(3)寫出F+D→G的化學方程式:。
(4)芳香化合物M是B的同分異構體,寫出符合下列要求的2種M的結構簡式:。
①1molM與足量銀氨溶液反應生成4molAg
②遇氯化鐵溶液顯色
③核磁共振氫譜顯示有3種不同化學環境的氫,峰面積之比1:1:1
(5)參照上述合成路線,分析在下列轉化中: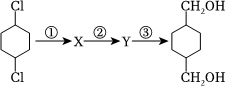 ,試劑①是 ,②是CH3CH2OH/濃H2SO4,③是。
,試劑①是 ,②是CH3CH2OH/濃H2SO4,③是。
(6)寫出用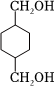 為原料經合適的反應制取化合物
為原料經合適的反應制取化合物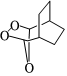 的合成路線(其他試劑任選) 。
的合成路線(其他試劑任選) 。
合成路線流程圖示例如圖: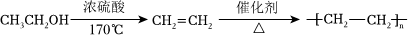 組卷:16引用:3難度:0.3
組卷:16引用:3難度:0.3


