2022年遼寧省沈陽五中高考化學模擬試卷(3月份)
發布:2024/4/20 14:35:0
一、選擇題:本題共15小題,每小題3分,共45分。在每小題給出的4個選項中,只有一項是符合題目要求的。
-
1.下列有關化學及人類社會發展歷程的說法中,正確的是( )
A.“所在山洋,冬月地上有霜,掃取以水淋汁后,乃煎煉而成”過程包括了溶解、蒸發、結晶等操作 B.“千淘萬漉雖辛苦,吹盡黃沙始到金”中,淘金原理與化學上的萃取一致 C.門捷列夫將元素按原子序數由小到大的順序依次排列,制出了第一張元素周期表 D.《茶疏》中對泡茶過程有如下記載:“治壺、投茶、出浴、淋壺、燙杯、釃茶、品茶”文中涉及過濾和蒸餾等化學實驗操作方法 組卷:35引用:3難度:0.8 -
2.下列表示不正確的是( )
A.NaHS的電子式: 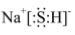
B.水分子的填充模型: 
C.CO2的結構式:O=C=O D.基態Br原子簡化電子排布式:[Ar]4s24p5 組卷:22引用:1難度:0.8 -
3.新材料的發展充分體現了“中國技術”“中國制造”和“中國力量”。下列成果所涉及的材料為金屬材料的是( )
A.“天問一號”火星探測器太陽翼的材料——石墨纖維復合聚酰胺薄膜 B.“長征五B”運載火箭中使用了耐熱性.導熱性好的材料——氮化鋁陶瓷 C.“領雁”AG50飛機主體結構的復合材料——玻璃纖維復合材料 D.“奮斗者”號深潛器載人艙的外殼——鈦合金 組卷:73引用:3難度:0.7 -
4.設NA表示阿伏加德羅常數的值,下列說法錯誤的是( )
A.常溫下,60gSiO2中含有Si-O極性鍵的數目為4NA B.常溫下,16.8g鐵粉與足量濃硝酸反應轉移電子數為0.9NA C.疊氮化銨(NH4N3)可發生爆炸反應:NH4N3=2N2↑+2H2↑,則每收集標準狀況下89.6L氣體轉移電子數為4NA D.1L0.1mol/L的Na2CO3溶液中H2CO3、HCO3-、CO32-的粒子總數為0.1NA 組卷:32引用:4難度:0.6 -
5.下列關于有機物的說法不正確的是( )
A.有機物(  )與氫氣 1:1加成后的產物只有一種
)與氫氣 1:1加成后的產物只有一種B.抗壞血酸分子(  )中有 2個手性碳原子
)中有 2個手性碳原子C.有機物的(  )一氯代物有4種
)一氯代物有4種D.2-丁烯(  ) 分子存在順反異構組卷:33引用:3難度:0.5
) 分子存在順反異構組卷:33引用:3難度:0.5 -
 6.某有機物A的結構簡式如圖所示,下列有關敘述正確的是( )
6.某有機物A的結構簡式如圖所示,下列有關敘述正確的是( )A.1molA最多可以與2molBr2發生反應 B.一個A分子中最多有8個碳原子在同一平面上 C.1molA與足量的NaOH溶液反應,最多可以消耗3molNaOH D.在一定條件下可以發生消去反應和取代反應 組卷:101引用:3難度:0.6
二、解答題(共4小題,滿分55分)
-
18.空氣污染治理是綜合工程,其中氮氧化合物的治理是環保的一項重要工作,合理應用和處理氮的化合物,在生產生活中有著重要的意義。

(1)已知:N2(g)+O2(g)═2NO(g)ΔH=+181.5kJ?mol-1。某科研小組嘗試利用固體表面催化工藝進行NO的分解。若用 、
、 、
、 和
和 分別表示N2、NO、O2和固體催化劑,在固體催化劑表面分解NO的過程如圖1所示。從吸附到解吸的過程中,能量狀態最低的是 (填字母)。
分別表示N2、NO、O2和固體催化劑,在固體催化劑表面分解NO的過程如圖1所示。從吸附到解吸的過程中,能量狀態最低的是 (填字母)。
(2)為減少汽車尾氣中NOx的排放,常采用CmHn(烴)催化還原NOx消除氮氧化物的污染。如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ?mol-1;
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160kJ?mol-1;
③CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g) ΔH3。
則ΔH3=。
(3)含氮化合物有很多種,其中亞硝酰氯(ClNO)是有機合成中常用的一種試劑。已知:2NO(g)+Cl2(g)?2ClNO(g)ΔH<0。
①一定溫度下,將2molNO(g)與2molCl2(g)置于2L恒容密閉容器中發生上述反應,若4min末反應達到平衡狀態,此時壓強是初始時的0.8倍,則0~4min內,平均反應速率υ(Cl2)=。下列現象可判斷反應達到平衡狀態的是(填選項字母)。
A.混合氣體的平均相對分子質量不變
B.混合氣體的密度保持不變
C.每消耗1molNO(g)同時生成1molClNO(g)
D.NO和Cl2的物質的量之比保持不變
②為加快反應速率,同時提高NO(g)的平衡轉化率,在保持其他條件不變時,可采取的措施有(填選項字母)。
A.升高溫度
B.縮小容器體積
C.使用合適的催化劑
D.再充入Cl2(g)
③一定條件下,在恒溫恒容的密閉容器中,按一定比例充入NO(g)和Cl2(g),平衡時ClNO(g)的體積分數隨的變化如圖2所示,當n(NO)n(Cl2)=2.5時,達到平衡狀態,ClNO(g)的體積分數可能是圖中的n(NO)n(Cl2)點(填“D”“E”或“F”)。
(4)已知:2NO(g)+O2(g)?2NO2(g)的反應歷程分兩步:
①2NO(g)?N2O2(g)(快)υ1正=k1正c2(NO),υ1逆=k1逆c(N2O2);
②N2O2(g)+O2(g)?2NO2(g)(慢),υ2正=k2正c(N2O2)?c(O2),υ2逆=k2逆c2(NO2)。
比較反應①的活化能與反應②的活化能E2,E2E1填“>”“<”或“=”);2NO(g)+O2(g)?2NO2(g)的平衡常數K與上述反應速率常數k1正、k1逆、k2正、k2逆的關系式為。組卷:51引用:2難度:0.6 -
19.近期,李蘭娟院士通過體外細胞實驗發現抗病毒藥物阿比多爾(H)能有效抑制冠狀病毒,同時能顯著抑制病毒對細胞的病變效應。合成阿比多爾的一條路線為:

已知: .回答下列問題:
.回答下列問題:
(1)阿比多爾分子中的含氧官能團為、,D的結構簡式為。
(2)反應②的化學方程式為;反應③的作用是;反應⑤的類型為。
(3)A的同分異構體中,能發生銀鏡反應且能與碳酸氫鈉溶液反應放出氣體的有種(不考慮立體異構)。
(4)以下為中間體D的另一條合成路線:
其中X、Y、Z的結構簡式分別為、、。組卷:26引用:2難度:0.6


