2021-2022學年湖北省荊州市沙市中學高一(上)期中化學試卷
發(fā)布:2024/4/20 14:35:0
一、單選題(本大題共15小題,每小題3分,共45分,每小題只有一個正確選項)
-
1.我國政府高度重視環(huán)境保護,明確提出并執(zhí)行了“碳達峰”、“碳中和”的時間表,下列有關(guān)敘述正確的是( )
A.二氧化碳是大氣中主要的污染物 B.燃料的燃燒和轉(zhuǎn)化不涉及氧化還原反應(yīng) C.為達到控碳目標,應(yīng)禁止使用一切含碳燃料 D.我國科學家在全球首創(chuàng)用二氧化碳完成淀粉[分子式為(C6H10O5)n]的全人工合成,以上過程一定涉及到氧化還原反應(yīng) 組卷:14引用:2難度:0.8 -
2.科學家發(fā)現(xiàn)了利用淚液來檢測糖尿病的方法,其原理是用氯金酸鈉(NaAuCl4)溶液與淚液中的葡萄糖發(fā)生反應(yīng),生成納米金單質(zhì)顆粒(直徑為20~60nm)。下列有關(guān)說法錯誤的是( )
A.氯金酸鈉中金元素的化合價為+3 B.檢測時,葡萄糖發(fā)生了還原反應(yīng) C.NaAuCl4在反應(yīng)中體現(xiàn)氧化性 D.納米金單質(zhì)顆粒分散在水中所得的分散系屬于膠體 組卷:21引用:6難度:0.7 -
3.分類方法在化學學科的發(fā)展中起到了非常重要的作用,下列5種分類標準中合理的有( )
①根據(jù)分散系是否具有丁達爾現(xiàn)象,將分散系分為溶液、膠體和濁液
②根據(jù)反應(yīng)中是否有電子的轉(zhuǎn)移,將化學反應(yīng)分為氧化還原反應(yīng)和非氧化還原反應(yīng)
③根據(jù)酸分子能電離出的氫離子個數(shù)將酸分為一元酸、二元酸等
④根據(jù)氧化物中是否含有金屬元素,將氧化物分為酸性氧化物和堿性氧化物
⑤根據(jù)物質(zhì)在水溶液里或熔融狀態(tài)下能否導(dǎo)電,將化合物分為電解質(zhì)和非電解質(zhì)A.5種 B.4種 C.3種 D.2種 組卷:216引用:16難度:0.7 -
4.鈉元素廣泛存在于自然界,中國科學技術(shù)大學的錢逸泰教授等以CCl4和金屬鈉為原料,在700℃時制造出納米級金剛石粉末。該成果發(fā)表在世界權(quán)威的《科學》雜志上,立刻被科學家們高度評價為“稻草變黃金”。下列關(guān)于含鈉元素物質(zhì)的說法錯誤的是( )
A.“稻草變黃金”的過程中元素種類沒有改變 B.NaCl與Na2CO3灼燒時火焰顏色相同 C.治療胃酸過多可以用NaHCO3,糕點生產(chǎn)也可以用NaHCO3 D.金屬鈉放置空氣中,最終會變成Na2O2 組卷:40引用:5難度:0.7 -
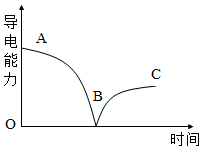 5.向一定體積的Ba(OH)2溶液中逐滴加入H2SO4溶液,測得混合溶液的導(dǎo)電能力隨時間的變化曲線如圖所示。下列說法正確的是( )
5.向一定體積的Ba(OH)2溶液中逐滴加入H2SO4溶液,測得混合溶液的導(dǎo)電能力隨時間的變化曲線如圖所示。下列說法正確的是( )A.AB段溶液的導(dǎo)電能力不斷減弱,說明產(chǎn)物BaSO4是非電解質(zhì) B.AB段反應(yīng)的離子方程式為Ba2++OH-+H++ ═BaSO4↓+H2OSO2-4C.BC段溶液的導(dǎo)電能力不斷增強,說明過量的Ba(OH)2發(fā)生電離 D.BC段溶液中:Fe3+、Na+、 和Cl-可以大量共存NH+4組卷:69引用:9難度:0.7 -
6.表中,對陳述Ⅰ、Ⅱ的正確性及兩者間是否具有因果關(guān)系的判斷都正確的是( )
選項 陳述Ⅰ 陳述Ⅱ 判斷 A 碳酸鈉溶液可用于治療胃病 Na2CO3可與鹽酸反應(yīng) Ⅰ對,Ⅱ?qū)Γ?/td> B 向Na2O2的水溶液中滴入酚酞變紅色 Na2O2與水反應(yīng)生成氫氧化鈉 Ⅰ對,Ⅱ錯,無 C 金屬鈉具有強還原性 高壓鈉燈發(fā)出透霧能力強的黃光 Ⅰ對,Ⅱ?qū)Γ?/td> D 過氧化鈉可為航天員供氧 Na2O2能與CO2和H2O反應(yīng)生成O2 Ⅰ對,Ⅱ?qū)Γ?/td> A.A B.B C.C D.D 組卷:241引用:18難度:0.7 -
7.油條的做法是將礬、堿、鹽按比例加入溫水中,再加入面粉攪拌成面團;放置,使面團產(chǎn)生氣體,形成孔洞.放置過程發(fā)生反應(yīng):2KAl(SO4)2?12H2O+3Na2CO3=2Al(OH)3↓+3Na2SO4+K2SO4+3CO2↑+21H2O.下列有關(guān)判斷正確的是( )
A.從物質(zhì)的分類角度來看,油條配方中的“礬、堿、鹽”均為鹽 B.放置過程發(fā)生的反應(yīng)為氧化還原反應(yīng) C.放置過程發(fā)生的反應(yīng)中,反應(yīng)物和生成物均為電解質(zhì) D.反應(yīng)的離子方程式為2Al3++3CO32-═2Al(OH)3↓+3CO2↑ 組卷:63引用:13難度:0.7
二、填空題(本大題共6小題,共55分)
-
20.我國制堿專家侯德榜先生潛心研究制堿技術(shù),發(fā)明了侯氏制堿法。工業(yè)上以侯氏制堿法為基礎(chǔ)生產(chǎn)焦亞硫酸鈉(Na2S2O5)的工藝流程如圖:
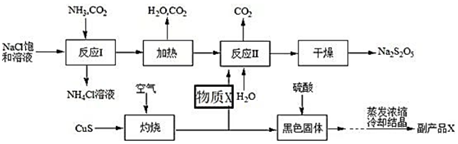
已知:反應(yīng)Ⅱ包含2NaHSO3?Na2S2O5+H2O等多步反應(yīng)。
(1)反應(yīng)Ⅰ的化學方程式為;在進行反應(yīng)Ⅰ時,向飽和NaCl溶液中先通入(填“CO2”或“NH3”)。
(2)圖中物質(zhì)X是SO2,“灼燒”時發(fā)生反應(yīng)的化學方程式為。
(3)已知Na2S2O5與稀硫酸反應(yīng)放SO2,其離子方程式為。
(4)副產(chǎn)品X化學式為;生產(chǎn)中可循環(huán)利用的物質(zhì)為(化學式)。組卷:74引用:3難度:0.6 -
21.過氧化鈉常用作漂白劑、殺菌劑、消毒劑,能與水和二氧化碳等物質(zhì)發(fā)生反應(yīng),保存不當時容易變質(zhì)。某實驗小組以過氧化鈉為研究對象進行了如圖實驗。

(1)探究一包Na2O2樣品是否已經(jīng)變質(zhì):取少量樣品,將其溶解,加入溶液,充分振蕩后有 白色沉淀,證明Na2O2已經(jīng)變質(zhì)。
(2)該實驗小組為了粗略測定過氧化鈉的質(zhì)量分數(shù),稱取了mg樣品,并設(shè)計如圖所示裝置來測定 過氧化鈉的質(zhì)量分數(shù)。
①裝置中儀器a的名稱是,裝置D的作用是。
②將儀器連接好以后,必須進行的第一步操作是。
③寫出裝置C中發(fā)生的主要反應(yīng)的化學方程式:。
④反應(yīng)結(jié)束后,在讀取實驗中生成氣體的體積時,你認為合理的是(填序號)。
a.讀取氣體體積前,需冷卻到室溫
b.調(diào)整量筒使E、F內(nèi)液面高度相同
c.視線與凹液面的最低點相平時讀取量筒中水的體積
⑤讀出量筒內(nèi)水的體積后,將其折算成氧氣的質(zhì)量為ng,則樣品中過氧化鈉的質(zhì)量分數(shù)為×100%。
⑥壓強不變時在一個密閉容器中放入足量過氧化鈉固體,然后充入等體積的CH4和O2,電火花引燃后充分反應(yīng),恢復(fù)至原溫度,余下氣體的體積為原體積的。組卷:34引用:3難度:0.5


