2021-2022學年遼寧省鐵嶺市調(diào)兵山市第二高級中學高二(上)期末化學試卷
發(fā)布:2024/12/18 17:0:2
一、單項選擇題,每題3分,滿分45分
-
1.古代詩詞中蘊含著許多科學知識,下列敘述正確的是( )
A.“冰,水為之,而寒于水”說明等質(zhì)量的水和冰相比,冰的能量更高 B.于謙《石灰吟》“千錘萬鑿出深山,烈火焚燒若等閑”,描述的石灰石煅燒是吸熱反應 C.曹植《七步詩》“煮豆燃豆萁,豆在釜中泣”,這里的變化只有化學能轉(zhuǎn)化為熱能 D.蘇軾《石炭?并引》“投泥潑水愈光明,爍玉流金見精悍”,所指高溫時碳與水蒸氣反應為放熱反應 組卷:191引用:11難度:0.8 -
2.乙烷燃燒熱為QkJ?mol-1,則下列熱化學方程式中正確的是( )
A.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=-2QkJ?mol-1 B.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=+2QkJ?mol-1 C.C2H6(g)+ O2(g)═2CO2(g)+3H2O(g)△H=-QkJ?mol-172D.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=-2QkJ?mol-1 組卷:20引用:2難度:0.8 -
3.化學知識和技術(shù)的發(fā)展離不開偉大的化學家。下列人物與其貢獻不匹配的是( )
A.侯德榜——工業(yè)制備燒堿 B.勒夏特列——化學平衡的移動 C.哈伯——利用氮氣和氫氣合成氨 D.蓋斯——反應熱的計算 組卷:12引用:2難度:0.8 -
4.某溫度下,恒容密閉容器中進行可逆反應:X(g)+Y(g)?2Z(g)+W(s)ΔH>0,下列說法正確的是( )
A.平衡后加入少量W,逆反應速率突然增大,正反應速率逐漸增大直到建立新的平衡狀態(tài) B.平衡后升高溫度,平衡正向移動,△H增大 C.平衡后加入Y,平衡正向移動,X、Y的轉(zhuǎn)化率均增大 D.容器中混合氣體的平均摩爾質(zhì)量不再變化時,反應達到平衡 組卷:11引用:1難度:0.6 -
5.下列反應在任何溫度下(所示狀態(tài))均不能自發(fā)進行的是( )
A.2H2O2(l)═O2(g)+2H2O(l)△H=-196kJ?mol-1 B.2Ag(s)+Cl2(g)═2AgCl(s)△H=-254kJ?mol-1 C.2N2(g)+O2(g)═2N2O(g)△H=+163kJ?mol-1 D.2HgO(s)═2Hg(l)+O2(g)△H=+182kJ?mol-1 組卷:185引用:3難度:0.7 -
6.在10L恒容密閉容器中通入1molN2和3molH2,一定條件下發(fā)生反應:N2(g)+3H2(g)?2NH3(g)。3min時測得生成1.8molNH3,則0~3min內(nèi)H2的平均反應速率為( )
A.0.03mol?L-1?min-1 B.0.06mol?L-1?min-1 C.0.09mol?L-1?min-1 D.0.27mol?L-1?min-1 組卷:17引用:4難度:0.7
二、非選擇題,滿分55分
-
18.如圖所示,某同學設計了一個燃料電池探究氯堿工業(yè)原理的相關問題,其中乙裝置中X為陽離子交換膜,請按要求回答相關問題:
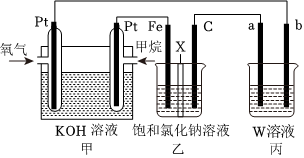
(1)石墨電極(C)作極,甲裝置中甲烷燃料電池的負極反應式為。
(2)若消耗2.24(標況)氧氣,則乙裝置中鐵電極上生成的氣體體積(標況)為L。
(3)若丙中以CuSO4 溶液為電解質(zhì)溶液進行粗銅(含Al、Zn、Ag、Pt、Au等雜質(zhì))的電解精煉,下列說法正確的是。
A.a(chǎn) 電極為純銅
B.粗銅接電源正極,發(fā)生還原反應
C.CuSO4溶液的濃度保持不變
D.利用陽極泥可回收Ag、Pt、Au等金屬
(4)若將乙裝置中兩電極用導線直接相連形成原電池,則石墨(C)電極上發(fā)生的電極反應為:。組卷:17引用:1難度:0.5 -
19.(14)以下是關于合成氨的有關問題,請回答:
(1)若在一容積為2L的密閉容器中加入0.2mol的N2和0.6mol的H2在一定條件下發(fā)生反應:N2(g)+3H2(g)?2NH3(g)ΔH<0,若在5分鐘時反應達到平衡,此時測得NH3的物質(zhì)的量為0.2mol。則平衡時c(N2)=。平衡時H2的轉(zhuǎn)化率為%。
(2)平衡后,若提高H2的轉(zhuǎn)化率,可以采取的措施有。
A.加了催化劑
B.增大容器體積
C.降低反應體系的溫度
D.加入一定量N2
(3)若在0.5L的密閉容器中,一定量的氮氣和氫氣進行如下反應:N2(g)+3H2(g)?2NH3(g)ΔH<0,其化學平衡常數(shù)K與溫度T的關系如表所示:
請完成下列問題:T/℃ 200 300 400 K K1 K2 0.5
①寫出化學平衡常數(shù)K的表達式。
②試比較K1、K2的大小,K1K2(填“>”、“<”或“=”);
③400℃時,反應2NH3(g)?N2(g)+3H2(g)的化學平衡常數(shù)為。當測得NH3、N2和H2物質(zhì)的量分別為3mol、2mol和2mol時,則該反應的v(N2)正v(N2)逆(填“>”、“<”
或“=”)。組卷:36引用:7難度:0.6


