2021-2022學年福建省莆田市荔城區中山中學九年級(下)第四次月考化學試卷
發布:2024/11/3 17:30:2
一、本卷共10小題,每小題3分,共30分。在每小題給出的四個選項中,只有一個選項符合題目要求。
-
1.下列化肥中,屬于復合肥料的是( )
A.KNO3 B.CO(NH2)2 C.Ca(H2PO4)2 D.(NH4)2SO4 組卷:30引用:5難度:0.9 -
2.對于下列化學用語,有關說法正確的是( )
①O2②KMnO4③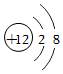 ④
④ ⑤
⑤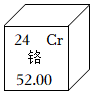
A.①表示兩個氧原子 B.②中錳元素的化合價為+7價 C.③④表示的元素位于同一周期 D.由⑤可知鉻的相對原子質量為52.00g 組卷:18引用:2難度:0.7 -
3.分類歸納的是學習化學知識的一種常用方法。下列分類正確的是( )
A.人體必需的微量元素:鐵、鈣 B.有機物:甲烷、乙醇、CC14 C.化合物:干冰、生石灰、石灰石 D.合金:生鐵、金剛石 組卷:16引用:1難度:0.9 -
4.下列實驗操作正確的是( )
A. 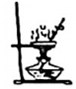
蒸發結晶B. 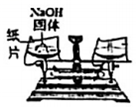
稱量氫氧化鈉固體C. 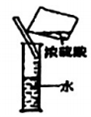
稀釋濃硫酸D. 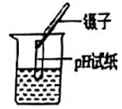
測定溶液pH組卷:7引用:1難度:0.7 -
5.持續防疫,化學助力。在抗擊新冠疫情過程中,常用戊二醛(化學式C5H8O2)對醫療器械等進行消毒。下列關于戊二醛的說法正確的是( )
A.戊二醛由5個碳原子、8個氫原子和2個氧原子構成 B.一個戊二醛分子中含有一個氧分子 C.氫元素的質量分數最大 D.戊二醛中碳、氧元素的質量比為15:8 組卷:29引用:4難度:0.5 -
6.下列知識整理的內容中,都正確的選項是( )
A.對現象的認識 B.對安全的認識 ①打開手電筒亮了,電池內化學能轉化為電能
②喝汽水打嗝,氣體溶解度隨溫度升高而增大①進入地窖前做燈火實驗
②煤爐上放盆水防止CO中毒C.對鑒別方法的認識 D.對生活的認識 ①鑒別硫酸銨和硫酸鉀一一取樣,加入熟石灰混合,聞氣味
②鑒別氯化鈉和硝酸銨一一加水①洗滌劑除油污一一溶解油污
②區分硬水和軟水一一用肥皂水A.A B.B C.C D.D 組卷:20引用:1難度:0.6
二、填空題(共8小題,每小題10分,滿分70分)
-
17.在對三星堆考古挖掘中出土了許多青銅面具,這些面具表面都有一層綠色的銅銹(主要成分是堿式碳酸銅),某學習小組對性質進行實驗探究。
Ⅰ、探究堿式碳酸銅的形成
經查閱資料,銅銹的主要成分是堿式碳酸銅【Cu2(OH)2CO3】,由此推測空氣中的肯定參加了反應,但不能確定空氣中的氧氣是否參與反應,為證明銅生銹是否需要氧氣,設計如圖實驗,你認為其中必須要做的對比實驗是(填序號)。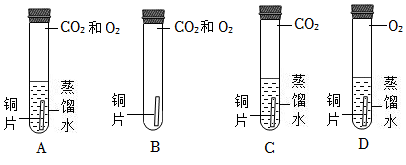
Ⅱ、探究堿式碳酸銅的組成
探究堿式碳酸銅中是否存在碳酸根離子的實驗方法(操作、現象及結論)。
Ⅲ、探究堿式碳酸銅受熱的變化
(1)小組設計了如圖裝置(夾持儀器已略去),并用于探究堿式碳酸銅的分解產物。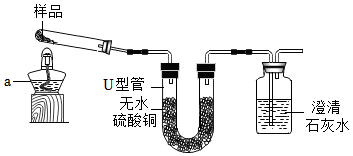
圖示加入樣品和試劑,加熱一段時間后,試管中固體變黑,U形管中無水硫酸銅變藍(無水硫酸銅為白色固體,遇水變藍),澄清石灰水變渾濁。已知黑色固體為CuO,寫出堿式碳酸銅受熱分解的化學方程式。
(2)小明在對堿式碳酸銅粉末加熱時發現,綠色固體先變成黑色,繼續高溫灼燒黑色固體變成紅色,同時有氣體產生,為弄清紅色固體的成分,進行了如下探究:
【查閱資料】Cu和Cu2O均為紅色固體,且Cu2O+H2SO4=Cu+CuSO4+H2O
【提出猜想】紅色固體是:I、CuⅡ、Cu2OⅢ、。
【進行實驗】
步驟①觀察到的實驗現象為操作 現象 結論 ①取灼燒后的紅色固體2.72g于試管中,加入足量稀硫酸加熱并充分振蕩,靜置 …… 猜想Ⅲ正確 ②過濾、洗滌、干燥 得紅色固體 ,根據上述實驗現象,小明認為猜想Ⅲ正確,但有同學認為小明的判斷不嚴謹,原因是,所以如要確定2.72g紅色固體成分,還需要補充的操作是,再通過計算得出結論。組卷:37引用:1難度:0.5 -
18.世界衛生組織規定飲用水中ClO2剩余量應小于0.2mg/L。取1L經ClO2消毒后的飲用水,與足量KI充分反應(原理為2ClO2+2KI═2KClO3+I2),測得生成I2的質量為0.508mg。通過計算判斷該飲用水中ClO2的含量是否符合世界衛生組織標準。
組卷:23引用:2難度:0.6


