2023年吉林省松原市前郭縣城鎮三校中考化學二模試卷
發布:2024/6/13 8:0:9
一、單項選擇題(每小題1分,共10分)
-
1.成語蘊含豐富的中華文化。下列成語的本義一定體現化學變化的是( )
A.盲人摸象 B.南轅北轍 C.火中取栗 D.繩鋸木斷 組卷:286引用:36難度:0.7 -
2.化學與生活息息相關。下列生活中常見的物質屬于純凈物的是( )
A.礦泉水 B.河水 C.蘇打水 D.蒸餾水 組卷:187引用:3難度:0.6 -
3.化學是一門以實驗為基礎的學科。下列實驗操作正確的是( )
A. 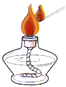
點燃酒精燈B. 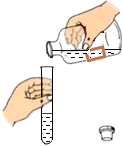
傾倒液體C. 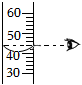
讀取液體的體積D. 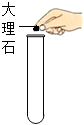
取用固體組卷:313引用:24難度:0.8 -
4.安全無小事,關系你我他。下列做法錯誤的是( )
A.發現有人煤氣中毒,立即移到通風處急救 B.點燃氫氣前,一定先要驗純 C.稀釋濃硫酸時,將濃硫酸沿器壁慢慢注入盛有水的燒杯中,并不斷攪拌 D.電器著火時,立即用大量水潑滅 組卷:2引用:2難度:0.7 -
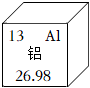 5.硬鋁常用于制造火箭、飛機的外殼,鋁元素的相關信息如圖所示,下列說法正確的是( )
5.硬鋁常用于制造火箭、飛機的外殼,鋁元素的相關信息如圖所示,下列說法正確的是( )A.鋁元素的相對原子質量為13 B.Al2O3中Al為+2價 C.硬鋁的強度和硬度比鋁的大 D.鋁是地殼中含量最多的元素 組卷:453引用:13難度:0.8 -
6.下列關于NaOH和Ca(OH)2的用途中錯誤的是( )
A.用Ca(OH)2制波爾多液 B.用Ca(OH)2改良酸性土壤 C.用NaOH溶液檢驗CO2 D.用NaOH固體干燥某些氣體 組卷:892引用:8難度:0.6
四、實驗與探究題(每空1分,化學方程式2分,共12分)
-
19.在學習了常見的酸和堿后,某化學興趣小組的同學圍繞“酸堿中和反應”,在老師引導下開展實驗探究活動,請你參與下列活動。
【實驗探究】將氫氧化鉀溶液與稀硫酸混合,觀察不到明顯現象,為證明氫氧化鉀溶液與稀硫酸發生了反應,三位同學進行了以下實驗。
(1)測定溶液pH變化
甲同學在實驗過程中測得溶液pH變化如圖1所示,則該同學是將(填字母序號)。
a.氫氧化鉀溶液滴入稀硫酸中
b.稀硫酸滴入氫氧化鉀溶液中
(2)測混合過程中的溫度變化
乙同學在實驗過程中測得混合溶液的溫度變化如圖2所示,說明稀硫酸與氫氧化鉀溶液發生的反應是放熱反應。圖2中B點表示的含義是。
(3)借助于酸堿指示劑
丙同學通過圖3所示實驗,他觀察到溶液由紅色變成無色,也證明氫氧化鉀溶液與稀硫酸發生了化學反應,反應的化學方程式為。
【提出問題】針對反應后溶液中溶質的成分,大家紛紛提出了猜想。
【猜想與假設】
猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有K2SO4和KOH。
【進行實驗】
(4)為了驗證猜想,學習小組選用Fe2O3粉末、BaCl2溶液,進行如下探究:
【實驗結論】通過探究,同學們一致確定猜想二是正確的。實驗方案 實驗操作 實驗現象 實驗結論 方案一 取少量反應后的溶液于試管中,加入Fe2O3粉末 溶液中有H2SO4,猜想二正確 方案二 取少量反應后的溶液于試管中,滴加BaCl2溶液 產生白色沉淀 溶液中有H2SO4,猜想二正確
【評價與反思】
(5)丁同學針對上述方案提出疑問,認為方案二是不合理的,理由是。
(6)同學們經過反思與討論,最后認為方案一中的Fe2O3粉末可以用下列的某些物質代替,也能得到同樣的實驗結論,請你選出可用藥品的字母序號。
A.Mg
B.CuO
C.KCl
D.Na2CO3組卷:10引用:2難度:0.5
五、計算題(共6分)
-
20.某煉鐵廠用含雜質20%的赤鐵礦(主要成分是氧化鐵)冶煉生鐵,求3500t這種礦石可煉出含鐵98%的生鐵的質量是多少?
組卷:587引用:7難度:0.5


