2020-2021學年江西省景德一中2班高一(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題只有一個正確答案,共48分)
-
1.用化學用語表示2Mg+CO2
2MgO+C中的相關微粒,其中不正確的是( )點燃A.中子數為12的鎂原子: Mg2412B.MgO的電子式: 
C.CO2的結構式:O═C═O D.碳原子的結構示意圖:  組卷:51引用:3難度:0.7
組卷:51引用:3難度:0.7 -
2.下列關于化學鍵的敘述正確的是( )
A.所有物質里都含有化學鍵 B.離子化合物中可能含有共價鍵 C.共價化合物中可能含有離子鍵 D.水分子中的化學鍵是非極性鍵 組卷:64引用:3難度:0.8 -
3.下列關于元素周期表和周期律的說法正確的是( )
A.現行元素周期表有七個周期,18個族 B.熔點:Li>K,沸點:I2>Br2 C.鹽酸的酸性比氫硫酸酸性強,可推測非金屬性:Cl>S D.At與I屬于同主族元素,可推測AgAt為難溶于水的白色固體 組卷:5引用:1難度:0.7 -
4.下列反應中生成物總能量高于反應物總能量的是( )
A.碳酸鈣受熱分解 B.鈉與水反應 C.鋁粉與氧化鐵粉末反應 D.氧化鈣溶于水 組卷:19引用:6難度:0.9 -
5.某小組為研究原電池原理,設計如圖裝置,下列敘述正確的是( )

A.若X為Fe,Y為Cu,鐵為正極 B.若X為Fe,Y為Cu,電子由銅片流向鐵片 C.若X為Fe,Y為C,碳棒上有紅色固體析出 D.若X為Cu,Y為Zn,鋅片發生還原反應 組卷:148引用:14難度:0.9 -
6.X,Y,Z均為短周期元素,X,Y處于同一周期,X,Z的最低價離子分別為X2-和Z-,Y+和Z-具有相同的電子層結構。下列說法正確的是( )
A.原子最外層電子數:X>Y>Z B.單質沸點:X>Y>Z C.離子半徑:X2->Y+>Z- D.原子序數:X>Y>Z 組卷:1866引用:68難度:0.7 -
7.高鐵電池是一種新型可充電電池,與普通高能電池相比,該電池能長時間保持穩定的放電電壓,高鐵電池的總反為:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH,下列敘述不正確的是( )放電充電A.放電時負極反應式為:Zn-2e-+2OH-=Zn(OH)2 B.放電時每轉移3mol電子,正極有1 mol K2FeO4被還原 C.充電時陰極附近溶液的堿性增強 D.放電時正極反應式為:Fe(OH)3-3e-+5OH-=FeO42-+4H2O 組卷:85引用:4難度:0.7
二、非選擇題(共52分)
-
21.氮的氧化物是大氣污染物之一,用活性炭或一氧化碳還原氮氧化物,可防止空氣污染。回答下列問題:
(1)汽車尾氣中常含有碳煙、CO、NO等有害物質,尾氣中含有碳煙的主要原因為。
(2)已知在298 K和101 kPa條件下,有如下反應:
反應①:C(s)+O2(g)═CO2(g)△H1=-393.5kJ?mol-1
反應②:N2(g)+O2(g)═2NO(g)△H2=+180.5kJ?mol-1
若反應CO2(g)+12N2(g)?12C(s)+NO(g)的活化能為a kJ?mol-1,則反應C(s)+2NO(g)?CO2(g)+N2(g)的活化能為12kJ?mol-1
(3)在常壓下,已知反應2CO(g)+2NO(g)?N2(g)+2CO2(g)△H(298 K)=-113.0 kJ?mol-1,△S(298K)=-145.3×10-3kJ/(mol?K),據此可判斷該反應在常溫下(填“能”或“不能”)自發進行。
(4)向容積為2L的真空密閉容器中加入活性炭(足量)和NO,發生反應C(s)+2NO(g)?N2 (g)+CO2(g),NO和N2的物質的量變化如下表所示,在T1℃、T2℃分別到達平衡時容器的總壓強分別為p1 kPa、p2 kPa。
①0~10min內,以NO表示的該反應速率v(NO)=物質的
量/molT1℃ T2℃ 0 5 min 10 min 15 min 20 min 25 min 30 min NO 2.0 1.16 0.80 0.80 0.50 0.40 0.40 N2 0 0.42 0.60 0.60 0.75 0.80 0.80 kPa?min-1。
②第15min后,溫度調整到T2,數據變化如上表所示,則p1p2(填“>”、“<”或“=”)。
③若30min時,保持T2不變,向該容器中再加入該四種反應混合物各2 mol,再次達平衡時NO的體積百分含量為。組卷:9引用:1難度:0.4 -
22.(1)乙基叔丁基醚(以ETBE表示)是一種性能優良的高辛烷值汽油調和劑。用乙醇與異丁烯(以IB表示)在催化劑HZSM-5催化下合成ETBE,反應的化學方程式為:C2H5OH(g)+IB(g)?ETBE(g)△H。回答下列問題:
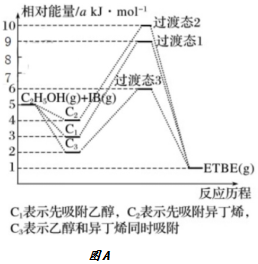
反應物被催化劑HZSM-5吸附的順序與反應歷程的關系如圖A所示,該反應的△H=kJ?mol-1。反應歷程的最優途徑是。(填C1、C2或C3)
(2)一定條件下,用Fe2O3、NiO或Cr2O3作催化劑對燃煤煙氣回收。反應為2CO(g)+SO2(g)2CO2(g)+S(l)△H=-270kJ?mol-1。催化劑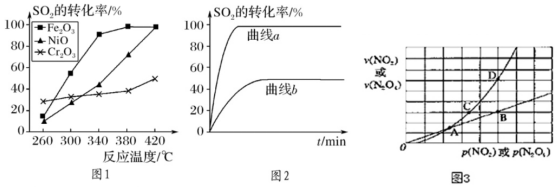
①其他條件相同、催化劑不同,SO2的轉化率隨反應溫度的變化如圖1,Fe2O3和NiO作催化劑均能使SO2的轉化率達到最高,不考慮催化劑價格因素,選擇Fe2O3的主要優點是:。
②某科研小組用Fe2O3作催化劑。在380℃時,分別研究了n(CO):n(SO2)為1:1、3:1時SO2轉化率的變化情況(圖2)。則圖2中表示n(CO):n(SO2)=3:1的變化曲線為。
(3)已知NO2存在如下平衡:2NO2(g)?N2O4(g)△H<0,在一定條件下NO2與N2O4的消耗速率與各自的分壓(分壓=總壓×物質的量分數)有如下關系:v(NO2)=k1?p2(NO2),v(N2O4)=k2?p(N2O4),相應的速率與其分壓關系如圖3所示。一定溫度下,k1、k2與平衡常數Kp(壓力平衡常數,用平衡分壓代替平衡濃度計算)間的關系是k1=;在圖標出點中,指出能表示反應達到平衡狀態的點是,理由是。組卷:86引用:1難度:0.5


