2020-2021學(xué)年北京市朝陽區(qū)高一(下)期末化學(xué)試卷
發(fā)布:2024/11/8 21:0:2
一.第一部分(選擇題,共42分)每小題只有一個(gè)選項(xiàng)符合題意。共14個(gè)小題,每小題3分,共42分。
-
1.汽車的零部件使用了四千余種不同的材料。下列零部件所用材料的主要成分屬于無機(jī)非金屬材料的是( )
A.車身主體--鋼鐵 B.汽車車窗--玻璃 C.汽車輪胎--合成橡膠 D.電線絕緣層--聚氯乙烯塑料 組卷:49引用:4難度:0.9 -
2.工業(yè)上常用電解法冶煉的金屬是( )
A.Al B.Fe C.Hg D.Ag 組卷:32引用:4難度:0.7 -
3.下列物質(zhì)的應(yīng)用中,利用了氧化還原反應(yīng)的是( )
A.用液氨作制冷劑 B.用H2和O2作燃料電池的反應(yīng)物 C.用CaO處理酸性廢水 D.用Na2CO3除去粗鹽中的Ca2+ 組卷:57引用:3難度:0.8 -
4.以下措施是為了加快化學(xué)反應(yīng)速率的是( )
A.葡萄酒中添加SO2作抗氧化劑 B.塑料中添加防老劑 C.燃煤發(fā)電時(shí)用煤粉代替煤塊 D.低溫保存運(yùn)輸疫苗 組卷:101引用:3難度:0.5 -
5.下列關(guān)于乙烯、乙醇、乙酸的說法不正確的是( )
A.乙烯屬于烴,乙醇、乙酸屬于烴的衍生物 B.乙烯不含官能團(tuán),乙醇、乙酸的官能團(tuán)相同 C.乙烯難溶于水,乙醇、乙酸易溶于水 D.三者之間存在轉(zhuǎn)化:乙烯 乙醇H2O乙酸酸性KMnO4溶液組卷:188引用:3難度:0.6 -
6.下列有關(guān)工業(yè)生產(chǎn)的說法不正確的是( )
A.利用油脂的加成反應(yīng)制肥皂 B.利用淀粉的水解反應(yīng)生產(chǎn)葡萄糖 C.通過煤的氣化得到水煤氣(CO、H2)等氣體燃料 D.通過石油的裂化和裂解得到乙烯、丙烯等化工原料 組卷:76引用:4難度:0.8
二.第二部分(非選擇題,共58分)
-
 19.氨既是一種重要的化工產(chǎn)品,也是一種重要的化工原料。
19.氨既是一種重要的化工產(chǎn)品,也是一種重要的化工原料。
(1)實(shí)驗(yàn)室利用如圖所示裝置及藥品制取氨氣。
①制取氨氣的化學(xué)方程式是。
②下列裝置中,可用于收集氨的是(填字母)。
(2)氨是生產(chǎn)氮肥的原料,經(jīng)過如下轉(zhuǎn)化可以得到NH4NO3。
NH3NO①NO2②HNO3③NH4NO3④
寫出反應(yīng)①的方程式:。
(3)過量施用氮肥會(huì)造成水體污染。納米零價(jià)鐵——反硝化細(xì)菌復(fù)合體系可脫除水體中的硝酸鹽(),脫氮原理及對(duì)某酸性廢水的脫氮效果如圖。NO-3
注:納米零價(jià)鐵對(duì)反硝化細(xì)菌具有抑制作用
①0~2天,發(fā)生的主要反應(yīng)為:Fe++NO-3═Fe2+++
②4~5天,檢測(cè)到納米零價(jià)鐵有剩余,但濃度無明顯變化,結(jié)合方程式說明原因:NO-3。
③6~8天,結(jié)合離子方程式說明溶液中濃度下降的原因是NO-3。組卷:106引用:4難度:0.7 -
20.小組探究NO2與NaOH溶液的反應(yīng)。
注:AgNO2為黃色固體,難溶于水。
(1)用Cu與濃HNO3制取NO2,化學(xué)方程式為。
(2)NO2不能用排水法收集,因?yàn)镹O2與水反應(yīng)生成和NO。
(3)將充滿NO2的試管倒扣在NaOH溶液中,液體迅速充滿試管,且較長(zhǎng)時(shí)間無明顯變化。
①取試管中溶液,加(填試劑),產(chǎn)生黃色沉淀,說明溶液中含有。NO-2
②寫出NO2與NaOH溶液反應(yīng)的化學(xué)方程式:。
(4)探究NO2與NaOH溶液反應(yīng)和NO2與水反應(yīng)還原產(chǎn)物N元素價(jià)態(tài)不同的原因。
查閱資料:NO2與水反應(yīng)分步進(jìn)行:
i.NO2溶于水生成HNO2(氧化性強(qiáng)于HNO3);
ii.HNO2不穩(wěn)定,發(fā)生分解。
實(shí)驗(yàn)探究:將充滿NO2的試管倒扣在水槽中,液面迅速上升,幾乎充滿試管(圖Ⅰ),一段時(shí)間后,試管中液面下降(圖Ⅱ)。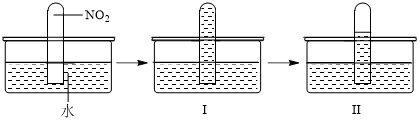
①檢驗(yàn)圖Ⅱ試管中氣體成分。(填操作和現(xiàn)象),證實(shí)氣體為NO。
②取圖Ⅰ試管中液體,滴加酸性KMnO4溶液,溶液褪色,證實(shí)溶液中存在HNO2。
小組討論將酸性KMnO4溶液更換為淀粉KI溶液的可行性。
甲同學(xué)認(rèn)為不可行,理由是;乙同學(xué)認(rèn)為可行,并通過對(duì)比實(shí)驗(yàn)證實(shí)了自己的觀點(diǎn),寫出乙同學(xué)的實(shí)驗(yàn)方案:。
③分析NO2與NaOH溶液反應(yīng)和NO2與水反應(yīng)還原產(chǎn)物N元素價(jià)態(tài)不同的原因:。組卷:79引用:2難度:0.4


