新人教版九年級下冊《8.2 金屬的化學性質》2019年同步練習卷(廣東省汕頭市龍湖實驗中學)(1)
發布:2024/4/20 14:35:0
一、選擇題
-
1.等質量的鎂和鋅分別放置在兩只燒杯中,分別加入足量的稀硫酸,能正確反映該變化的是( )
A. 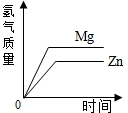
B. 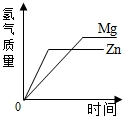
C. 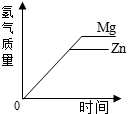
D. 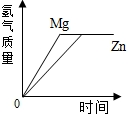 組卷:115引用:3難度:0.7
組卷:115引用:3難度:0.7 -
2.下列圖形正確的是( )
A. 
煅燒碳酸鈣B. 
雙氧水分解C. 
向等體積、等濃度的稀鹽酸中加金屬D. 
分別向稀鹽酸中加入等質量Fe和Mg組卷:32引用:1難度:0.5 -
3.工業冶煉金屬錳的原理是3MnO2+4Al
3Mn+2Al2O3,該反應屬于( )高溫A.置換反應 B.化合反應 C.分解反應 D.復分解反應 組卷:315引用:39難度:0.9 -
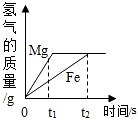 4.將等質量的鎂和鐵分別放入等質量、相同質量分數的稀鹽酸中,產生氫氣的質量和反應時間的關系如圖所示,下列說法錯誤的是( )
4.將等質量的鎂和鐵分別放入等質量、相同質量分數的稀鹽酸中,產生氫氣的質量和反應時間的關系如圖所示,下列說法錯誤的是( )A.反應結束后鎂一定有剩余 B.反應消耗鹽酸的總質量一定相等 C.0-t1時段,產生氫氣的質量鎂比鐵大 D.0-t2時段,參加反應的鎂的質量與鐵相等 組卷:2651引用:77難度:0.7 -
 5.如圖,將等質量的鋅和鐵分別入入左、右試管中,加入等質量、等質量分數的稀鹽酸,充分反應后,冷卻到室溫,金屬均有剩余,(U型管內為水,初始液面相平,反應過程中裝置氣密性良好)下列說法正確的是( )
5.如圖,將等質量的鋅和鐵分別入入左、右試管中,加入等質量、等質量分數的稀鹽酸,充分反應后,冷卻到室溫,金屬均有剩余,(U型管內為水,初始液面相平,反應過程中裝置氣密性良好)下列說法正確的是( )A.右試管中溶液為淺綠色 B.兩試管中所得溶液的質量相等 C.U型管中液面左升右降 D.U型管中液面仍相平 組卷:458引用:43難度:0.5
四、填空題(共2小題,每小題0分,滿分0分)
-
14.一定量銅粉和鋅粉組成的混合物與足量稀鹽酸充分反應,過濾,將濾渣在空氣中充分加熱,加熱后所得產物的質量恰好等于原混合物的質量,則原混合物中銅的質量分數為
.組卷:255引用:39難度:0.5 -
15.已知木炭還原氧化銅實驗中發生的主要反應:C+2CuO
2Cu+CO2↑.化學興趣小組對該實驗產物(假設反應物已完全反應)作如下探究:高溫
探究一:檢驗產物的成分
【提出問題】實驗產物是暗紅色固體,很難觀察到紫紅色固體.暗紅色固體是什么?
【查閱資料】氧化亞銅(Cu2O)為紅色固體;Cu2O+H2SO4═CuSO4+Cu+H2O.
【猜想與假設】暗紅色固體除銅外還可能含有Cu2O.
【設計實驗】取少量暗紅色固體,加入稀硫酸,如果觀察到現象:,說明暗紅色固體含有Cu2O.
探究二:測定產物中Cu2O的含量
原理:Cu2O+H22Cu+H2O,稱取一定質量的固體樣品,用如圖裝置進行實驗(固定裝置略去,堿石灰為氧化鈣和氫氧化鈉的混合物),通過測定反應前后裝置d的質量達到實驗目的.△
(1)裝置a中用稀硫酸而不用稀鹽酸,原因是;
(2)若不加裝置e,實驗結果會偏高,原因是;
(3)點燃酒精燈前涉及的部分操作如下,正確的順序是
①打開K2,關閉K1 ②檢查裝置的氣密性
③連接儀器 ④關閉K2,打開K1,通氫氣一段時間
(4)還可通過測定反應前后裝置(填“a”、“b”或“c”)的質量達到實驗目的.組卷:215引用:5難度:0.1


