2022-2023學年福建省福州四中高二(上)期末化學試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(本題包括12小題,每小題4分,共48分,每小題只有一個選項符合題意。)
-
1.學習“化學平衡移動原理”后,以你的理解,下列敘述正確的是( )
A.升高溫度,化學平衡一定會發(fā)生移動 B.2HI(g)?H2(g)+I2(g)達平衡后,增大壓強使顏色變深,可用勒夏特列原理解釋 C.在盛有一定量NO2的注射器中,向外拉活塞,其中氣體顏色先變淺再變深,甚至比原來深 D.對于已達平衡的體系,改變影響化學平衡的條件,不可能出現(xiàn)V正增大,V逆減小的情況 組卷:170引用:4難度:0.6 -
2.H2和I2在一定條件下能發(fā)生反應:H2(g)+I2(g)?2HI(g),1molH2完全反應放出akJ熱量。已知:
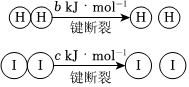 (a、b、c均大于零)
(a、b、c均大于零)
下列說法不正確的是( )A.反應物的總能量高于生成物的總能量 B.斷開1molH-H鍵和1molI-I鍵所需能量大于斷開2molH-I鍵所需能量 C.斷開2molH-I鍵所需能量約為(c+b+a)kJ D.向密閉容器中加入2molH2和2molI2,充分反應放出的熱量小于2akJ 組卷:89引用:1難度:0.6 -
3.25℃時,水的電離達到平衡:H2O?H++OH-△H>0,下列敘述正確的是( )
A.向水中加入稀氨水,平衡逆向移動,c(OH-)降低 B.向水中加入少量固體硫酸氫鈉,c(H+)增大,Kw不變 C.由水電離出的c(H+)═1×10-12mol/L的溶液pH一定為12 D.將水加熱,Kw增大,pH不變 組卷:112引用:3難度:0.8 -
4.某小組同學進行如下實驗探究:
已知:難溶電解質 顏色 Ksp ZnS 白色 1.6×10-24 CuS 黑色 1.3×10-36 FeS 黑色 6.3×10-18 ≈1.26×10-12;常溫下,幾種難溶物質的顏色和溶度積常數(shù)如圖。1.6×10-24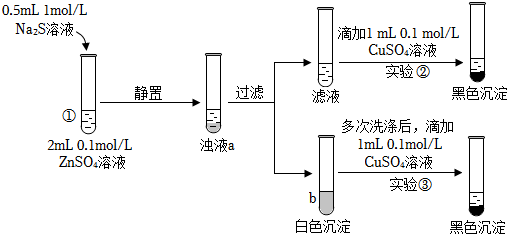
下列說法中,不正確的是( )A.①中濁液生成的原因是:Zn2++S2-═ZnS↓ B.a(chǎn)中濁液中存在溶解平衡:ZnS(s)?Zn2+(aq)+S2-(aq) C.實驗②和③生成黑色沉淀,可用相同的離子方程式表示 D.若在試管b中滴加1mL0.1mol?L-1FeSO4溶液,白色沉淀可以轉化為黑色沉淀 組卷:42引用:2難度:0.5 -
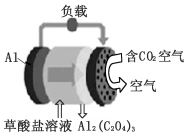 5.《科學美國人》評出的2016年十大創(chuàng)新技術之一是碳呼吸電池,電池原理如圖所示,已知草酸鋁[Al2(C2O4)3]難溶于水。則下列有關說法正確的是( )
5.《科學美國人》評出的2016年十大創(chuàng)新技術之一是碳呼吸電池,電池原理如圖所示,已知草酸鋁[Al2(C2O4)3]難溶于水。則下列有關說法正確的是( )A.該裝置將電能轉變?yōu)榛瘜W能 B.正極的電極反應為C2 -2e-═2CO2O2-4C.每生成1molAl2(C2O4)3,有 6mol 電子流過負載 D.草酸鹽溶液中的陽離子移向Al電極 組卷:33引用:3難度:0.7
二.簡答填空題(本題共5題,共52分)
-
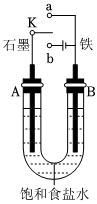 16.某課外活動小組用如圖裝置進行實驗,試回答下列問題:
16.某課外活動小組用如圖裝置進行實驗,試回答下列問題:
(1)若開始時開關K與a連接,B極的Fe發(fā)生腐蝕(填“析氫”或“吸氧”)。
(2)若開始時開關K與b連接,下列說法正確的是(填序號)。
①溶液中Na+向A極移動
②從A極處逸出的氣體能使?jié)駶櫟腒I淀粉試紙變藍
③反應一段時間后加適量鹽酸可恢復到電解前電解質的濃度
④若標準狀況下B極產(chǎn)生2.24L氣體,則溶液中轉移0.2mol電子
(3)該小組同學認為,如果模擬工業(yè)上離子交換膜法制燒堿的方法,那么可以設想用如圖裝置電解硫酸鉀溶液來制取氫氣、氧氣、硫酸和氫氧化鉀。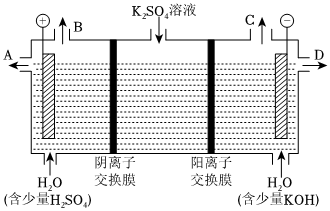
①該電解槽的陽極反應式為,此時通過陰離子交換膜的離子數(shù)(填“大于”“小于”或“等于”)通過陽離子交換膜的離子數(shù)。
②制得的氫氧化鉀溶液從出口(填“A”“B”“C”或“D”)導出。用惰性電極電解體積為1L的CuSO4溶液,當陰陽極都產(chǎn)生3.36L(標況)氣體時,請問硫酸銅的濃度為,若要此溶液恢復到原狀態(tài)需要加入(填選項)。
A.CuSO4
B.CuO
C.Cu(OH)2
D.Cu2(OH)2CO3組卷:24引用:1難度:0.5 -
17.某油脂廠廢棄的油脂加氫鎳催化劑主要含金屬Ni、Al、Fe及其氧化物,還有少量其他不溶性物質。采用如圖工藝流程回收其中的鎳制備硫酸鎳晶體(NiSO4?6H2O):
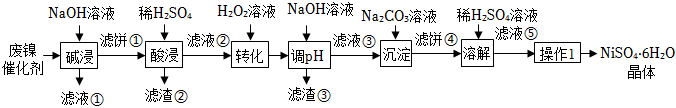
金屬離子 Ni2+ Al3+ Fe3+ Fe2+ 開始沉淀時(c=0.01mol?L-1)的pH 7.2 3.7 2.2 7.5 沉淀完全時(c=1.0×10-5mol?L-1)的pH 8.7 4.7 3.2 9.0 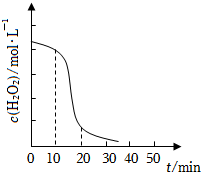
回答下列問題:
(1)“堿浸”中NaOH的兩個作用分別是①溶解鋁及其氧化物,②。
(2)“轉化”過程中反應的離子方程式為,c(H2O2)隨時間t的變化關系如圖所示,反應開始10~20min內(nèi)c(H2O2)迅速減小,原因可能是(不考慮溶液溫度變化)。
(3)為除去溶液中的Al、Fe元素,“轉化”后加入適量NaOH溶液調節(jié)pH,也可以用(從下面四個選項選擇)代替。
A.NiO
B.Cl2
C.Ni(OH)2
D.氨水
(4)利用上述表格數(shù)據(jù),計算Ni(OH)2的Ksp=。如果“轉化”后的溶液中Ni2+濃度為1.0mol?L-1,則“調pH”應控制的pH范圍是。
(5)硫酸鎳結晶水合物的形態(tài)與溫度的關系如下表。
從濾液⑤中獲得穩(wěn)定NiSO4?6H2O晶體的操作1依次是蒸發(fā)濃縮、溫度 低于30.8℃ 30.8℃~53.8℃ 53.8℃~280℃ 高于280℃ 晶體形態(tài) NiSO4?7H2O NiSO4?6H2O 多種結晶水合物 NiSO4 、過濾、洗滌、干燥。
(6)分離出NiSO4?6H2O晶體后的剩余液體要循環(huán)使用,則應該回流到流程中濾液的位置(填②、③、⑤),其目的是。組卷:33引用:3難度:0.5


