2021-2022學年江蘇省連云港市高一(上)期末化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題:共12小題,每小題3分,共42分.每小題只有一個選項最符合題意.
-
1.國慶慶典晚會上的焰火發射藥中含有K2FeO4。從物質分類的角度看,K2FeO4屬于( )
A.鹽 B.堿 C.氧化物 D.有機物 組卷:33引用:1難度:0.9 -
2.做心電圖檢查時,在儀器和皮膚接觸部位需涂抹一種無色電解質溶液。該電解質溶液是( )
A.醫用酒精 B.淀粉溶液 C.氯化鈉溶液 D.葡萄糖溶液 組卷:31引用:2難度:0.7 -
3.反應NH4Cl2+NaNO2═NaCl+N2↑+2H2O放熱且產生氣體,可用于冬天石油開采。下列說法正確的是( )
A.N2的結構式:N=N B.H2O的電子式: 
C.Cl-結構示意圖: 
D.NaNO2電離方程式:NaNO2═ +Na+NO-2組卷:14引用:1難度:0.7 -
4.實驗操作規范是實驗的基本要求。下列實驗操作正確的是( )
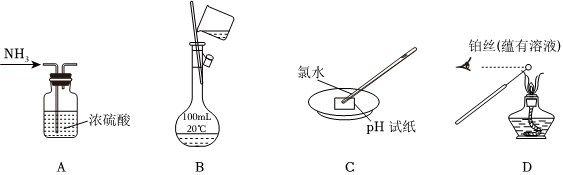
A.圖A可用于干燥NH3 B.圖B可用于配制100mLNaCl溶液 C.圖C可用于測氯水的pH D.圖D可用于檢驗鉀元素 組卷:15引用:1難度:0.7 -
5.下列有關鈉及其化合物的性質與用途對應關系錯誤的是( )
A.NaHCO3受熱易分解,可用于治療胃酸過多癥 B.Na2O2可吸收CO2產生O2,可用作呼吸面具供氧劑 C.Na2CO3溶液呈堿性,常用熱的純堿溶液去除物品表面的油污 D.鈉鉀合金常溫下呈液態,導熱性好,可用作快中子反應堆的熱交換劑 組卷:43引用:1難度:0.7
二、非選擇題:共4題,共58分.
-
17.鋁是活潑的金屬,某學習小組通過實驗探究鋁及其化合物的性質.
(1)用坩堝鉗夾住一片未打磨過的薄鋁片在酒精燈上加熱,鋁片內有熔化的物質被包裹著,但沒有熔融下滴.原因是.
(2)向AlCl3溶液中逐滴滴加氨水至氨水過量,實驗現象為.
(3)Al(OH)3既能溶于鹽酸又能溶于NaOH溶液,Al(OH)3溶于NaOH溶液的離子方程式為.
(4)AlCl3可作污水處理劑或石油工業的催化劑,通過如圖所示裝置制取少量AlCl3.
已知:無水氯化鋁是白色晶體,易升華,遇水或水蒸氣發生劇烈反應,產生Al(OH)3,同時看到有白霧現象.
①裝置A中反應的化學方程式為.
②該實驗中有兩處加熱裝置,實驗時先點燃的是,(填“A”或“D”)裝置的酒精燈.理由是.
③裝置E和裝置F之間連接有球形干燥管,作用是.
④無水AlCl3遇水蒸氣反應的化學方程式.組卷:28引用:1難度:0.5 -
18.研究SO2的性質,對SO2的污染防治與利用意義重大。
(1)將含有SO2的工業尾氣凈化后通入到1L0.1mol?L-1Na2CO3溶液中制備少許Na2SO3。
已知:向Na2CO3溶液中通入較少SO2時:SO2+H2O+2Na2CO3=Na2SO3+2NaHCO3;
較多SO2時會有CO2放出:當SO2過量時:SO2+H2O+Na2SO3=2NaHSO3。
溶液中各種組分的質量分數(ω)隨通入SO2的量變化關系如圖1所示。
①圖1中曲線2表示的組分質量分數先增大后降低的原因是。
②圖1中曲線3表示的組分為(填化學式)。
(2)碘循環工藝不僅能吸收SO2降低環境污染,同時又能制得氫氣,反應流程如圖2。
①該工藝流程中,反應①溫度不能過高的原因可能是。
②該工藝中,若有1mol SO2被氧化,產生標準狀況下氫氣的體積為。
(3)實驗室可利用SO2制取硫代硫酸鈉晶體(Na2S2O3?5H2O),為測定某樣品中硫代硫酸鈉晶體的質量分數,進行如下實驗:
步驟1:稱取1.00g樣品,溶于水,配成100mL的溶液,備用。
步驟2:量取15mL0.0100mol?L-1的KMnO4酸性溶液并加入過量KI溶液,充分反應。
步驟3:向步驟2所得溶液中滴加樣品溶液至20.00mL時,恰好完全反應。
已知:I-可以被空氣中氧氣氧化,樣品中的雜質與I2不發生反應。涉及的反應有:2+10I-+16H+=2Mn2++5I2+8H2O;I2+2S2MnO-4=S4O2-3+2I-。O2-6
①通過計算確定該樣品中Na2S2O3?5H2O的質量分數(寫出計算過程)。
②若所用的KI溶液在空氣中放置時間過長,可能會導致實驗結果(填“偏大”、“偏小”、“無影響”)組卷:37引用:1難度:0.5


