2016-2017學年河北省保定市定州中學承智班高二(下)周練化學試卷(4.9)
發布:2024/4/20 14:35:0
一、選擇題
-
1.下表所列各組第Ⅰ欄中的化學反應與第Ⅱ欄中的化學反應,都可以用第Ⅲ欄中的離子方程式表示的是( )
選項 第Ⅰ欄 第Ⅱ欄 第Ⅲ欄 A 往少量NaOH溶液中投入鋁片 往過量NaOH溶液中投入鋁片 2Al+2OH-+2H2O═2AlO2-+3H2↑ B 往Fe2(SO4)3溶液中滴入氫氧化鈉溶液 往Fe2(SO4)3溶液中滴入氫氧化鋇溶液 Fe3++3OH-═Fe(OH)3↓ C 往NaHCO3溶液中滴入Ca(OH)2溶液 往NaHCO3溶液中滴入NaOH溶液 OH-+HCO3-═CO32-+H2O D 往NaOH溶液中通入過量CO2 往NaOH溶液中通入少量CO2 CO2+OH-═HCO3- A.A B.B C.C D.D 組卷:45引用:9難度:0.7 -
2.下列敘述正確的是( )
A.金屬氧化物不一定是堿性氧化物 B.HCl、H2S、NH3都是電解質 C.強酸強堿都是離子化合物 D.FeBr3、FeCl2、CuS都不能直接用化合反應制備 組卷:14引用:2難度:0.9 -
3.下列分散系中具有丁達爾現象的有( )
A.蔗糖溶液 B.Fe(OH)3膠體 C.蛋白質溶液 D.NaCl溶液 組卷:26引用:3難度:0.5 -
4.廢舊電池集中處理的首要原因是( )
A.回收電池中的石墨電極 B.回收電池外殼的金屬材料 C.防止電池中汞、鎘等重金屬對土壤和水源的污染 D.防止電池中的滲出液腐蝕其他物品 組卷:9引用:4難度:0.9 -
5.下列關于1S電子在原子核外出現的概率分布圖(電子云)的說法中,正確的是( )

A.通常用小黑點來表示電子的多少 B.小黑點密表示在該核外空間的電子數多 C.小黑點密表示在該核外空間的單位體積內電子出現的概率大 D.通常用小黑點來表示電子繞核作高速圓周運動 組卷:17引用:2難度:0.7 -
6.下列說法錯誤的是( )
A.第ⅤA族元素的幾種氣態氫化物中,NH3是穩定性最高的氫化物 B.由于 和C2-2為等電子體,所以可以判斷O2+2的電子式為O2+2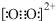
C.含離子鍵的純凈物一定存在金屬元素 D. 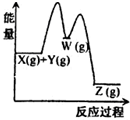 某反應X(g)+Y(g)?Z(g)△H<0 分兩步進行:X(g)+Y(g)?W(g)△H>0和W(g)?Z(g)△H<0,反應過程中的能量變化如圖組卷:6引用:3難度:0.9
某反應X(g)+Y(g)?Z(g)△H<0 分兩步進行:X(g)+Y(g)?W(g)△H>0和W(g)?Z(g)△H<0,反應過程中的能量變化如圖組卷:6引用:3難度:0.9 -
7.已知反應:①Cl2+2KBr═2KCl+Br2;②KClO3+6HCl═3Cl2↑+KCl+3H2O;③2KBrO3+Cl2═Br2+2KClO3下列說法正確的是( )
A.氧化性由強到弱的順序為KBrO3>KClO3>Cl2>Br2 B.①中KCl是氧化產物,KBr 發生還原反應 C.③中1mol氧化劑參加反應得到電子的物質的量為2mol D.反應②中氧化劑與還原劑的物質的量之比為1:6 組卷:389引用:20難度:0.7
二、實驗題
-
21.鋁是一種重要金屬,從鋁土礦(主要成分為Al2O3,Fe2O3、SiO2等)中冶煉Al的工業生產流程如下圖:

(1)沉淀B的化學式為,溶液A中含的陽離子主要有.
(2)寫出步驟II生成溶液C 的離子方程式,步驟I、Ⅱ、Ⅲ都要用到的分離方法是.
(3)生產過程中,除CaO可以循環使用外,還可以循環使用的物質有:(填化學式).
(4)生產中曾用鋁熱反應焊接鋼軌,則鋁與氧化鐵發生反應的化學方程式為:
(5)經分析,a噸鋁土礦可以冶煉出b噸的鋁(假設各生產環節中無損耗),則原鋁土礦中Al2O3的純度(質量分數)(用含a、b的最簡式表示).組卷:56引用:3難度:0.5 -
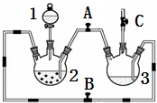 22.某化學興趣小組擬用如圖裝置制備氫氧化亞鐵并觀察其顏色.提供化學藥品:鐵屑、稀硫酸、氫氧化鈉溶液.
22.某化學興趣小組擬用如圖裝置制備氫氧化亞鐵并觀察其顏色.提供化學藥品:鐵屑、稀硫酸、氫氧化鈉溶液.
(1)稀硫酸應放在中(填寫儀器名稱).
(2)本實驗通過控制A、B、C三個開關,將儀器中的空氣排盡后,再關閉開關、打開開關就可觀察到氫氧化亞鐵的顏色.試分析實驗開始時排盡裝置中空氣的理由
(3)實驗時為防止儀器2中鐵粉通過導管進入儀器3中,可采取的措施是.
(4)在FeSO4溶液中加入(NH4)2SO4固體可制備摩爾鹽晶體 (相對分子質量392),該晶體比一般亞鐵鹽穩定,不易被氧化,易溶于水,不溶于乙醇.
①為洗滌(NH4)2SO4?FeSO4?6H2O粗產品,下列方法中最合適的是
A.用冷水洗 B.先用冷水洗,后用無水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
②為了測定產品的純度,稱取a g產品溶于水,配制成500mL溶液,用濃度為c mol?L-1的酸性KMnO4溶液滴定.每次所取待測液體積均為25.00mL,實驗結果記錄如下:
滴定過程中發生反應的離子方程式為實驗次數 第一次 第二次來 第三次 消耗高錳酸鉀溶液體積/mL 25.52 25.02 24.98
滴定終點的現象是
通過實驗數據計算的該產品純度為(用字母ac表示).上表中第一次實驗中記錄數據明顯大于后兩次,其原因可能是
A.實驗結束時俯視刻度線讀取滴定終點時酸性高錳酸鉀溶液的體積
B.滴定前滴定管尖嘴有氣泡,滴定結束無氣泡
C.第一次滴定用的錐形瓶用待裝液潤洗過,后兩次未潤洗
D.該酸性高錳酸鉀標準液保存時間過長,有部分變質,濃度降低.組卷:9引用:2難度:0.5


