2021-2022學(xué)年新疆烏魯木齊八中高二(下)期中化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題:(每題只有一個(gè)正確答案,每題2分,共42分)
-
1.下列有關(guān)認(rèn)識(shí)正確的是( )
A.各能級(jí)的原子軌道數(shù)按s、p、d、f的順序依次為1、3、5、7 B.各能層的能級(jí)都是從s能級(jí)開(kāi)始至f能級(jí)結(jié)束 C.各能層含有的能級(jí)數(shù)為n-1 D.各能層含有的電子數(shù)為2n2 組卷:382引用:23難度:0.7 -
2.下列有關(guān)元素周期表分區(qū)的說(shuō)法錯(cuò)誤的是( )
A.p區(qū)不包含副族元素 B.第五周期有15種f區(qū)元素 C.d區(qū)、ds區(qū)均不存在非金屬元素 D.s區(qū)所有元素的p能級(jí)電子均為全滿(mǎn)或全空狀態(tài) 組卷:57引用:6難度:0.8 -
3.下列化學(xué)用語(yǔ)表述正確的是( )
A.鎂原子由1s22s22p63s13p1→1s22s22p63s2時(shí),原子釋放能量,由激發(fā)態(tài)轉(zhuǎn)化成基態(tài) B.基態(tài)Se的價(jià)電子排布式:3d104s24p4 C.基態(tài)鈹原子最外層電子的電子云圖為: 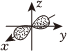
D.電子僅在激發(fā)態(tài)躍進(jìn)到基態(tài)時(shí)才會(huì)產(chǎn)生原子光譜 組卷:129引用:7難度:0.6 -
4.下列四種元素中,第一電離能由大到小順序正確的是( )
①原子含有未成對(duì)電子最多的第二周期元素
②電子排布為1s2的元素
③周期表中電負(fù)性最強(qiáng)的元素
④原子最外層電子排布為3s23p4的元素.A.②③①④ B.③①④② C.①③④② D.無(wú)法比較 組卷:56引用:4難度:0.9 -
5.已知X、Y、Z、W是短周期元素。X元素原子的2p能級(jí)處于半充滿(mǎn)狀態(tài);Y元素原子最外電子層(L電子層)上s電子數(shù)和p電子數(shù)相等;Z元素的+2價(jià)陽(yáng)離子的核外電子排布與氖原子相同;W元素原子的M電子層有1個(gè)未成對(duì)的p電子。下列說(shuō)法一定正確的是( )
A.含有X元素的化合物一定是共價(jià)化合物 B.Y元素的電負(fù)性大于X元素的電負(fù)性 C.X元素的單質(zhì)與Z元素的單質(zhì)在一定條件下能發(fā)生化合反應(yīng) D.W元素的單質(zhì)能與NaOH溶液反應(yīng)放出氫氣 組卷:5引用:3難度:0.6 -
6.具有下列電子層結(jié)構(gòu)的原子或離子,其對(duì)應(yīng)的元素一定屬于同一周期的是( )
A.兩原子N層上都有1個(gè)s電子,一個(gè)原子無(wú)d電子,另一個(gè)原子有d電子 B.兩原子其核外全部都是s電子 C.最外層電子排布為2s22p5的原子和最外層電子排布為2s22p6的離子 D.原子核外M層上的s、p能級(jí)都充滿(mǎn)電子,而d能級(jí)上沒(méi)有電子的兩種原子 組卷:15引用:4難度:0.7 -
7.許多金屬鹽都可以發(fā)生焰色反應(yīng),其原因是激發(fā)態(tài)的電從能量高的軌道躍遷到能量低的軌道時(shí),能量以一定的波長(zhǎng)(可見(jiàn)光區(qū)域)光的形式釋放。下列現(xiàn)象和應(yīng)用與電子躍遷無(wú)關(guān)的是( )
A.激光 B.石墨導(dǎo)電 C.霓虹燈 D.原子光譜 組卷:83引用:5難度:0.7 -
8.下列說(shuō)法正確的是( )
A.所有的原子軌道都具有一定的伸展方向,因此所有的共價(jià)鍵都具有方向性 B.某原子跟其他原子形成共價(jià)鍵時(shí),其共價(jià)鍵數(shù)一定等于該元素原子的價(jià)電子數(shù) C.基態(tài)C原子有兩個(gè)未成對(duì)電子,所以最多只能形成2個(gè)共價(jià)鍵 D.1個(gè)N原子最多只能與3個(gè)H原子結(jié)合形成NH3分子,是由共價(jià)鍵的飽和性決定的 組卷:224引用:5難度:0.8
二、填空題題:(共58分)
-
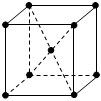 24.Ⅰ.如圖是金屬鎢晶體中一個(gè)晶胞的結(jié)構(gòu)示意圖。實(shí)驗(yàn)測(cè)得金屬鎢的密度為19.30g?cm-3,鎢的相對(duì)原子質(zhì)量是183.9。假設(shè)金屬鎢原子為等徑剛性球,試完成下列問(wèn)題:
24.Ⅰ.如圖是金屬鎢晶體中一個(gè)晶胞的結(jié)構(gòu)示意圖。實(shí)驗(yàn)測(cè)得金屬鎢的密度為19.30g?cm-3,鎢的相對(duì)原子質(zhì)量是183.9。假設(shè)金屬鎢原子為等徑剛性球,試完成下列問(wèn)題:
(1)鎢的晶胞堆積方式為,每一個(gè)晶胞中均攤到個(gè)鎢原子,空間利用率為。
(2)列式表達(dá)晶胞的邊長(zhǎng)a。
(3)計(jì)算鎢的原子半徑r。(用含a的代數(shù)式表達(dá))
Ⅱ.一種離子晶體的晶胞如圖其中陽(yáng)離子以A表示,陰離子以B表示。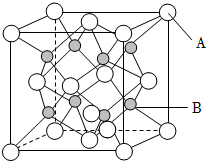
(4)每個(gè)晶胞中含A離子的數(shù)目為,含B離子數(shù)目為。
(5)若A的核外電子排布與Ar相同,B的電子排布與Ne相同,則該離子化合物的化學(xué)式是。
(6)陽(yáng)離子周?chē)嚯x最近的陰離子數(shù)為,陰離子周?chē)嚯x最近的陽(yáng)離子數(shù)。
(7)已知A的離子半徑為rcm,則該晶胞的體積是cm3。組卷:15引用:1難度:0.5 -
25.X、Y、Z、W、R、Q為前30號(hào)元素,且原子序數(shù)依次增大。X是元素周期表中原子半徑最小的元素;Y元素基態(tài)原子有三個(gè)能級(jí)上有電子,且每個(gè)能級(jí)上的電子數(shù)相等;Z元素基態(tài)原子的單電子數(shù)在同周期元素基態(tài)原子中最多;W與Z同周期,第一電離能比Z的低;R與Y同主族;Q的最外層只有一個(gè)電子,其他電子層均有2n2個(gè)電子(n表示電子層序數(shù))。請(qǐng)回答下列問(wèn)題:
(1)元素Q在元素周期表中的位置為,Q+的核外電子排布式為。
(2)化合物X2W2的電子式為,W的雜化方式為;的空間結(jié)構(gòu)為ZW-2。
(3)Y、R的最高價(jià)氧化物中沸點(diǎn)較高的是(填化學(xué)式),原因是。Y、R的最高價(jià)氧化物對(duì)應(yīng)水化物酸性較強(qiáng)的是(填化學(xué)式),通過(guò)離子方程式可以證明。
(4)原子坐標(biāo)參數(shù)和晶胞參數(shù)是晶胞的兩個(gè)基本參數(shù)。
①圖a中原子坐標(biāo)參數(shù)分別為:A(0,0,0),B(,12,0),C(12,0,12),則D的原子坐標(biāo)參數(shù)為12。
②圖b為銅的晶胞,銅原子半徑為Rnm,NA是阿伏加德羅常數(shù)的值,則銅晶體的密度為g?cm-3(用含R、NA的式子表示)。組卷:11引用:1難度:0.5


