2022年上海市徐匯區高考化學三模試卷
發布:2024/4/20 14:35:0
一、選擇題(共40分,每小題2分。每小題只有一個正確答案)
-
1.金屬表面的電子在光線照射下逸出產生電流的現象稱為光電效應。以下堿金屬中最容易發生光電效應的是( )
A.Na B.K C.Rb D.Cs 組卷:33引用:3難度:0.7 -
2.下列各組物質中,化學鍵類型和晶體類型都相同的是( )
A.Ar和K B.NaCl和NaOH C.CH4和H2O D.CO2和SiO2 組卷:34引用:2難度:0.6 -
3.實驗室制備Na2S2O3的反應原理:2Na2S+Na2CO3+4SO2→3Na2S2O3+CO2。下列說法正確的是( )
A.O原子的軌道表示式: 
B.Na2S的電子式: 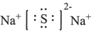
C.SO2是V型的非極性分子 D.CO2的結構式: 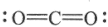 組卷:16引用:1難度:0.7
組卷:16引用:1難度:0.7 -
4.1934年居里夫婦用a粒子轟擊金屬原子
X,發現了人工放射性。涉及反應:wzX+wzHe→42Y+30z+2n(10n為中子),其中X、Y的最外層電子數之和為8。下列說法正確的是( )10A.元素Y的相對原子質量為30 B.X是鋁元素 C.原子半徑:Y>X D.Y的含氧酸屬于強電解質 組卷:29引用:2難度:0.5 -
5.下列關于硫酸的說法正確的是( )
A.常溫下,可用鐵片與濃硫酸制取FeSO4 B.實驗室用98%的濃硫酸與Na2SO3固體制取SO2 C.實驗室制備乙烯時,濃硫酸與乙醇的體積投料比約為3:1 D.等質量的水和發煙硫酸(H2SO4?xSO3)混合后所得溶質質量分數為50% 組卷:38引用:2難度:0.6 -
6.雙氧水(H2O2)與下列溶液反應,不能體現H2O2氧化性的是( )
A.酸性KMnO4溶液 B.淀粉KI溶液 C.溶有SO2的BaCl2溶液 D.鹽酸酸化的FeCl2溶液 組卷:34引用:2難度:0.7 -
7.硫酸銅晶體中結晶水含量測定的實驗中,會導致測定結果偏小的操作是( )
A.在空氣中冷卻 B.加熱時有晶體濺出 C.玻璃棒上沾有少量固體 D.加熱后有少量黑色固體生成 組卷:21引用:2難度:0.7 -
8.汽車碰撞時,安全氣囊中發生反應:10NaN3+2KNO3→K2O+5Na2O+16N2↑。若氧化產物比還原產物多7mol,下列說法錯誤的是( )
A.生成8molN2 B.1molKNO3被還原 C.轉移7mol電子 D.15mol氮原子被氧化 組卷:48引用:3難度:0.7
二、綜合題(共60分)
-
23.一種類昆蟲信息激素中間體M的合成路線如圖:
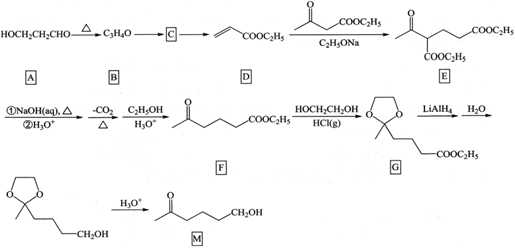
完成下列填空:
(1)A中官能團的名稱是、,A的合成方法之一:CH3CHO+XA,則X的結構式為OH-。
(2)反應A→B和D→E的反應類型分別是、。檢驗B是否完全轉化為C的方法是。
(3)寫出E→F的第一步反應①的化學方程式。設計步驟F→G的目的是。
(4)寫出一種滿足下列條件的M的同分異構體的結構簡式。
ⅰ.1mol M與足量金屬Na反應生成1molH2;
ⅱ.不能使Br/Br2/CCl4溶液褪色;
ⅲ.分子中有3種不同環境下的氫原子。
(5)結合題意,將以CH2=CH2為原料合成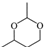 的合成路線補充完整 。
的合成路線補充完整 。
CH2=CH2CH3CHO→……→O2CuCl2-PdCl2,H2O 組卷:26引用:1難度:0.5
組卷:26引用:1難度:0.5 -
24.乙烷裂解制乙烯的方法有:
①直接裂解:C2H6(g)?C2H4(g)+H2(g)+Q1kJ(Q1<0)
②氧氣氧化裂解:2C2H6(g)+O2(g)?2C2H4(g)+2H2O(g)+Q2kJ(Q2>0)
完成下列填空:
(1)800℃時,在一恒壓密閉容器中加入一定量C2H6,發生反應①,達到平衡后向容器中通入稀有氣體He,C2H6的平衡轉化率(選填“增大”“減小”或“不變”)。要使該反應的平衡常數增大,可采取的措施是。
乙烷氧氣氧化裂解制乙烯,除發生反應②外,還發生副反應③:2C2H6(g)+7O2(g)?4CO2(g)+6H2O(g)。在800℃時用乙烷氧氣氧化裂解制乙烯,乙烷的轉化率、乙烯的選擇性和收率隨投料比的變化關系如圖所示。n(C2H6)n(O2)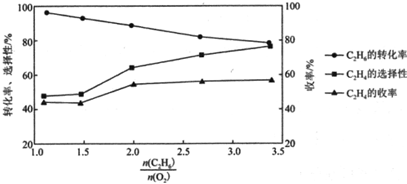
已知:
C2H4的選擇性=×100%生成的C2H4的物質的量反應的C2H6的物質的量
C2H4的收率=C2H6的轉化率×C2H4的選擇性
(2)控制=2而不采用選擇性更高的n(C2H6)n(O2)=3.5,除可防止積碳外,另一原因是n(C2H6)n(O2);<2時,n(C2H6)n(O2)越小,乙烷的轉化率越大,乙烯的選擇性和收率越小的原因是n(C2H6)n(O2)。
(3)T℃時,將2molC2H6和3molO2通入1L的恒容密閉容器中發生反應②③,t min達到平衡,平衡時C2H4的收率為60%,C2H4選擇性為75%。C2H6的轉化率為;0~tmin內,C2H4的平均生成速率為,O2的平衡濃度c(O2)=mol?L-1。
(4)通過比較反應①②的熱效應,指出氧化裂解法的優點。組卷:30引用:1難度:0.6


