2021-2022學年河北省衡水市冀州一中高三(上)期中化學試卷
發布:2024/4/20 14:35:0
一、單選題(每個3分,共27分)
-
1.“碳中和”是指一定時間內排放的碳總量與吸收的碳總量相互抵消,實現碳“零排放”,下列有關碳循環、碳中和的說法,錯誤的是( )
A.每個人都在參與碳循環,碳循環中的“碳”是指碳單質 B.開發可再生能源,降低化石燃料的需求量,以控制二氧化碳排放量 C.大力植樹造林,嚴禁亂砍濫伐森林,以控制二氧化碳排放量 D.碳中和能有效維持碳循環的相對穩定,控制日趨嚴重的溫室效應 組卷:9引用:2難度:0.9 -
2.將一定量純凈的氨基甲酸銨置于密閉真空容器中(假設容器體積不變,固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡:H2NCOONH4(s)?2NH3(g)+CO2(g)。下列能判斷該反應已經達到化學平衡的個數有( )
①v(NH3)正=2v(CO2)逆
②密閉容器中總壓強不變
③密閉容器中混合氣體的密度不變
④密閉容器中混合氣體的平均相對分子質量不變
⑤密閉容器混合氣體的總物質的量不變
⑥密閉容器中CO2的體積分數不變
⑦混合氣體總質量不變A.4個 B.5個 C.6個 D.7個 組卷:54引用:7難度:0.6 -
3.下列離子方程式書寫不正確的是( )
A.少量Cl2通入過量的Na2CO3溶液中:Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO- B.Ba(NO3)2溶液中通入少量SO2:3Ba2++2NO3-+3SO2+2H2O═3BaSO4↓+2NO↑+4H+ C.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O D.惰性電極電解MgCl2水溶液:Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑通電組卷:1引用:1難度:0.7 -
4.對下列粒子組在溶液中能否大量共存的判斷和分析均正確的是( )
粒子組 判斷和分析 A Na+、Al3+、Cl-、NH3?H2O 不能大量共存,因發生反應:Al3++4NH3?H2O═AlO2-+4NH4++H2O B I-、H2O2、Na+、H+ 不能大量共存,因發生反應:2I-+H2O2+2H+═2H2O+I2 C Na+、Fe3+、SO42-、H2O2 能大量共存,粒子間不反應 D H+、Na+、Cl-、MnO4- 能大量共存,粒子間不反應 A.A B.B C.C D.D 組卷:4引用:1難度:0.7 -
5.反應N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1可用于工業合成氨。在容積固定不變的密閉容器中加入1mol N2和3mol H2發生反應。下列敘述正確的是( )
A.該反應達到平衡時,放出的熱量等于92.4kJ B.達到平衡后向容器中通入1mol氦氣,平衡不移動 C.降低溫度和縮小容器體積均可使該反應的平衡常數增大 D.常溫常壓下,有22.4L的N2反應時轉移了6mol電子 組卷:13引用:2難度:0.6
三、填空題(共57分)
-
 16.CH4-CO2催化重整時發生反應:CH4(g)+CO2(g)?2CO(g)+2H2(g),不僅可以得到合成氣(CO和H2),還對溫室氣體的減排具有重要意義。回答下列問題:
16.CH4-CO2催化重整時發生反應:CH4(g)+CO2(g)?2CO(g)+2H2(g),不僅可以得到合成氣(CO和H2),還對溫室氣體的減排具有重要意義。回答下列問題:
(1)某溫度下,向1L的密閉容器中充入2molCH4與1molCO2,發生CH4-CO2催化重整反應,10min時達到平衡,測得平衡混合物中CO(g)的體積分數為20%,則用CH4表示的反應速率為。
(2)在一定溫度下,向固定容積為2L的密閉容器中充入1moCH4與1molCO2發生CH4-CO2催化重整反應,達平衡時CO2的平衡轉化率為50%,則此條件下該反應的平衡常數為K=;平衡后保持溫度不變,若再充入1.5molCH4、1.5molCO2、1molCO、1molH2,則此時v正v逆。(選填“>”、“<”或“=”)
(3)已知:C(s)+2H2(g)=CH4(g)ΔH1=-75kJ?mol-1
C(s)+O2(g)=CO2(g)ΔH2=-394kJ?mol-1
C(s)+O2(g)=CO(g)ΔH3=-111kJ?mol-112
①催化重整反應CH4(g)+CO2(g)?2CO(g)+2H2(g)的ΔH=kJ?mol-1。
②反應中催化劑活性會因積碳反應而降低,同時存在的消碳反應則使積碳量減少。相關數據如下表:
由上表判斷,催化劑X積碳反應CH4(g)═C(s)+2H2(g) 消碳反應CO2(g)+C(s
)═2CO(g)ΔH/(kJ?mol-1) +75 +172 活化能/(kJ?mol-1) 催化劑X 33 91 催化劑Y 43 72 Y(填“優于”或“劣于”),理由是。
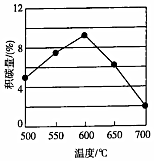
③反應進料氣組成、壓強及反應時間相同的情況下,某催化劑表面的積碳量隨溫度的變化關系如圖所示,升高溫度時,下列關于積碳反應、消碳反應的平衡常數(K)和速率(v)的敘述正確的是(填標號)。
A.K積、K消均增加
B.v消減小、v積增加
C.K積減小、K消增加
D.溫度高于600℃,v消增加的倍數比v積增加的倍數大組卷:3引用:1難度:0.5 -
17.深紫外固體激光器可用于高溫超導、催化劑研究等領域。我國自主研發的用氟硼鈹酸鉀(KBe2BO3F2)晶體制造深紫外固體激光器技術領先世界。回答下列問題:
(1)請畫出O原子的價層電子排布圖:,基態Be、B、O三種元素的原子第一電離能由大到小的順序為。
(2)在500℃~600℃氣相中,氯化鈹以二聚體Be2Cl4的形式存在,在該二聚體中Be原子的雜化方式是,1molBe2Cl4含有的配位鍵數目為。
(3)Xe是第五周期的稀有氣體元素,與F形成的XeF4中心原子的價層電子對數為,下列對XeF4中心原子雜化方式推斷合理的是(填標號)。
A.sp
B.sp2
C.sp3d2
D.sp3d
(4)甲醇的沸點(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之間,其原因是。
(5)BeO晶體是制備氟硼鈹酸鉀晶體的原料之一,其晶胞結構與ZnS類似,如圖所示。Be原子的配位數是;該晶胞中原子的位置可以用原子分數坐標表示,若原子A,B的坐標分別為(0,0,0),(,12,1);則C原子坐標為12。設O與Be的最近距離為apm,用NA表示阿伏加德羅常數的值,則BeO晶體的密度的計算表達式為g?cm-3(用含a和NA的式子表示)。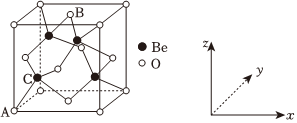 組卷:5引用:1難度:0.6
組卷:5引用:1難度:0.6


