2022-2023學(xué)年重慶市萬(wàn)州二中高三(上)月考化學(xué)試卷(12月份)
發(fā)布:2024/9/13 13:0:8
一、單選題(共14小題,每題3分,共42分)
-
1.下列有關(guān)唐詩(shī)中詩(shī)句的說(shuō)法正確的是( )
A.韓愈的詩(shī)“天街小雨潤(rùn)如酥”中“酥”指動(dòng)物的油,易溶于水 B.劉禹錫的詩(shī)“農(nóng)父綠蓑衣”中“綠蓑”的主要成分是纖維素,屬于天然有機(jī)高分子 C.白居易的詩(shī)“秋霜欲下手先知,燈底裁縫剪刀冷”中“剪刀冷”說(shuō)明金屬熔點(diǎn)低 D.李白寫(xiě)道“花間一壺酒,獨(dú)酌無(wú)相親”,描述飲酒的場(chǎng)景,白酒指含75%乙醇的乙醇溶液 組卷:5引用:2難度:0.5 -
2.設(shè)NA為阿伏加德羅常數(shù)的值。下列說(shuō)法正確的是( )
A.電解飽和食鹽水得到0.4molNaOH,則生成氯氣分子數(shù)為0.2NA B.標(biāo)準(zhǔn)狀況下,2.24LH2O所含氫原子的數(shù)目等于0.2NA C.Na2O2和H2O反應(yīng),當(dāng)產(chǎn)生2.24LO2時(shí)轉(zhuǎn)移的電子數(shù)為0.4NA D.密閉容器中,1molN2(g)與3molH2(g)反應(yīng)制備氨氣,形成6NA個(gè)N-H鍵 組卷:6引用:3難度:0.6 -
3.常溫下,下列各組離子在指定溶液中一定能大量共存的是( )
A.澄清透明的溶液中:Na+、H+、MnO4-、OH- B. =1×1012的溶液中:K+、Na+、CO32-、AlO2-c(OH-)c(H+)C.0.1mol?L-1FeCl3溶液:K+、NH4+、I-、SCN- D.能使甲基橙變紅的溶液中:Na+、Ca2+、S2-、CO32- 組卷:10引用:4難度:0.7 -
4.下列說(shuō)法錯(cuò)誤的是( )
A.常溫下,pH=7的溶液中不能大量存在Al3+、Fe3+ B.向含Mg(HCO3)2的溶液中加入足量NaOH溶液的離子方程式:Mg2++HCO3-+OH-═MgCO3↓+H2O C.向NaClO溶液中通入過(guò)量二氧化碳的離子方程式:ClO-+CO2+H2O═HClO+HCO3- D.向H2C2O4溶液中加少量NaOH溶液的離子方程式:H2C2O4+OH-═HC2O4-+H2O 組卷:6引用:3難度:0.7 -
5.在800℃下BI與As4單質(zhì)可發(fā)生化學(xué)反應(yīng)制備具有超高熱導(dǎo)率半導(dǎo)體材料--BAs晶體。下列說(shuō)法錯(cuò)誤的是( )
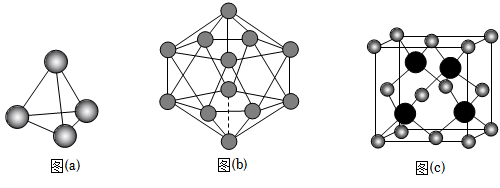
A.圖(a)表示As4結(jié)構(gòu),As4分子中成鍵電子對(duì)數(shù)與孤對(duì)電子數(shù)之比為3:1 B.圖(b)表示單質(zhì)硼晶體B12的基本結(jié)構(gòu)單元,該基本單元為正二十面體 C.圖(b)所示單質(zhì)硼晶體的熔點(diǎn)為2180℃,它屬于共價(jià)晶體 D.圖(c)表示BAs的晶胞結(jié)構(gòu),若晶胞參數(shù)為anm,則BAs晶體密度為 g/cm3344×1021a3NA組卷:44引用:3難度:0.5 -
6.2022年10月諾貝爾化學(xué)獎(jiǎng)授予三位在“咔嚓”(click)化學(xué)和生物正交化學(xué)有突出研究的化學(xué)家。如圖是首個(gè)click化學(xué)反應(yīng)。下列說(shuō)法錯(cuò)誤的是( )

A.化合物A能與NaOH發(fā)生中和反應(yīng) B.化合物B的分子式為C8H6,屬于芳香烴 C.化合物C中所有碳原子不可能共平面 D.化合物B、C能被氧化為羧酸 組卷:16引用:3難度:0.6
二、解答題(共4個(gè)小題,合計(jì)58分)
-
 17.氫氣是重要的化工原料,也是未來(lái)理想的能源物質(zhì)。回答下列問(wèn)題:
17.氫氣是重要的化工原料,也是未來(lái)理想的能源物質(zhì)。回答下列問(wèn)題:
(1)利用H2進(jìn)行煙氣催化還原脫硫的反應(yīng)機(jī)理如下:2H2(g)+SO2(g)═S(g)+2H2O(g)ΔH。已知由元素最穩(wěn)定的單質(zhì)生成1mol純化合物時(shí)的反應(yīng)熱稱為該化合物的標(biāo)準(zhǔn)摩爾生成焓E。已知SO2(g)、H2O(g)的標(biāo)準(zhǔn)摩爾生成焓分別為-296.9kJ?mol-1、-241.8kJ?mol-1,1mol固態(tài)硫轉(zhuǎn)變?yōu)闅鈶B(tài)硫原子吸熱280.0kJ,則上述反應(yīng)的焓變?chǔ)=kJ?mol-1。
(2)H2是水煤氣的重要組成部分,已知水煤氣反應(yīng)的反應(yīng)機(jī)理如下:CO2(g)+H2(g)═H2O(g)+CO(g)ΔH1>0(Ⅰ),在723K時(shí),將0.10mol的H2(g)和0.20mol的CO2(g)通入抽空的恒溫鋼瓶中,發(fā)生反應(yīng)(Ⅰ)。平衡后水蒸氣的物質(zhì)的量分?jǐn)?shù)為0.10。今在容器中加入過(guò)量的氧化鈷CoO(s)和金屬鈷Co(s),在容器中又增加了如下兩個(gè)平衡:CoO(s)+H2(g)═Co(s)+H2O(g)ΔH2(Ⅱ);CoO(s)+CO(g)═Co(s)+CO2(g)ΔH3(Ⅲ)。經(jīng)分析知容器中水蒸氣的物質(zhì)量分?jǐn)?shù)為0.30。回答下列問(wèn)題:
①K1、K2、K3分別為反應(yīng)(Ⅰ)、(Ⅱ)、(Ⅲ)的平衡常數(shù),則計(jì)算得出K2=;K3=。
②Shibata曾做過(guò)以下實(shí)驗(yàn):i.使純H2緩慢地通過(guò)處于994K下的過(guò)量CoO(s),CoO部分被還原為Co(s),平衡后氣體中H2的物質(zhì)的量分?jǐn)?shù)為0.0250;ii.在同一溫度下用CO還原CoO(s),平衡后氣體中CO的物質(zhì)的量分?jǐn)?shù)為0.0192,則反應(yīng)(Ⅱ)的ΔH20(填“>”“<”或“=”,下同);升高溫度,反應(yīng)(Ⅲ)正反應(yīng)速率的改變程度β1逆反應(yīng)速率的改變程度β2。
(3)電解法可實(shí)現(xiàn)CO2資源化利用,電解CO2制HCOOH的原理示意圖如圖所示:
①a、b表示CO2進(jìn)氣管,其中(填“a”或“b”)管是不需要的。
②寫(xiě)出陰極的電極反應(yīng)式:。組卷:3引用:2難度:0.5 -
18.一種新型含硅阻燃劑的合成路線如圖。請(qǐng)回答:
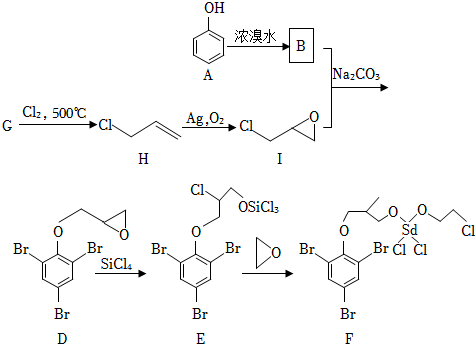
(1)化合物A轉(zhuǎn)化為B的化學(xué)方程式為,B的官能團(tuán)名稱是。
(2)G的結(jié)構(gòu)簡(jiǎn)式為,H的系統(tǒng)命名為。
(3)H→I的反應(yīng)類(lèi)型是。
(4)D的分子式為,反應(yīng)B+I→D中Na2CO3的作用是。
(5)D的逆合成分析中有一種前體分子C9H10O2,符合下列條件的該前體分子的同分異構(gòu)體有種。
①核磁共振氫譜有4組峰;
②能發(fā)生銀鏡反應(yīng);
③與FeCl3發(fā)生顯色反應(yīng)。組卷:3引用:2難度:0.3


