新人教版必修1高考題同步試卷:3.2 幾種重要的金屬化合物(01)
發(fā)布:2024/4/20 14:35:0
一、選擇題(共15小題)
-
1.下列金屬中,表面自然形成的氧化層能保護(hù)內(nèi)層金屬不被空氣氧化的是( )
A.K B.Na C.Fe D.Al 組卷:1494引用:67難度:0.9 -
2.下列有關(guān)NaClO和NaCl混合溶液的敘述正確的是( )
A.該溶液中,H+、NH4+、SO42-、Br-可以大量共存 B.該溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 C.向該溶液中滴入少量FeSO4溶液,反應(yīng)的離子方程式為:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O D.向該溶液中加入濃鹽酸,每產(chǎn)生1molCl2,轉(zhuǎn)移電子約為6.02×1023個 組卷:2962引用:37難度:0.5 -
3.下列有關(guān)說法正確的是( )
A.在酒精燈加熱條件下,Na2CO3、NaHCO3固體都能發(fā)生分解 B.Fe(OH)3膠體無色、透明,能產(chǎn)生丁達(dá)爾現(xiàn)象 C.H2、SO2、CO2三種氣體都可用濃H2SO4干燥 D.SiO2既能和NaOH溶液反應(yīng)又能和氫氟酸反應(yīng),所以是兩性氧化物 組卷:2064引用:24難度:0.9 -
4.下列有關(guān)物質(zhì)性質(zhì)的比較,錯誤的是( )
A.溶解度:小蘇打<蘇打 B.密度:溴乙烷>水 C.硬度:晶體硅<金剛石 D.碳碳鍵鍵長:乙烯>苯 組卷:869引用:15難度:0.9 -
5.某同學(xué)將光亮的鎂條放入盛有NH4Cl溶液的試管中,有大量氣泡產(chǎn)生,為探究該反應(yīng)原理,該同學(xué)做了以下實(shí)驗(yàn)并觀察到相關(guān)現(xiàn)象,由此得出的結(jié)論不合理的是( )
選項(xiàng) 實(shí)驗(yàn)及現(xiàn)象 結(jié)論 A 將濕潤的紅色石蕊試紙放在試管口,試紙變藍(lán) 反應(yīng)中有NH3產(chǎn)生 B 收集產(chǎn)生的氣體并點(diǎn)燃,火焰呈淡藍(lán)色 反應(yīng)中有H2產(chǎn)生 C 收集氣體的同時測得溶液的pH為8.6 弱堿性溶液中Mg也可被氧化 D 將光亮的鎂條放入pH為8.6的NaHCO3溶液中,有氣泡產(chǎn)生 弱堿性溶液中OH-氧化了Mg A.A B.B C.C D.D 組卷:1375引用:14難度:0.9 -
6.化學(xué)無處不在,與化學(xué)有關(guān)的說法不正確的是( )
A.侯氏制堿法的工藝過程中應(yīng)用了物質(zhì)溶解度的差異 B.可用蘸濃鹽酸的棉棒檢驗(yàn)輸送氨氣的管道是否漏氣 C.碘是人體必需微量元素,所以要多吃富含高碘酸的食物 D.黑火藥由硫磺、硝石、木炭三種物質(zhì)按一定比例混合制成 組卷:1902引用:25難度:0.9 -
7.向下列溶液滴加稀硫酸,生成白色沉淀,繼續(xù)滴加稀硫酸,沉淀又溶解的是( )
A.Na2SiO3 B.BaCl2 C.FeCl3 D.NaAlO2 組卷:500引用:21難度:0.9 -
8.足量下列物質(zhì)與等質(zhì)量的鋁反應(yīng),放出氫氣且消耗溶質(zhì)物質(zhì)的量最少的是( )
A.氫氧化鈉溶液 B.稀硫酸 C.鹽酸 D.稀硝酸 組卷:1155引用:51難度:0.9 -
9.為了除去MgCl2酸性溶液中的Fe3+,可在加熱攪拌的條件下加入一種試劑過濾后,再加入適量的鹽酸,這種試劑是( )
A.NH3?H2O B.NaOH C.Na2CO3 D.MgCO3 組卷:516引用:117難度:0.9 -
10.將適量鐵粉放入三氯化鐵溶液中,完全反應(yīng)后,溶液中的Fe3+和Fe2+濃度相等.則已反應(yīng)的Fe3+和未反應(yīng)的Fe3+的物質(zhì)的量之比是( )
A.2:3 B.3:2 C.1:2 D.1:1 組卷:1453引用:74難度:0.9
三、解答題(共11小題)
-
 29.檸檬酸亞鐵(FeC6H6O7)是一種易吸收的高效鐵制劑,可由綠礬(FeSO4?7H2O)通過下列反應(yīng)制備:FeSO4+Na2CO3═FeCO3↓+Na2SO4 FeCO3+C6H8O7═FeC6H6O7+CO2↑+H2O 下表列出了相關(guān)金屬離子生成氫氧化物沉淀的pH(開始沉淀的pH按金屬離子濃度為1.0mol?L-1計(jì)算)。
29.檸檬酸亞鐵(FeC6H6O7)是一種易吸收的高效鐵制劑,可由綠礬(FeSO4?7H2O)通過下列反應(yīng)制備:FeSO4+Na2CO3═FeCO3↓+Na2SO4 FeCO3+C6H8O7═FeC6H6O7+CO2↑+H2O 下表列出了相關(guān)金屬離子生成氫氧化物沉淀的pH(開始沉淀的pH按金屬離子濃度為1.0mol?L-1計(jì)算)。
(1)制備FeCO3時,選用的加料方式是金屬離子 開始沉淀的pH 沉淀完全的pH Fe3+ 1.1 3.2 Al3+ 3.0 5.0 Fe2+ 5.8 8.8 (填字母),原因是。
a.將FeSO4溶液與Na2CO3溶液同時加入到反應(yīng)容器中
b.將FeSO4溶液緩慢加入到盛有Na2CO3溶液的反應(yīng)容器中
c.將Na2CO3溶液緩慢加入到盛有FeSO4溶液的反應(yīng)容器中
(2)生成的FeCO3沉淀需經(jīng)充分洗滌,檢驗(yàn)洗滌是否完全的方法是。
(3)將制得的FeCO3加入到足量檸檬酸溶液中,再加入少量鐵粉,80℃下攪拌反應(yīng)。①鐵粉的作用是。②反應(yīng)結(jié)束后,無需過濾,除去過量鐵粉的方法是。
(4)最后溶液經(jīng)濃縮、加入適量無水乙醇、靜置、過濾、洗滌、干燥,獲得檸檬酸亞鐵晶體。分離過程中加入無水乙醇的目的是。
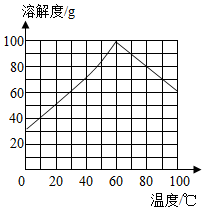
(5)某研究性學(xué)習(xí)小組欲從硫鐵礦燒渣(主要成分為Fe2O3、SiO2、Al2O3) 出發(fā),先制備綠礬,再合成檸檬酸亞鐵。請結(jié)合如圖的綠礬溶解度曲線,補(bǔ)充完整由硫鐵礦燒渣制備FeSO4?7H2O晶體的實(shí)驗(yàn)步驟(可選用的試劑:鐵粉、稀硫酸和NaOH溶液):向一定量燒渣中加入足量的稀硫酸充分反應(yīng),,得到FeSO4溶液,,得到FeSO4?7H2O 晶體。組卷:1115引用:13難度:0.1 -
30.現(xiàn)有一定量含有Na2O雜質(zhì)的Na2O2試樣。請從下圖中選用適當(dāng)?shù)膶?shí)驗(yàn)裝置,設(shè)計(jì)一個最簡單的實(shí)驗(yàn),測定Na2O2試樣的純度(可供選用的反應(yīng)物只有CaCO3固體,6摩爾/升鹽酸和蒸餾水)。
請?zhí)顚懴铝锌瞻祝?br />(1)寫出實(shí)驗(yàn)中Na2O2和Na2O分別發(fā)生反應(yīng)的化學(xué)方程式。
(2)應(yīng)選用的裝置是(只要求寫出圖中裝置的標(biāo)號)
(3)所選用裝置的連接順序應(yīng)是(填各接口的字母;連接膠管省略)。。組卷:88引用:13難度:0.5


